Механизмы развития (патогенез) неинфекционного васкулита
Основные иммунологические факторы, которые инициируют неинфекционный васкулит:
(1) отложение иммунных комплексов;
(2) наличие антинейтрофильных цитоплазматических антител;
(3) наличие антител к эндотелиальным клеткам.
а) Иммунные комплексы. Нарушения при отложении иммунных комплексов схоже с экспериментально индуцированными нарушениями, обусловленными иммунными комплексами, — реакцией Артюса и сывороточной болезнью.
Многие системные иммунные заболевания, например системная красная волчанка (СКВ) и узелковый полиартериит, проявляются как васкулит, опосредованный иммунными комплексами. В пораженных васкулитом тканях обычно выявляют антитела и компоненты системы комплемента, хотя природу антигенов, ответственных за их отложение, установить часто невозможно.
Можно обнаружить также комплексы антиген-антитело (например, ДНК-антиДНК при СКВ-ассоциированном васкулите), хотя чувствительность и специфичность тестов для определения циркулирующих иммунных комплексов являются низкими. Кроме того, иммунные комплексы играют определенную роль при следующих видах васкулитов:
- васкулите, опосредованном лекарственной гиперчувствительностью. В основе такого васкулита лежит образование иммунных комплексов. В некоторых случаях лекарственные средства (например, пенициллин) связываются с белками сыворотки. Другие агенты, такие как стрептокиназа, сами являются чужеродными белками. В обоих случаях антитела к белкам, модифицированным лекарственными средствами, или к чужеродным молекулам вызывают образование иммунных комплексов.
Клинические проявления широко варьируют, однако чаще всего наблюдаются в коже. Они могут быть слабыми и самокупирующимися или тяжелыми и даже фатальными. Васкулит, опосредованный лекарственной гиперчувствительностью, важно идентифицировать, т.к. прекращение использования лекарственного средства обычно приводит к купированию заболевания;
- васкулите, вторичном по отношению к вирусной инфекции. Антитела к вирусным белкам образуют иммунные комплексы, которые могут быть обнаружены в сыворотке и поражениях сосудов. Так, до 30% пациентов, страдающих узелковым полиартериитом (см. далее), инфицированы вирусом гепатита В; инфекция вызывает васкулит, обусловленный поверхностным антигеном вируса гепатита В (HBsAg) и антителами анти-HBsAg.
Во многих случаях остается неясным, образуются ли иммунные комплексы в каком-то другом месте, а затем откладываются в определенных сосудах или образуются in situ из присутствующего в сосудистой стенке антигена, с которым связываются циркулирующие антитела. Кроме того, нередко при этом виде васкулита комплексы антиген-антитело немногочисленны. Можно полагать, что ко времени постановки диагноза на основании исследования тканей иммунные комплексы в них уже отсутствуют или в патогенезе включаются какие-то другие механизмы.
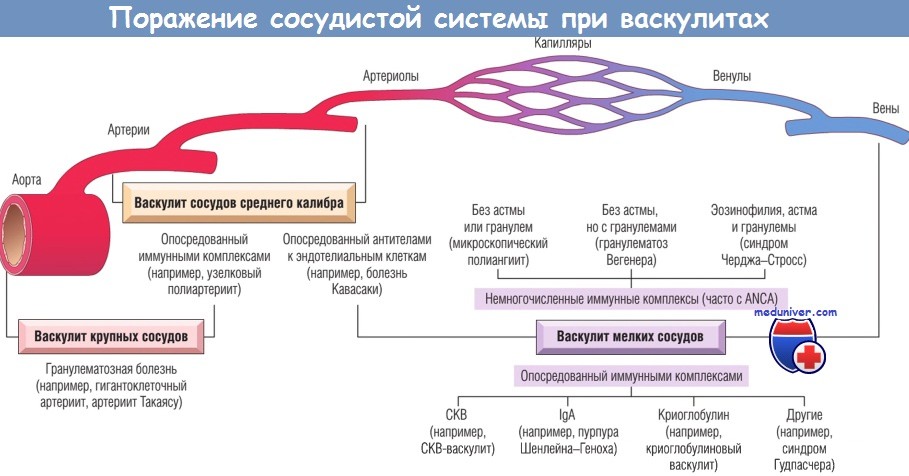
Обратите внимание на значительное перекрытие распределения.
ANCA — антинейтрофильные цитоплазматические антитела; Ig — иммуноглобулин; СКВ — системная красная волчанка
б) Антинейтрофильные цитоплазматические антитела. У многих пациентов с васкулитом обнаруживают циркулирующие антитела, реагирующие с антигенами цитоплазмы нейтрофилов, — антинейтрофильные цитоплазматические антитела (ANCA). Эти антитела составляют гетерогенную группу аутоантител, направленных против компонентов (главным образом ферментов) первичных гранул нейтрофилов, лизосом моноцитов и эндотелиальных клеток.
Ранее ANCA классифицировали соответственно их внутриклеточному распределению: цитоплазматические (с-ANCA) и перинуклеарные (p-ANCA). В настоящее время ANCA различают по антигенам-мишеням:
- антинейтрофильные цитоплазматические антитела к миелопероксидазе (MPO-ANCA). МРО — это компонент лизосомных гранул, в обычных условиях участвующий в образовании свободных радикалов кислорода. MPO-ANCA индуцируют разнообразные терапевтические агенты, в частности пропилтиоурацил. Эти антитела также называют p-ANCA;
- антинейтрофильные цитоплазматические антитела к протеиназе 3 (PR3-ANCA). PR3 является компонентом азурофильных гранул нейтрофилов и гомологична многочисленным микробным пептидам, что объясняет появление PR3-ANCA. Эти антитела также называют c-ANCA.
PR3-ANCA не обладают высокой специфичностью, но их обычно обнаруживают у пациентов с гранулематозом Вегенера. Присутствие MPO-ANCA характерно для микроскопического полиангиита и синдрома Черджа-Стросс. На связь определенных ANCA с заболеваниями также влияют расовые и географические особенности.
ANCA — полезный диагностический маркер при васкулитах, ассоциированных с этими антителами. Высота титра ANCA может отражать степень активности воспалительного процесса. Титр ANCA возрастает также при рецидивах заболевания. Тесная связь титров ANCA с активностью заболевания указывает на патогенетическую роль этих антител.
Точные механизмы такой зависимости неизвестны, однако ANCA могут непосредственно активировать нейтрофилы и тем самым стимулировать высвобождение реактивных метаболитов кислорода и протеолитических ферментов. Эти процессы в сосудах приводят к взаимодействию нейтрофилов с эндотелиальными клетками и последующему повреждению эндотелия.
Кроме того, антигены для ANCA локализуются в основном внутриклеточно, поэтому труднодоступны для циркулирующих антител. В настоящее время накапливается все больше данных о том, что специфичные для ANCA антигены либо конститутивно присутствуют в небольшом количестве на плазматической мембране, либо транслоцируются на клеточную поверхность активированных и подвергающихся апоптозу нейтрофилов.
Предполагаемый механизм васкулита, ассоциированного с ANCA, можно представить следующим образом:
- лекарственные средства или перекрестно реагирующие антигены микроорганизмов индуцируют образование ANCA. С другой стороны, стимулировать образование ANCA (при соответствующем уровне чувствительности организма) может экспрессия PR3 и МРО на клеточной поверхности или их высвобождение нейтрофилами (например, в случае инфекции);
- последующая инфекция, действие эндотоксинов или другие воспалительные стимулы вызывают продукцию цитокинов, например TNF, индуцирующих поверхностную экспрессию PR3 и МРО нейтрофилами и клетками других типов;
- ANCA реагируют с клетками, активированными этими цитокинами, и либо прямо повреждают клетки (например, эндотелиальные), либо индуцируют дальнейшую активацию клеток (например, нейтрофилов);
- активированные ANCA нейтрофилы дегранулируют и высвобождают реактивные метаболиты кислорода, токсичные для эндотелиальных клеток, непосредственно повреждая эндотелий и опосредованно — другие ткани.
Следует отметить, что у некоторых пациентов с воспалительными заболеваниями, но в отсутствие васкулита (в частности, при воспалительном заболевании кишечника, первичном склерозирующем холангите, ревматоидном артрите) обнаруживают ANCA не к PR3 и МРО, а к другим компонентам.
в) Антитела к эндотелиальным клеткам. Присутствие этих антител может предрасполагать к развитию определенного вида васкулитов, например болезни Кавасаки.
Далее кратко рассмотрим наиболее изученные васкулиты, опять же подчеркивая, что между ними существует значительный перекрест симптомов. Кроме того, необходимо иметь в виду, что у некоторых пациентов с васкулитом отсутствуют классические признаки, которые позволили бы отнести заболевание к определенному виду.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) гигантоклеточного артериита"
Оглавление темы "Васкулиты":- Клиника расслоения аорты
- Классификация (виды) васкулитов
- Механизмы развития (патогенез) неинфекционного васкулита
- Механизмы развития (патогенез) гигантоклеточного артериита
- Механизмы развития (патогенез) артериита Такаясу
- Механизмы развития (патогенез) узелкового полиартериита
- Механизмы развития (патогенез) болезни Кавасаки
- Механизмы развития (патогенез) микроскопического ангиита
- Механизмы развития (патогенез) синдрома Черджа-Стросса
- Механизмы развития (патогенез) гранулематоза Вегенера

