Интрацитоплазматическая инъекция сперматозоидов (ИЦИС). Методика
Интрацитоплазматическая инъекция сперматозоидов (ИЦИС) заключается во введении одного сперматозоида непосредственно в цитоплазму ооцита. Данный метод был впервые успешно применен к ооциту человека в 1994 г. и с тех пор коренным образом изменил лечение бесплодия с выраженным мужским фактором.
Инъекция сперматозоида в цитоплазму яйцеклетки позволяет опустить многие шаги при обработке спермы и предварительные приготовления, не снижая показателей оплодотворений. В настоящее время идут споры о том, когда следует проводить интрацитоплазиматическую инъекцию сперматозоидов (ИЦИС).
Некоторые программы используют этот метод довольно свободно, в то время как другие остаются более консервативными. Следующие показания для проведения интрацитоплазматической инъекции сперматозоидов (ИЦИС) подтверждены опытным путем.
• Пара уже обращалась к традиционной инсеминации, однако безрезультатно.
• Общая концентрация подвижных сперматозоидов менее 10 млн/мл.
• Морфологически среди сперматозоидов присутствует менее 4% нормальных форм по точному критерию (может зависеть от других параметров спермы, таких как концентрация, подвижность и объем).
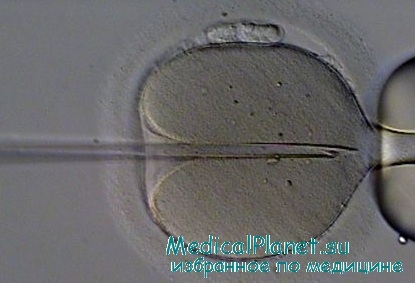
Техника интрацитоплазматической инъекции сперматозоидов (ИЦИС)
Оборудование для интрацитоплазматической инъекции сперматозоидов (ИЦИС), как и для любой другой процедуры микроманипуляции, состоит из инвертированного фазово-контрастного микроскопа с микроманипуляторами и инъекторами, позволяющими осуществлять манипуляции и клеточную хирургию. Стадия нагревания при использовании микроскопа рекомендована для поддержания постоянной температуры, хотя некоторые группы показывают весьма приемлемый результат без применения стадии нагревания при микроманипуляции.
Гидравлическая система в микроманипуляторе должна работать с максимальной точностью, а микроскоп следует закреплять в очень стабильном положении.
Удаление кумулюса и corona radiata, окружающих яйцеклетку (десорбирование), — важный этап интрацитоплазматической инъекции сперматозоидов (ИЦИС). Кумулюсные клетки следует удалить, чтобы они не препятствовали наблюдению за яйцеклеткой и инъекции. Можно использовать две иглы для отделения большинства кумулюсных клеток путем «срезания» кумулюса, оставляя лишь несколько клеток с гаметой. Ооциты, уже почти освобожденные от кумулюсных клеток, можно подвергнуть 30-секундному воздействию раствора обрабатывающей среды, содержащему 80 МЕ/мл гиалу-ронидазы и добавляющемуся вручную пипеткой, чтобы удалить оставшиеся клетки.
Затем ооциты сразу же промывают в обрабатывающей среде без гиалуронидазы, снова добавляемой при помощи пипетки с внутренним диаметром немного больше ооцита.
Сосуды для инъекции могут быть подготовлены разными способами. Процедуру можно осуществить в 5 мкл обрабатывающей среды с добавлением протеина и покрытием из минерального масла в небольшой чашке Петри. 5 мкл 7% раствора повидона в обрабатывающей среде можно поместить в центр сосуда для интрацитоплазматической инъекции сперматозоидов (ИЦИС).
Непосредственно перед инъекцией в каплю повидона добавляют около 1 мкл суспензии сперматозоидов. Высокая вязкость этого раствора замедляет движение сперматозоидов и упрощает их обездвиживание и аспирацию. Кроме того, она предотвращает прилипание сперматозоидов к внутренней поверхности инъекционной пипетки. Во время инъекции десорбированные ооциты помещают в раствор в соотношении 1 ооцит на каплю около 5 мкл раствора повидона, содержащего обработанные сперматозоиды.
Следует добавлять в сосуд не более двух яйцеклеток одновременно во избежание длительного воздействия окружающей среды вне инкубатора.
С помощью инъекционной пипетки сперматозоиды извлекают из капли. Обнаруживают подвижный сперматозоид с нормальной морфологией, и при помощи инъекционной пипетки отсекают хвост. Затем сперматозоид аспирируют в пипетку, начиная с хвоста, подготавливая к интрацитоплазматической инъекции сперматозоидов (ИЦИС), и помещают пипетку в каплю с ооцитом.
Удерживающую пипетку применяют для манипуляций с яйцеклеткой в положении с полярным тельцем под углом 12 или 6 ч условного циферблата. К пипетке прилагают давление для удержания ооцита на месте во время инъекции. Инъекционную пипетку располагают в соответствии с внешней границей оволеммы на экваториальной плоскости, соответствующей 3 ч условного циферблата.
Затем сперматозоид перемещают на кончик пипетки, которым надавливают на вителлиновый слой. Иглу вводят в вителлиновый слой и оволемму. Когда кончик пипетки проникает в оволемму, осторожно аспирируют небольшое количество овоплазмы, чтобы удостовериться в разрыве мембраны. Затем сперматозоид вводят в цитоплазму яйцеклетки, а пипетку извлекают. Следует избегать инъекций чрезмерного количества среды.
- Рекомендуем далее ознакомиться со статьей "Оценка оплодотворения ооцита при ЭКО. Критерии"
Оглавление темы "Анализ спермы, ооцитов":- Хирургический забор спермы. Микрохирургическая эпидидимальная аспирация спермы (MECA)
- Тестикулярный забор-аспирация спермы (ТЕСА). Микроскопический тестикулярный забор спермы (микроТЕСА)
- Консервация сперматозоидов. Обработка ооцитов при ЭКО
- Забор яйцеклетки при ЭКО. Оценка состояния ооцита
- Созревание ооцитов in vitro при ЭКО. Гормоны
- ЭКО. Традиционное оплодотворение
- Интрацитоплазматическая инъекция сперматозоидов (ИЦИС). Методика
- Оценка оплодотворения ооцита при ЭКО. Критерии
- Оценка состояния эмбриона при ЭКО. Критерии
- Культивирование эмбриона при ЭКО. Вспомогательное инкубирование

