Забор яйцеклетки при ЭКО. Оценка состояния ооцита
Перед забором яйцеклетки необходимо подготовить лабораторию, чтобы обеспечить оптимальные условия для быстрого, эффективного и безопасного забора ооцита и помещения его в инкубатор. Правильная подготовка сводит к минимуму воздействие окружающей среды на ооцит вне инкубатора.
Условия в палате перед забором яйцеклетки. Перед забором яйцеклетки важно удостовериться, что условия в лаборатории стабильны. Все поверхности должны быть чистыми, температура нагревательных блоков должна составлять 37 °С, то есть совпадать с температурой катетеров, используемых для извлечения фолликулярной жидкости. Рекомендуют перед применением прополоскать все пипетки и сосуды в культуральной среде.
Среды для яйцеклеток. Рекомендуют готовить обрабатывающую и культуральную среды за день до забора яйцеклетки. Сосуды для культуральной среды следует готовить и хранить в инкубаторе с углекислым газом накануне процедуры. Обрабатывающую среду перед использованием необходимо нагревать на водяной бане или в сухом инкубаторе. При выполнении процедур вспомогательных репродуктивных технологий (ВРТ) следует поддерживать температуру среды 37 °С.
Забор ооцита. Необходимо подготовить пробирки, содержащие обрабатывающую среду и препарат гепарина для предотвращения коагуляции. Не нарушая стерильности, их помещают в нагревательный блок в палате, где будет производиться забор. Извлеченную фолликулярную жидкость помещают в обрабатывающую среду при температуре 37 °С, содержащую белок, а затем сразу же доставляют в лабораторию.
В лаборатории проводят экспресс-анализ пунктата на наличие ооцит-кумулюсных комплексов. После обнаружения ооцита его ополаскивают обрабатывающей средой, быстро градуируют и помещают в предварительно уравновешенный сосуд с культуральной средой в инкубаторе с углекислым газом. Все это нужно делать быстро. В том случае, если лаборатория расположена далеко от палаты, где проводят забор ооцита, следует использовать передвижное оборудование и проводить поиск яйцеклетки в палате, где осуществляли ее забор, а также использовать такое оборудование для транспортировки ооцитов в лабораторию. Обычно в этих целях используют транспортный ламинал, оборудованный микроскопом.
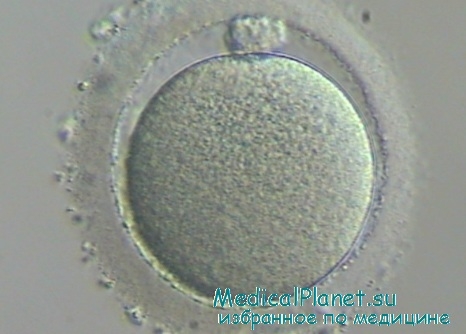
Оценка состояния ооцита
Ооцит-кумулюсные комплексы подсчитывают перед инкубацией. Точное определение степени зрелости ооцитов на момент забора помогает при расчете времени оплодотворения, а также вероятности успеха; кроме того, могут быть выявлены какие-либо отклонения. Первичная оценка ооцита основана на непосредственном визуальном анализе морфологии ооцит-кумулюсного комплекса. Оценка основана на характеристиках кумулюса и corona radiata. Первый осмотр следует проводить быстро, во время поиска ооцита в фолликулярной жидкости. При ЭКО с традиционной инсеминацией яйценосный холмик не удаляют перед оплодотворением, таким образом, возможности наблюдения ограничены.
Незрелые ооциты определяют как находящиеся в стадии мейоза, предшествующей метафазе второго деления мейоза. В их число входят ооциты в профазе I деления мейоза, определяемые по наличию зародышевого пузырька или ядерной оболочки в цитоплазме и отсутствию направительного тельца в перивителлиновом пространстве. Если кумулюс и corona radiata присутствуют, обычно они сильно уплотнены. При продолжении профазы I ооцит вступает в метафазу первого деления мейоза. Эта промежуточная стадия зрелости определяется исчезновением зародышевого пузырька и отсутствием первого полярного тельца. В ооцитах в стадии I деления мейоза яйценосный холмик может быть увеличен, но corona radiata все еще находится в сжатом виде.
Экструзия первого полярного тельца обозначает переход ооцита к зрелости, т.е. к стадии II деления меиоза. Ооциты в этой стадии мейоза обычно обладают полностью развитым кумулюсом. В норме ооцит остается в стадии II мейоза до оплодотворения, когда второе деление мейоза продолжается, происходит экструзия второго направительного тельца, формируются мужской и женский пронуклеусы.
Гистологическое исследование ооцита после удаления кумулюса позволяет оценить его морфологически. Следует учитывать внешний вид цитоплазмы, вителлинового слоя, полярного тельца. Гомогенная цитоплазма с однородным цветом и гранулярностью, занимающая большую часть пространства внутри вителлинового слоя, свидетельствует о хорошем качестве ооцита. Вакуоли, темную окраску, сжатую форму или гранулярность расценивают при анализе морфологического качества ооцита как негативные признаки. Рассмотрение формы и толщины вителлинового слоя может оказаться важным; в стадии развития не должно быть трещин, и толщина его должна быть соответствующей.
Существует множество систем оценки морфологии ооцита. Приведенная ниже система — пример оценки на основе внешнего вида:
• 0. Атретический ооцит, дегенерация.
• 1. Есть зародышевый пузырек. Ооцит еще очень незрелый.
• 2. Corona radiata плотный/темный, но зародышевый пузырек отсутствует. Кумулюс начинает отслаиваться, но ооцит сложно разглядеть, он еще незрелый.
• 3. Corona radiata сияет и освобождается, яйценосный холмик свободен и рассеян. Ооцит можно различить, но первое полярное тельце до сих пор отсутствует. Ооцит незрелый, велика вероятность экструзии полярного тельца в ближайшее время.
• 4. Оптимальный уровень зрелости для осуществления оплодотворения. Кумулюс полностью развит, первое полярное тельце просматривается.
- Рекомендуем далее ознакомиться со статьей "Созревание ооцитов in vitro при ЭКО. Гормоны"
Оглавление темы "Анализ спермы, ооцитов":- Хирургический забор спермы. Микрохирургическая эпидидимальная аспирация спермы (MECA)
- Тестикулярный забор-аспирация спермы (ТЕСА). Микроскопический тестикулярный забор спермы (микроТЕСА)
- Консервация сперматозоидов. Обработка ооцитов при ЭКО
- Забор яйцеклетки при ЭКО. Оценка состояния ооцита
- Созревание ооцитов in vitro при ЭКО. Гормоны
- ЭКО. Традиционное оплодотворение
- Интрацитоплазматическая инъекция сперматозоидов (ИЦИС). Методика
- Оценка оплодотворения ооцита при ЭКО. Критерии
- Оценка состояния эмбриона при ЭКО. Критерии
- Культивирование эмбриона при ЭКО. Вспомогательное инкубирование

