Консервация сперматозоидов. Обработка ооцитов при ЭКО
Криоконсервация сперматозоидов человека стала перспективным методом хранения с тех пор, как в 1949 г. Полдж при проведении исследований на домашней птице обнаружил, что сперматозоиды можно защитить от переохлаждения путем добавления глицерола. Вскоре после этого Шерман описал успешную криоконсервацию, размораживание человеческих сперматозоидов и последующее успешное зачатие.
С тех пор огромное количество исследований сосредоточено на изучении физических и химических изменений, происходящих при замораживании, а также на оценке методов и веществ для оптимальной криоконсервации. Хотя многие усовершенствованные аспекты криобиологии выходят за пределы вопросов данного текста, несколько основных принципов необходимо рассмотреть.
Криоконсервация стала важной частью вспомогательных репродуктивных технологий (ВРТ). Пациенты с эякуляторной дисфункцией, которым требуется вибростимуляция или электроэякуляция, могут заморозить сперматозоиды и использовать аликвоты спермы для попыток оплодотворения несколько циклов спустя, не прибегая повторно к процедуре забора сперматозоидов.
Криоконсервация сперматозоидов, извлеченных хирургическим путем, рекомендована для использования в последующих циклах ЭКО и ИЦИС во избежание необходимости повторного проведения процедур. Оплодотворение спермой донора основано на длительном и надежном хранении большого количества образцов спермы. Пациенты, столкнувшиеся с лечением, способным негативно отразиться на фертильности, могут выбрать хранение сперматозоидов для использования в будущем.

Обработка ооцитов при ЭКО
Успехи в области производства культуральной среды значительно повлияли на качество эмбрионов и частоту наступления беременности. Все средства, используемые в ВРТ, теперь есть в продаже. Перед использованием необходимо протестировать их на наличие токсинов и способность поддерживать рост и развитие эмбриона. Открывать средства следует только в вытяжном шкафу с ламинарным потоком, следя за поддержанием стерильности при добавлении протеина.
После какой-либо подготовки среды или добавления компонентов следует профильтровать ее, чтобы гарантировать стерильность.
Для получения наилучших результатов при выполнении всех процедур особое внимание следует уделять подготовке лаборатории. Желательно, чтобы лаборатория располагалась как можно ближе к палате, в которой осуществляют забор яйцеклетки и пересадку эмбриона. Необходимо контролировать окружающую среду, не допуская присутствия токсинов.
Также для лаборатории рекомендуют приточно-вытяжную вентиляцию, регулируют температуру и освещение. Вытяжной шкаф с ламинарным потоком необходим для подготовки среды и манипуляций с гаметами и зародышами.
Все оборудование лаборатории ЭКО необходимо ежедневно проверять на исправность. Жесткая программа контроля качества очень важна для гарантии устойчивых результатов в эмбриологической лаборатории. Все среды, оборудование и другие материалы (сосуды и пипетки), контактирующие с гаметами и зародышами, должны быть биологически совместимы с эмбрионами млекопитающих.
Тестирование зародыша мыши может выявить наличие токсинов, субоптимального качества и субоптимальных условий культивирования. Тест заключается в культивировании зародыша мыши со стадии зиготы до уровня бластоцисты в условиях лаборатории.
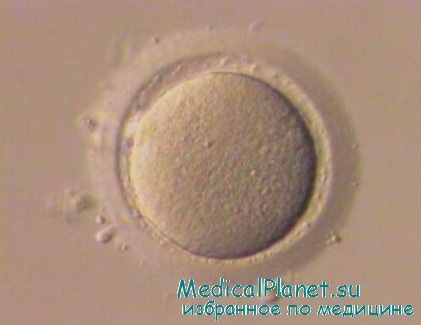
Лабораторное обеспечение обработки ооцитов
В процедурах вспомогательных репродуктивных технологий (ВРТ) применяют два основных типа среды: раствор, используемый при извлечении гамет и эмбрионов из инкубатора с углекислым газом, и культуральную среду, применяемую при культивировании в инкубаторе с углекислым газом. Обе среды состоят из комбинации питательных веществ, необходимых для поддержания раннего метаболизма зародыша, подходящего рН и осмолярности.
Следует также добавить источник протеина, например альбумин или синтетическую сыворотку, в соотношении 2-15 мг/л. Добавление протеина важно не только для стабильности рН и осмолярности, оно упрощает манипуляции с ооцитами и зародышами, снижая естественное взаимодействие клеток с поверхностями.
Среда для сбора ооцитов представляет собой модифицированную культуральную среду с добавлением буферного раствора, называемого HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота), способного поддерживать рН в стабильном состоянии вне инкубатора с углекислым газом. Однако HEPES изменяет деятельность ионных каналов в плазматической мембране и может обладать некоторой токсичностью в зависимости от концентрации, температуры и времени воздействия. По этой причине рекомендуют минимизировать время контакта клеток с буферным раствором HEPES.
Чтобы предотвратить образование сгустков свернувшейся крови при использовании обрабатывающей среды во время забора яйцеклетки, рекомендуют добавлять в среду антикоагулянт, например препарат гепарина, в небольшой концентрации. Сгустки могут затруднить визуализацию ооцит-кумулюсного комплекса.
Среда для культивирования зародышей обычно содержит буферный раствор бикарбоната и находится в инкубационной камере. Важно поддерживать стабильную температуру и рН в данной среде, так как зародыши крайне чувствительны к изменениям этих факторов. Культуральную среду, применяемую при развитии эмбрионов в инкубационных камерах до использования помещают в камеру с углекислым газом.
Для увеличения стабильности рН, если сосуд временно находится вне камеры с углекислым газом, а также для предотвращения испарения рекомендуют покрывать среду минеральным маслом. Это препятствует попаданию летучих органических смесей, которые могут быть токсичны для эмбриона, из воздуха.
- Рекомендуем далее ознакомиться со статьей "Забор яйцеклетки при ЭКО. Оценка состояния ооцита"
Оглавление темы "Анализ спермы, ооцитов":- Хирургический забор спермы. Микрохирургическая эпидидимальная аспирация спермы (MECA)
- Тестикулярный забор-аспирация спермы (ТЕСА). Микроскопический тестикулярный забор спермы (микроТЕСА)
- Консервация сперматозоидов. Обработка ооцитов при ЭКО
- Забор яйцеклетки при ЭКО. Оценка состояния ооцита
- Созревание ооцитов in vitro при ЭКО. Гормоны
- ЭКО. Традиционное оплодотворение
- Интрацитоплазматическая инъекция сперматозоидов (ИЦИС). Методика
- Оценка оплодотворения ооцита при ЭКО. Критерии
- Оценка состояния эмбриона при ЭКО. Критерии
- Культивирование эмбриона при ЭКО. Вспомогательное инкубирование

