Местные ретиноиды: механизм действия, фармакология
Местные ретиноиды - краткий обзор:
- Определение: любая молекула, которая сама по себе или посредством метаболической трансформации связывает или активирует рецепторы ретиновой кислоты.
- Ретиноидные рецепторы: активируемые лигандом факторы транскрипции.
- Преобладающие в коже человека ретиноидные рецепторы: γ-рецептор ретиноевой кислоты (RAR-γ) и ретиноидный X рецептор а (RXR-α).
- Гетеродимеры RAR-γ/RAR-α связываются с чувствительными к ретиноевой кислоте элементами и отвечают за ретиноидную сигнализацию.
- Клиническое применение местных ретиноидов:
- Показания по инструкции — акне, псориаз, кожная Т-клеточная лимфома, саркома Капоши, мелазма и фотостарение кожи.
- Показания вне инструкции по благоприятным результатам клинических испытаний — поствоспалительные гиперпигментации, ранние стрии и естественное старение кожи.
- Местное раздражение кожи: главным образом вследствие вызываемой ретиноидами гиперплазии эпидермиса. Клинические назначения следует регулировать с учетом тяжести местных реакций.
Ретиноиды используются в местных препаратах как медицинского, так и косметического назначения. В одних продуктах используются ретиноиды естественного происхождения, в других — синтетические молекулы. Все ретиноиды, однако, обладают предсказуемым фармакологическим действием, которое проявляется в инициации ответных реакций на коже человека и объясняется тем, что внутриядерные рецепторы ретиноидов действуют как факторы транскрипции.
Действительно, открытие и описание рецепторов ретиноевой кислоты (RAR) и ретиноидных X рецепторов (RXR) явилось поворотным пунктом в понимании механизма действия ретиноидов и натолкнуло на предположение о том, что ретиноиды действуют подобно гормонам. В 1976 г. Michael Spom и соавт. первоначально определили ретиноиды как группу, включающую как природные вещества с активностью витамина А, так и синтетические аналоги ретинола. Эта концепция уже не соответствует действительности. В настоящее время ретиноид определяется как любая молекула, которая сама по себе или в результате метаболической конверсии связывает и активирует рецепторы ретиноевой кислоты, возбуждая таким образом транскрипционную активность чувствительных к ретиноевой кислоте генов, что приводит к специфическим биологическим реакциям.
а) Механизм действия:
1. Ретиноидные рецепторы. Открытие рецепторов ретиноевой кислоты и описание этих рецепторов, как обладающих молекулярными признаками, похожими на рецепторы стероидных/тиреоидных гормонов, явилось знаковым событием. Общей для этих рецепторов характеристикой является то, что они связываются с регуляторными участками в ДНК, которые называют элементами гормонального ответа или целевыми последовательностями, и активируют лиганд-зависимую транскрипцию генов. Поэтому их называют факторами лиганд-зависимой (или гормонозависимой) транскрипции. Эти рецепторы связываются со специфическими последовательностями ДНК как димеры. В отличие от рецепторов стероидных гормонов, которые образуют гомодимеры (два идентичных мономера), рецептор RAR, рецептор витамина D (VDR) и рецептор тиреоидных гормонов TR связываются со своими элементами с большей аффинностью как гетеродимеры (два различных мономера).
Важным партнером для гетеродимеризации и последующего функционирования RAR, VDR и TR является RXR, физиологическим лигандом которого является 9-cis ретиноевая кислота. Способность RXR-рецепторов взаимодействовать с несколькими рецепторами указывает на их важность как регуляторных белков. Имеются три различных рецептора в семействе RAR (α, β и γ) и в семействе RXR (α, β и γ), каждый из них кодируется различными генами. Кроме того, каждый из рецепторов имеет изоформы, что дополнительно разнообразит спектр ретиноидных рецепторов.
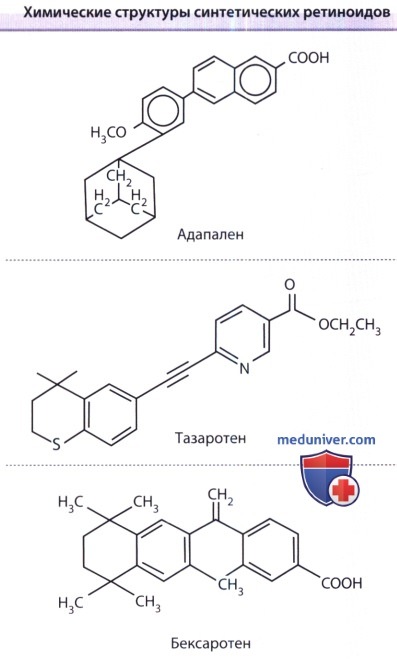
2. Ретиноиды с рецепторной селективностью. Идентификация и описание функциональной характеристики семейств ретиноидных рецепторов проложили путь к открытию лекарств. Синтетические молекулы можно было проверять на способность связывать и активировать определенные рецепторы. У многих из подобных веществ отсутствует структурное сходство с полностью транс-ретинолом или ретиноевой кислотой, но они все же считаются ретиноидами, поскольку способны активировать рецепторы, реализуя таким образом ретиноидный эффект. Адапален и тазаротен представляют собой два синтетических ретиноида, которые удовлетворяют этому описанию и которые применялись у людей как местные лекарства. Адапален имеет ограниченную рецепторную специфичность, обладая слабой аффинностью к RAR-α, более высокой аффинностью к RAR-β и γ при отсутствии взаимодействия с RXR-α.
Тазаротен не может прямо связываться с рецепторами RAR или RXR. Однако его метаболит, тазаротеновая кислота, обладает рецепторной селективностью к рецепторам RAR (RAR-β> RAR-γ > RAR-α) и является главной активной формой. Бексаротен — это селективный к рецептору RXR ретиноид (рексиноид), который в 100 раз активнее связывается с RXR, чем с рецептором RAR.
3. Ретиноидные рецепторы в коже человека. Системный анализ сравнительных уровней RAR и RXR в коже человека показывает, что в эпидермисе человека экспрессированы RAR-α, RAR-γ, RXR-α и матричные РНК (mRNAs) рецепторов RXR-β. Эти сравнительные уровни матричных РНК ретиноидных рецепторов являются отражением сравнительных уровней белков. Общее количество RXR-рецепторов в ядрах эпидермальных клеток человека в пять раз больше чем RAR-рецепторов. Среди RAR-белков 87% составляют RAR-γ и 13% RAR-α, при этом RAR-β не определяется. Среди RXR-белков 90% составляют RXR-α. Более того, только гетеродимеры RXR-α и RAR (в основном у) связываются с чувствительными к ретиноевой кислоте элементами (RAREs). При физиологических уровнях рецепторов RAR и RXR в коже человека они связывают RAREs как гетеродимеры и трансактивируют эти чувствительные элементы в ответ на лиганды RAR, но не RXR. Однако ключевым является рецептор RXR, поскольку гетеродимер не связывается с RARE без присутствия RXR-белка.
Облучение кожи человека ультрафиолетовым светом вызывает быстрое и значительное уменьшение ретиноидных рецепторов как RAR-γ, так и RXR-α. Хотя такое уменьшение уровней рецепторов временное, и через два дня уровни восстанавливаются до прежнего состояния, УФ-облучение приводит к функциональному нарушению зависящей от рецепторов чувствительности кожи человека к ретиноидам. Интересно отметить, что предварительное, до УФ-облучения, лечение кожи полностью транс-ретиноевой кислотой уменьшает потерю рецепторов и ускоряет их восстановление.
4. Целевые гены ретиноидов и каскад их активации в коже человека. Действие ретиноидов опосредуется в основном, если не исключительно, ретиноидными рецепторами. Учитывая, что эти рецепторы являются факторами транскрипции, итоговое воздействие ретиноидов на кожу (изменения в фенотипе) должно осуществляться через регулируемую экспрессию генов. Самым известным механизмом, посредством которого ретиноидные рецепторы модулируют экспрессию гена, является активация ретиноидных целевых генов путем прямой связи с RAREs в промоутере гена, что стимулирует механизм базальной транскрипции. В коже клеточный белок II, связывающий ретиноевую кислоту (CRABP), а также клеточный белок, связывающий ретинол (CRBP), 4-гидроксилаза ретиноевой кислоты (СУР26) и кератин 6 (все они содержат RAREs) регулируются полностью транс-ретиноевой кислотой.
Однако продукты этих генов, вероятно, не являются эффекторами ретиноидного ответа и, значит, не ответственны за плеотропные эффекты ретиноидов в коже. Несомненно, будут идентифицированы дополнительные гены, регулируемые элементами RARE, кодирующие белки, прямо или косвенно функционирующие как модуляторы роста и дифференцировки кожи. Вероятен также сценарий, когда эти белковые продукты, в свою очередь, активируют другие, не содержащие RARE гены в каскадной реакции и вызывают в коже клинические признаки действия ретиноидов.
Описание молекулярных процессов, ответственных за утолщение эпидермиса как наиболее выразительную гистологическую характеристику кожи, получавшей лечение полностью транс-ретиноевой кислотой, иллюстрирует вышеизложенную концепцию. Причиной гиперплазии эпидермиса является усиленная пролиферация базальных кератиноцитов. Отмечается также увеличение маркеров дифференцировки инволюкрина, лориклина, филаггрина и эпидермальной трансглютаминазы. Эти эпидермальные изменения в совокупности приводят к шелушению и отторжению чешуек. Такой гиперпролиферативный ответ эпидермиса на ретиноевую кислоту осуществляется посредством ядерного рецептора. Существенное значение среди регулируемых ретиноидными рецепторами генов, участвующих в контроле клеточного роста, имеют лиганды рецептора эпидермального фактора роста (EGF). В коже человека in vivo местная ретиноевая кислота индуцирует гепарин-связывающий EGF(HB-EGF) и амфирегулин (AR), которые стимулируют рост базальных клеток посредством активации поверхностного рецептора EGF. Интересно отметить, что ни HB-EGF, ни AR не содержат элементов RARE. Поэтому не представляется вероятной прямая модуляция HB-EGF и AR со стороны RARE. Скорее рецепторы RAR/RXR сами регулируют другие факторы транскрипции, которые, в свою очередь, регулируют экспрессию генов AR и HB-EGF. Эти факторы транскрипции еще предстоит идентифицировать.
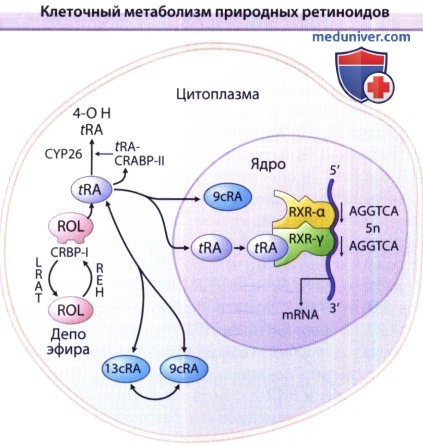
Ретинол (ROL), поступающий в клетку, связывается с клеточным белком I (CRBP-связывающий ретинол клеточный белок).
Ретинол может подвергаться этерификации посредством лецитин-ретинол-ацетилглронсферазы (LRAT) и накапливаться в форме ретинол-эфиров.
Гидролиз ретинол-эфира его гидролазой (REH) дает свободный ROL. Последующее окисление ROL производит ретиноевую ксилоту RA, которая связывается с клеточным белком CRABP (клеточный белок, связывающий ретиноевую кислоту).
Полностью транс-ИА (fRA) путем изомеризации преобразуется в 9-cis-RA (9cRA).
В процессе гидроксилирования транс-ретиноевой кислоты (fRA) посредством CYP26 (ферментом цитохрома Р450) генерируется 4-ОН RA, который находится в сравнительно неактивном состоянии.
RAR и RXR-внутриядерные рецепторы ретиноидов. В коже человека гетеродимеры RAR-γ и RXR-α, связанные с чувствительными к RA элементами (такими как прямые повторы AGGTCA) трансдуцируют действие ретиноидов в присутствии RAR-лигандов.
б) Фармакология:
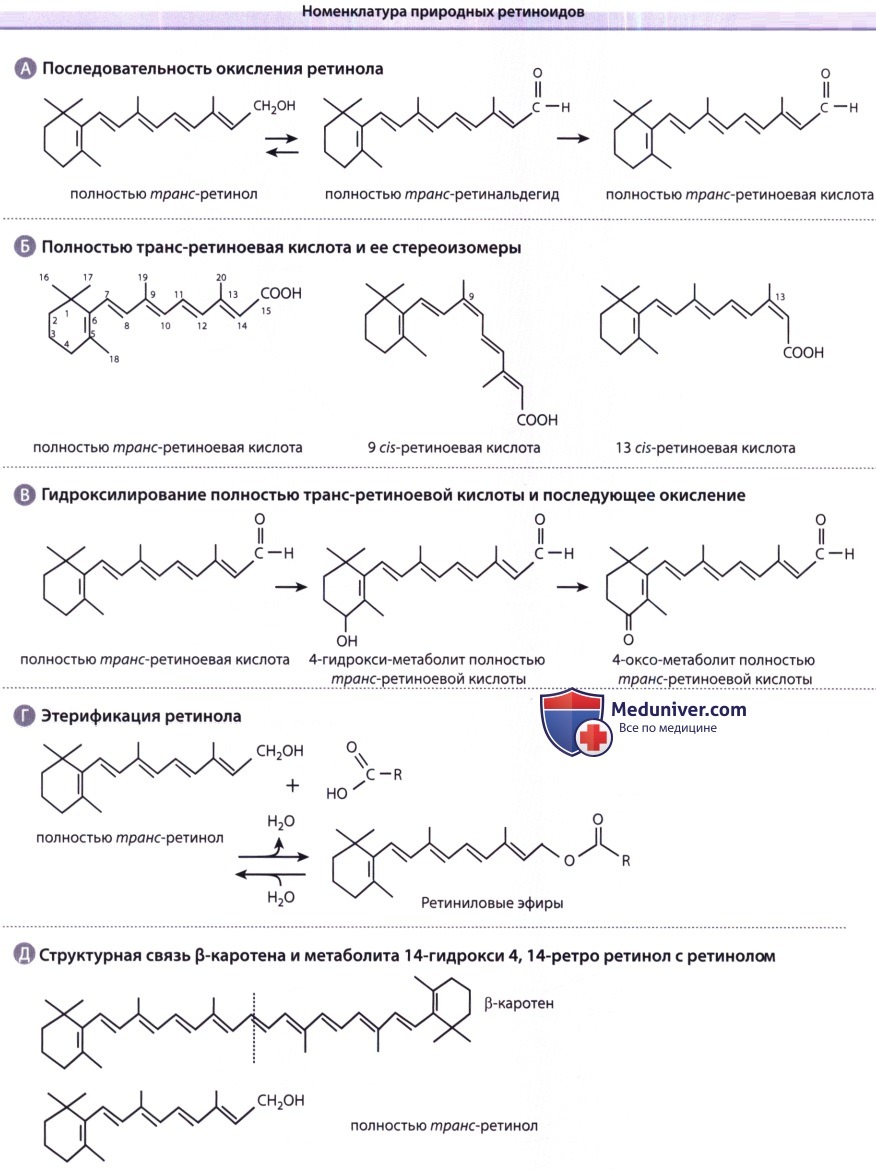
1. Номенклатура. Полностью транс-ретиноевая кислота (третиноин), которая связывается с рецепторами RAR и активирует их, является производным продуктом последовательного окисления полностью транс-ретинола (или витамина А) и полностью транс-ретинальдегида. Это молекула с 20-атомами углерода, которая содержит циклогексановое кольцо, боковую цепочку с четырьмя двойными связями (все в транс-конфигурации) и концевую группу карбоксильной кислоты. Нумерация атомов углерода показана на рисунке ниже. Термины «9-cis- и 13-cis-ретиноевая кислота» относятся к стереоизомерам полностью транс-ретиноевой кислоты, в которых двойная связь начинается с девятого и тринадцатого атомов углерода соответственно, находится в cis-, а не в транс-конфигурации. 9-цис-ретиновевая кислота связывается с рецептором RXR-α с высокой аффинностью, при этом она в 40 раз активнее, чем полностью транс-ретиноевая кислота на RXR-α. 9-цис-ретиноевая кислота может также связываться с рецепторами RAR и поэтому иногда называется панагонистом ретиноидных рецепторов.
Четвертый атом углерода расположен в циклогексановом кольце полностью транс-ретиноевой кислоты и участвует в реакции гидроксилирования для производства 4-гидрокси-метаболита полностью транс-ретиноевой кислоты. Добавление гидроксильной группы к циклогексановому кольцу делает молекулу более полярной и более податливой для выделения/элиминации из клеток и организмов. Биологически она также гораздо менее активна. 4-гидрокси-метаболит полностью транс-ретиноевой кислоты может далее окисляться в 4-оксо-метаболит ретиноевой кислоты.
Группа веществ, которую называют ретиниловыми эфирами, функционирует как молекулярная форма накопления ретинола. Эти вещества образуются путем этерификации ретинола жирными кислотами, которые специфицируют эфир. Например, ретинил пальминат образуется, когда ретинол этерифицируется пальмитиновой кислотой. При гидролизе ретиниловых эфиров ретинол восстанавливается. Симметричную молекулу с 40 атомами углерода (в два раза больше, чем у ретинола или ретиноевой кислоты) имеет β-каротин, который содержится в зеленых и желто-оранжевых фруктах и овощах. Как можно предположить исходя из стехиометрии, одна молекула этого каротеноида при расщеплении центральной двойной связи способна произвести две молекулы ретинола.
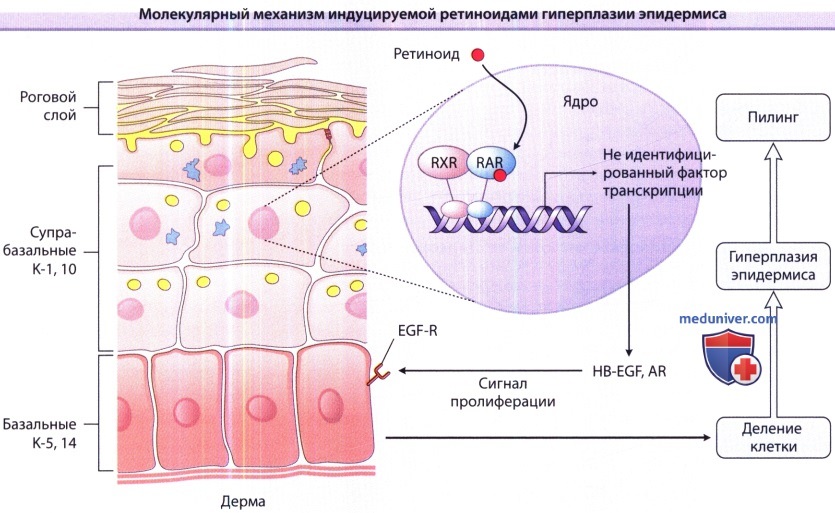
Местное применение ретиноида активирует гетеродимеры RAR/RXR (рецептора ретиноевой кислоты/ретиноидного X рецептора) в супрабазальных кератиноцитах, что приводит к активизации пока не идентифицированных факторов транскрипции. Они, в свою очередь, активируют синтез гепарин-связывающего эпидермального фактора роста (HB-EGF) и амфирегулина (AR).
Посредством активизации EGF-R (рецептора эпидермального фактора роста), HB-EGF и AR вызывают пролиферацию базальных кератиноцитов и последующее шелушение/отторжение чешуек рогового слоя.
2. Этерификация и окисление ретиноидов. Местное лечение кожи человека полностью транс-ре-тинолом повышает уровни ретиниловых эфиров в эпидермальном слое более чем в 10 раз. Эта реакция катализируется двумя ферментами: (1) лецитин/ретинол ацилтрансферазой и (2) ацил коэнзим А/ретинол ацилтрянсферазой. В кератиноцитах человека в процессе этерификации ретинола преобладает активность лецитин/ретинол ацилтрансферазы.
При последующем окислении полностью транс-ретинола образуется полностью шрянс-ретиноевая кислота и полностью транс-ретинальдегид в качестве промежуточного метаболита. Первый этап (окисление полностью тран-ретинола в полностью транс-ретиноевую кислоту) ограничивает скорость образования полностью транс-ретиноевой кислоты. Местное применение полностью транс-ретинола на кожу человека приводит к гистологическим и молекулярным изменениям, которые имитируют изменения после лечения полностью транс-ретиноевой кислотой. К таким изменениям относятся гиперплазия эпидермиса, вызванная пролиферацией кератиноцитов, а также эпидермальный спонгиоз, уплотнение рогового слоя и индукция белков CRBP, CRABР-II и CYP26. В коже, после лечения ретинолом, уровни полностью транс-ретиноевой кислоты минимальные и не отличаются от уровней в нормальной коже, на которую ретинол не применялся. Отсутствие накопления полностью транс-ретиноевой кислоты в коже после лечения ретинолом, является результатом жестко регулируемой конверсии ретинола в ретинальдегид и эффективного гидроксилирования полностью транс-ретиноевой кислоты, которое осуществляется с помощью CYP26.
Тот факт, что полностью транс-ретинол и ретиноевая кислота вызывают сходные реакции в коже человека, но ретинол при этом не приводит к заметному увеличению уровней ретиноевой кислоты, указывает на эндогенно синтезируемую ретиноевую кислоту как на гораздо более эффективный активатор ретиноидного механизма, чем ретиноевая кислота, поступающая экзогенным путем.
3. Гидроксилирование полностью трарнс-ретиноевой кислоты. В коже человека происходит катаболизация полностью транс-ретиноевой кислоты вначале в более полярный 4-гидрокси-метаболит, который затем метаболизируется в 4-оксо-метаболит ретиноевой кислоты. 4-гидрокси-ретиноевая кислота в 10 раз слабее индуцирует ретиноидные реакции в кератиноцитах человека и коже мышей, чем полностью транс-ретиноевая кислота. Без лечения в нормальной коже человека активность CYP26 минимальна. Однако местное применение полностью транс-ретиноевой кислоты или полностью транс-ретинола на кожу человека увеличивает CYP26 в несколько раз. При лечении 9-cis или 13-cis-ретиноевой кислотой, индуцируется также активность гидроксилазы, однако примечательно, что она имеет субстратную специфичность только для изомера полностью транс-ретиноевой кислоты и не гидроксилирует 9-cis или 13-cis-ретиноевую кислоту, ретинол или ретинальдегиды. При применении полностью транс-ретиноевой кислоты максимальная активность CYP26 индуцируется через 24 часа лечения под окклюзией. Активность CYP26 можно эффективно подавить кетоконазолом и родственными азолом — лиарозолом.
Поскольку лиарозол блокирует основной путь инактивации полностью транс-ретиноевой кислоты фармакологическим путем, он может служить миметиком ретиноевой кислоты или усиливать реакции в человеческой коже в ответ на полностью транс-ретинол и ретиноевую кислоту. Выбор СУР26 в качестве мишени воздействия привел к появлению современного класса новых химических структур, получивших название блокаторы метаболитов ретиноевой кислоты (БМРК). Исследование еще одного БМРК, таларозола, показало, что его местное применение приводит к повышению экспрессии мРНК белков CRABP II и CYP26. Хотя БМРК были внедрены в дерматологическую практику несколько лет тому назад, разработка этих препаратов пока идет медленно. Целью разработки будущих БМРК является достижение избирательного воздействия на СУР26 без влияния на другие ферменты, такие как метаболизирующая стероиды ароматаза или 17,20-лиаза.
- Рекомендуем далее ознакомиться со статьей "Показания для местных ретиноидов"
Редактор: Искандер Милевски. Дата публикации: 16.8.2019

