Лучевая терапия болезней кожи: виды, дозы, режимы
Лучевая терапия - краткий обзор:
- Лучевая терапия включает совокупность различных терапевтических вариантов, в том числе брахитерапию, наружную дистанционную лучевую терапию и лучевую терапию заряженными частицами.
- Клинические эффекты лучевой терапии приводят к ранним и поздним изменениям кожи:
- К ранним эффектам относятся воспалительные реакции и десквамация.
- Поздние эффекты включают фиброзные изменения и атрофию придатков кожи.
- Вызванная облучением малигнизация является редким, но серьезным побочным эффектом, проявляющимся, в среднем, через 10 лет после терапии.
- Лучевая терапия показана в случае отдельных доброкачественных пролиферативных заболеваний, если более традиционные терапевтические мероприятия оказались неэффективными.
- Лучевая терапия является одним из вариантов первичной или вспомогательной терапии злокачественных заболеваний кожи.
Первым документально зафиксированным терапевтическим применением облучения был случай лечения кожного злокачественного заболевания у пациента с плоскоклеточной карциномой носа в 1900 году. В течение следующего столетия лучевая терапия широко применялась для терапии злокачественных и доброкачественных заболеваний кожи как у взрослых, так и у детей.
По мере осознания отдаленных последствий лучевой терапии, в частности риска вызванной облучением малигнизации, ее применение при лечении детей, а также доброкачественных заболеваний пошло на спад. Лучевая терапия продолжает играть небольшую, но важную роль в лечении доброкачественных пролиферативных заболеваний кожи, но чаще применяется как вспомогательное мероприятие или альтернатива хирургическому лечению в случае предзлокачественных или злокачественных очагов.
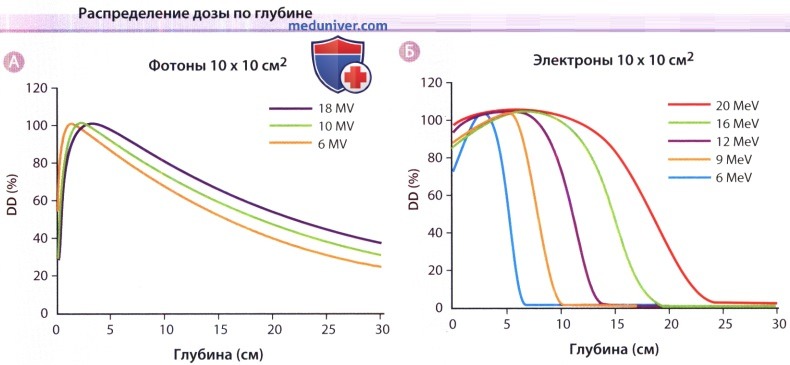
А. Распределение максимальной дозы облучения в процентах (DD) по глубине ткани (в см) в зависимости от энергии фотона (Х-лучей). По мере возрастания энергии фотона, уменьшается процент дозы, попадающей на поверхность и возрастает процент дозы, достигающей более глубоких тканей.
Б. Аналогичная взаимосвязь существует и для терапии электронами. Но в отличие от фотонов, процент дозы, достигающей как поверхностных, так и глубоких тканей, возрастает по мере увеличения энергии электрона. Обратите внимание на разницу в шкале; в отличие от фотонов, энергия электрона практически полностью поглощается на более поверхностных глубинах.
а) Виды лучевой терапии. Возможен выбор из нескольких видов лучевой терапии, при этом некоторые виды являются общедоступными, в то время как другие проводятся только в специализированных центрах. Выбор осуществляется на основании анатомической локализации и размера очага-мишени, биологии опухоли, характера важных окружающих структур и доступности этого варианта терапии.
Для кожных очагов, в частности, важную роль в определении оптимальной терапии играет глубина очага. Высокоэнергетические фотоны, в форме у- или Х-лучей, чаще всего генерируются линейным ускорителем и образуют спектр энергий. Падающее излучение отдает свою энергию, проходя через вещество, и ослабляется в зависимости от расстояния и плотности ткани. Высокоэнергетические лучи доставляют более высокую дозу энергии в глубину ткани и пропорционально меньшую дозу на её поверхность. Низкоэнергетическое излучение отдает энергию в первую очередь мишени на поверхности, не затрагивая ткани, расположенные в глубине.
Энергии, которые чаще всего применяются в терапевтических целях, расположены в мегавольтном диапазоне и доставляются в дозах, подходящих для терапии мишеней в тканях человека. Чтобы доставить более высокие дозы более глубоким тканевым структурам, излучение должно щадить поверхностные структуры, в частности кожу, которая, в противном случае, уменьшала бы величину поступающей вглубь дозы. В отличие от этого, энергии, поглощаемые поверхностными структурами, часто лучше подходят для мишеней в коже. Кривые глубины поглощения и дозы облучения, демонстрирующие зависимость поглощения Х-лучей от их энергии, представлены на рисунке ниже. Большинство применяющихся в клинической практике линейных ускорителей генерируют излучение в диапазоне 6-18 мегавольт (МВт).
Ортовольтные рентгеновские лучи, низкоэнергетические фотоны с максимальной энергией в диапазоне 125-400 киловольт, часто применяются для дерматологических показаний, поскольку их доза достигает максимума на поверхности кожи. По мере проникновения лучей глубже, в мягкие ткани, доза быстро уменьшается. Половина энергетического потока поглощается на глубине первых нескольких сантиметров, что идеально подходит для терапии поверхностных мишеней при минимизации дозы, поступающей в более глубокие здоровые ткани. Ортовольтные лучи генерируются специальными терапевтическими рентгеновскими установками, которые не так распространены, как установки для мегавольтной терапии.
Пограничные лучи — это рентгеновские лучи с еще более низкой энергией в диапазоне 5-15 кВт, которые, доставляют свою дозу облучения на более поверхностную глубину, чем ортовольтные лучи. В прошлом они применялись для терапии поверхностных доброкачественных заболеваний кожи. В этих случаях большинство процессов в мишенях происходит на глубине 1 мм от поверхности кожи. Пограничные лучи больше не рекомендуются в качестве терапии первой линии для рутинного лечения доброкачественных заболеваний кожи.
Лучевая терапия заряженными частицами (как повсеместно доступными электронами, так и протонами, установки для которых имеются лишь в отдельных региональных центрах) обычно применяется для лечения онкологических заболеваний. Электроны генерируются теми же линейными ускорителями, которые используются для производства фотонов с энергией в мегавольтном диапазоне. Для дерматологических показаний обычно применяются электронные лучи, поскольку они способны доставлять высокие дозы энергии на поверхность кожи, при этом в глубине ткани поглощаемая доза быстро уменьшается до ничтожно малых величин. Распределение дозы поглощаемых электронов, так же как и фотонов, зависит от параметра энергии.
Высокоэнергетические электроны доставляют дозу облучения на большую глубину; у фотонов также существует зависимость между глубиной и энергией. Но в отличие от щадящих поверхность кожи свойств высокоэнергетических фотонов, возрастание энергии электронов приводит к увеличению дозы облучения на поверхности кожи. Характеристики распределения поглощаемой дозы электронов по глубине ткани описаны на рисунке ниже.
Протоны — это заряженные частицы, генерируемые большими и дорогими циклотронами или синхротронами, которые имеются лишь в небольшом количестве специализированных центров. Благодаря крупной массе протонов, боковое рассеяние во время пенетрации протонного луча незначительное. Доставка дозы происходит не столько на более поверхностном или более глубоком уровне, а в основном в пределах нескольких миллиметров в конце пробега протонов (пика Брэгга). Модулируя энергию протонного луча, можно более точно доставлять дозу энергии глубоким опухолевым мишеням, так чтобы облучение меньше попадало на окружающую здоровую ткань.
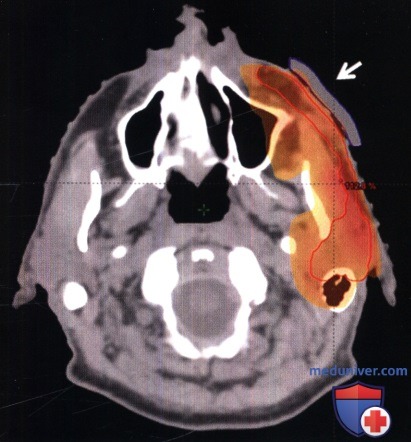
Пациенту в возрасте 61 года была проведена резекция глубокой инвазивной плоскоклеточной карциномы в области скуловой дуги с поражением лимфатических узлов околоушной железы и лицевого нерва.
Для обработки ложа опухоли, наряду с оставшейся околоушной железой и ходом лицевого нерва, применялись мегавольтные протоны.
Эквивалентный плотности ткани болюс (белая стрелка) помещали над опухолевым ложем, чтобы увеличить кожную дозу в этой области до 100%.
б) Модуляция наружного излучения. Планирование лучевой терапии предполагает принятие целого ряда сложных решений относительно подходящей модальности облучения, энергии излучения, ориентации лучей, положения пациента и применения терапевтических приспособлений. Последние помогают повысить дозу излучения в целевых структурах и блокировать или уменьшить воздействие облучения на здоровые ткани. Термином «болюс» обозначают материал, эквивалентный ткани по плотности, который обычно применяют при лучевой терапии поверхностных злокачественных опухолей кожи. Его можно изготовить различной толщины и применять на кожу пациента во время ежедневного лечения.
Болюс потенциально служит следующим целям: в случае высокоэнергетических X-лучей (напр., мегавольтной энергии) или низкоэнергетических электронов доза на поверхности будет низкой по сравнению с дозой в расположенных глубже тканях. Поместив на кожу болюс соответствующей толщины, можно увеличить попадающую на поверхность кожи дозу до терапевтического уровня. Это показано на рисунке ниже. Еще одна функция болюса — ослабить падающий луч, чтобы понизить дозу, попадающую в глубокие структуры, например, во время терапии рака кожи на виске уменьшить дозу, проникающую в головной мозг. Материал болюса может применяться также для компенсации сложной топографии и равномерного распределения дозы при терапии кожи вокруг носа и ушей, как показано на рисунке ниже.
Лучам можно придавать форму различными приспособлениями в зависимости от их энергии. Лучи мегавольтной терапии можно формировать изготовленными на заказ блоками из свинцового сплава толщиной 7 см, которые соответствуют нужной форме; большинство современных линейных ускорителей имеют многолистовой коллиматор (МЛК), который содержит смещающиеся вольфрамовые листки, соответствующие нужной для терапии апертуре. Излучение электронного луча обычно блокируют изготовленными по заказу блоками из свинца или свинцового сплава. Ортовольтное излучение блокируется с применением более тонкого свинцового щитка, который обычно помещают на кожу пациента. Примеры блокирующих приспособлений показаны на рисунке ниже.
Традиционно, лучи наружного дистанционного облучения формируются с применением блоков или статических многолистовых коллиматоров для соответствия мишени, контуры которой определяются клинически или с помощью КТ, либо другого метода визуализации. Пучки лучей, угол падения луча и величину энергий выбирают так, чтобы избегать отдельных здоровых структур, и доза рассчитывается с многократными изменениями, пока не будет создан приемлемый план. В настоящее время, если опухолевая мишень расположена вблизи ограничивающей дозу структуры, все чаще применяется метод «инверсного планирования». Лучевая терапия с модуляцией интенсивности дозы (IMRT) предполагает применение индивидуальных не статичных лучей; апертура изменяется в ходе терапии для точной настройки энергетической установки.
в) Дозы лучевой терапии и режим дозирования. В международной системе единиц (СИ) единицей облучения является грей (Гр), который определяется как один джоуль энергии излучения, поглощаемый одним килограммом массы ткани. Альтернативной единицей поглощенной дозы, которую грей почти совершенно заменил, является рад (акроним английского термина radiation absorbed dose); один грей равен 100 радам. Доза зависит от объема мишени, который определяется лечащим врачом-онкологом. Для большинства злокачественных опухолей эпителия общая доза находится в диапазоне 50-80 Гр, лимфоидные неоплазии типично отвечают на дозы 15-40 Гр. Отдельные доброкачественные заболевания можно лечить более низкими дозами; в случае гипертрофических рубцов и келоидов обычно назначают дозы в диапазоне 4-20 Гр.
Термин фракционирование обозначает доставку определенной дозы облучения в течение нескольких разделенных во времени сеансов, что рекомендуется как для усиления эффективности воздействия на тканевые мишени, так и для восстановления поврежденных лучевым воздействием здоровых тканей. Следовательно, режим фракционирования может применяться как для усиления воздействия дозы на мишень, таки для минимизации лучевого повреждения здоровых тканей. Обычные схемы фракционирования с применением традиционной лучевой терапии предусматривают проведение сеансов с интервалами от двух до одного раза в неделю.
Эффективность лучевой терапии в большой мере зависит от режима терапии: от общего количества дней, в течение которых распределены сеансы, и от величины фракционной дозы. Обычная ежедневная доза при сеансах пять дней в неделю составляет 1,8-2 Гр в день. Сравнить различные режимы фракционирования можно с помощью математического преобразования в биологически эффективную дозу (БЭД), используя формулу, включающую такие параметры, как количество фракций, величину фракции и характеристики восстановления ДНК в ткани-мишени.
- Рекомендуем далее ознакомиться со статьей "Лучевой дерматит: механизмы, клиника"
Редактор: Искандер Милевски. Дата публикации: 2.10.2019

