Взаимосвязь между клиническими и лабораторными данными при пигментной ксеродерме
Пациенты с пигментной ксеродермой имеют гиперчувствительность к УФ излучению, точно так же как их культивированные клетки. Кожные и глазные нарушения поразительно ограничены подверженными УФ-воздействию областями, а защищенные от УФ участки (такие как подмышечные впадины, ягодицы и сетчатка) обычно не страдают. То, что чернокожие пациенты с ПК имеют повышенную частоту развития рака кожи, указывает на нормально функционирующую систему репарации ДНК, обеспечивающую более высокую защиту против рака кожи, чем натуральная пигментация черной кожи.
а) Группы комплементации. С клиническими проявлениями, расцениваемыми как пигментная ксеродерма, связаны по меньшей мере восемь молекулярных дефектов, что показано выделением семи групп комплементации недостаточной эксцизионной репарации ДНК (от А до G). Обсуждение клонированных ПК генов и их функции можно найти в отдельных статьях на сайте. Список заболеваний, вызванных мутациями в ПК и СК гена, опубликован на сайте xpmutations.org Клинические проявления заболевания и гены репарации ДНК сложно соотносятся между собой. Множественные NER-гены связаны по меньшей мере с целым спектром разных клинических фенотипов. Клинический фенотип может быть связан с дефектами в каждом из нескольких генов.
И наоборот, мутации в одном гене могут быть связаны с несколькими различными клиническими фенотипами. Эти комплексные взаимосвязи и роли генов репарации ДНК в регуляции транскрипции и иммунных функциях активно изучаются.
б) Группа комплементации А. Группа комплементации А состоит из пациентов с наиболее тяжелыми неврологическими и соматическими нарушениями (синдром де Санктис-Каккионе), а также пациентов с минимальной неврологической симптоматикой или без нее. Длительное наблюдение за этими пациентами выявило взаимосвязь между генотипом и фенотипом. Пациенты с наиболее тяжелым течением болезни, по-видимому, имеют усеченные мутации в обоих аллелях гена ХРА, что ведет к отсутствию определяемых нормальных протеинов.
Напротив, у пациентов с минимальными неврологическими нарушениями отмечаются сплайс-мутации, которые позволяют получать небольшое количество нормальной матричной РНК (мРНК). Эта форма наблюдается в США, Европе и странах Среднего Востока и является наиболее распространенной формой ПК в Японии. Примерно 90% японцев с ПК-A имеют одну и ту же мутацию замены основания. Этот признак послужил основой для развития быстрого диагностического подхода для японских пациентов с ПК типа А (в том числе и при пренатальной диагностике) с использованием полимеразной цепной реакции небольшого образца ДНК. Было установлено, что гетерозиготные носители такой приводящей к болезни мутации, имеющие один мутированный и один нормальный аллель, составляют почти 1% японской популяции.
в) Группа комплементации В. Группа комплементации В включает пять пациентов четырех родовых кланов, у которых были выявлены изменения кожи, характерные для ПК (включая новообразования), в сочетании с неврологическими и глазными симптомами, типичными для синдрома Коккейна. В другой семье было две взрослых сестры с ПК без СК, у которых были выявлены меланомы глаз, впоследствии родивших здоровых детей. Примечательно, что у пациента с ТТД также был выявлен дефект гена ХРВ.

г) Группа комплементации С. Пациенты из группы комплементации за редким исключением страдают ПК с поражением кожи и глаз, но без неврологических нарушений. Эта группа является распространенной в США, Европе и Египте, но редко наблюдается в Японии. Большинство пациентов имеют усеченные мутации в обоих аллелях, что приводит к неопределяемым уровням мРНК ХРС (вследствие нонсенс-опосредованного распада матрицы). Так или иначе, сплайс-мутации в области «лассо» и точек ветвления, приводящие к образованию лишь 3-5% нормальной мРНК, вызвали более легкую клиническую картину у одной семьи из Турции.
Пациенты с ПК типа С обычно не имеют в анамнезе тяжелых ожогов в ответ на минимальное солнечное воздействие, и иногда диагноз впервые выставляется при наличии рака кожи в детском возрасте. Сообщалось, что у одного пациента с ПК-С отмечалась гиперчувствительность к ионизирующему излучению; однако коррекция гена ХРС не привела к исправлению клеточной гиперчувствительности в ответ на ионизирующее излучение, что позволяет предположить, что в данном случае имелся дефект более чем одного гена.
д) Группа комплементации D. У пациентов из группы комплементации D описано шесть различных клинических фенотипов. У них может развиваться кожная ПК с поздним началом неврологических нарушений на втором десятилетии жизни или ПК без неврологических нарушений. Сообщалось о двух пациентах с ПК-D, с клиническими признаками как ПК, так и СК. Клетки пациентов с фотосенситивной формой ТТД (без ПК) также были отнесены к группе комплементации ПК D. Сообщалось о двух пациентах с комбинированными симптомами ТТД и ПК (у одного пациента был рак кожи) и мутациями в гене XPD. Наконец, у пациента с церебро-окулярно-фасциально-скелетным (ЦОФС) синдромом была выявлена мутация в гене XPD.
е) Группа комплементации Е. В родовом клане в Европе и в нескольких семейных родах Японии была выявлена группа комплементации Е. Мы исследовали взрослых пациентов со множественным раком кожи в трех группах родства в Соединенных Штатах и Германии и не обнаружили неврологических проявлений.
ж) Группа комплементации F. Пациенты группы комплементации F были идентифицированы преимущественно в Японии. Большинство этих пациентов имеют легкие клинические симптомы без неврологических нарушений или рака кожи. Однако недавно мы выявили две семьи с началом во взрослом возрасте тяжелого нейродегенеративного процесса при мутациях в гене ХРЕ. Остаточная степень репарации ДНК так или иначе очень низка (лишь 10-20% от нормы).
з) Группа комплементации G. Тринадцать пациентов из группы комплементации G были выявлены в США, Европе и Японии. Среди этих пациентов отмечается большое разнообразие клинических признаков. У нескольких пациентов с мутациями в гене XPG были клинические проявления как ПК, так и тяжелого СК с кахексией и летальным исходом на первом десятилетии жизни. Другие пациенты с различными мутациями в этом же гене не имели неврологических нарушений.
и) Вариантная пигментная ксеродерма. Клетки при вариантной ПК имеют нормальную эксцизионную репарацию ДНК (NER) и, таким образом, не попадают ни в одну из групп комплементации клеток с дефектной эксцизионной репарацией ДНК. При этом заболевании, однако, отмечается нарушение в склонной к ошибкам ДНК-полимеразе (Pol η), которая обходит участки повреждения ДНК без репарации. Большая часть пациентов с вариантной пигментной ксеродермой имеет клинические проявления пигментной ксеродермы без неврологических нарушений. Кожные и глазные симптомы у одних пациентов были тяжелыми, у других имели легкое течение.
Гетерозиготы. Гетерозиготные носители ПК (родители и некоторые другие родственники) являются носителями гена ПК, но не имеют клинических проявлений. Для определения, имеют ли данные лица повышенный риск развития рака кожи, нет достаточного объема эпидемиологических данных. При анализе клеток гетерозиготных носителей пигментной ксеродермы большинство исследований клеточной функции или репарации ДНК дают нормальные результаты.
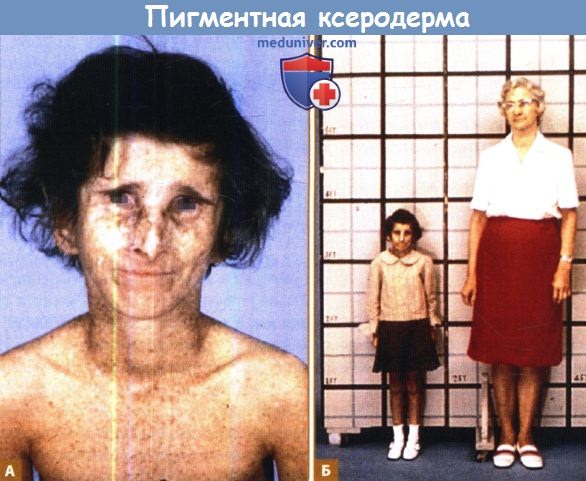
А. 28-летняя пациентка (ХР11BE) группы комплементации пигментной ксеродермы В с пигментными изменениями и атрофией кожи.
У пациентки клювовидный нос и недостаточность подкожно-жировой клетчатки, что типично для синдрома Коккейна.
Б. У пациентки низкий рост (менее 120 см). Ее мать — облигатный носитель гетерозиготы без клинических проявлений.
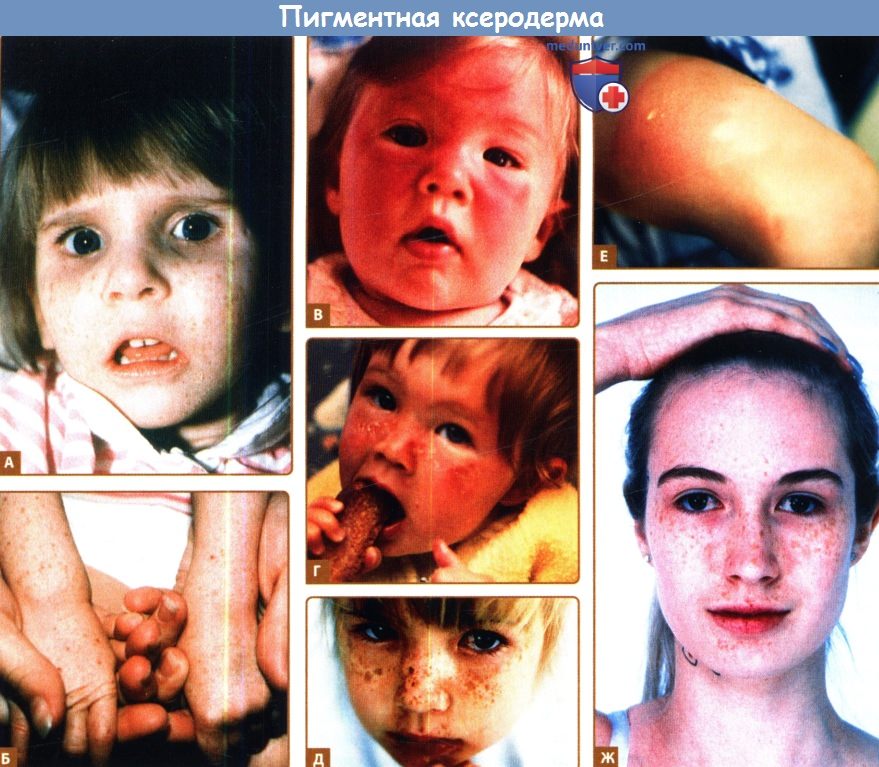
А, Б. XP82DC. В-Ж. ХР65ВЕ. А. Пациентка с XP82DC в возрасте трех лет с глубоко-посаженными глазами, что характерно для синдрома Коккейна (СК) и неравномерной лентигинозной пигментацией на лице, характерной для ПК; виден комплекс ПК-СК.
Б. Пациентка с XP82DC в возрасте 3-х лет с характерными для ПК пигментными изменениями на предплечьях и дорсальных поверхностях ладоней наряду стойкой, прозрачной кожей и хорошо видимыми венами. Маленький размер ее рук очевиден в сравнении с руками ее матери.
В. Пациентка с ХР65ВЕ в возрасте шести месяцев, перенесшая тяжелый солнечный ожог на лице при минимальном воздействии солнечного света. На коже лба, щек и окологлазничной области видны эритема и отек.
Г. Пациент с ХР65ВЕ в возрасте девяти месяцев с эритемой и отслоением кожи скуловой области на лице после воздействия солнца.
Д. Пациентка с ХР65ВЕ в возрасте 4,5 лет с пигментными изменениями на носу, скуловой области и других участках кожи лица.
Е. Пациент с ХР65ВЕ в возрасте 4,5 лет с образованием волдырей после солнечного ожога на коже верхней части бедра. Обратите внимание на незатронутый участок кожи над коленом, где был применен солнцезащитный крем.
Ж. Пациентка с ХР65ВЕ с минимальными пигментными изменениями на лице и незатронутыми шеей и ладонями. Она использует специальные средства для защиты кожи от солнечного воздействия.
- Рекомендуем далее ознакомиться со статьей "Синдром Коккейна - этиология, клиника, диагностика"
Редактор: Искандер Милевски. Дата публикации: 17.12.2018

