Болезни от нестабильности генома и нарушения репарации ДНК - классификация, причины
Наследственные заболевания связанные с нестабильностью генома и репарации ДНК - краткий обзор:
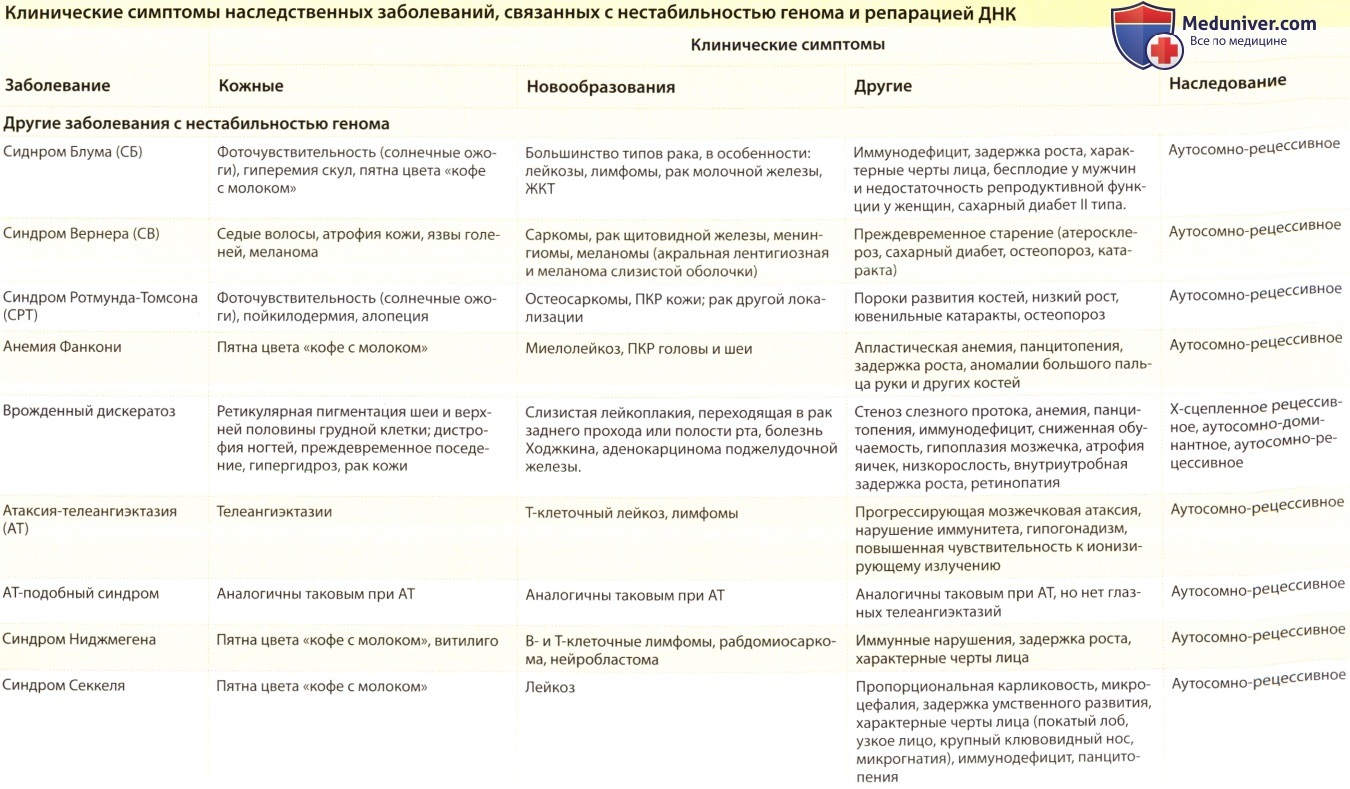
- Термин «нестабильность генома» характеризует большую группу наследственных заболеваний с выраженными кожными изменениями; во многих случаях отмечается повышенный риск развития рака.
- Причиной нестабильности генома является нарушение процессов репарации и/или поддержания нормальной структуры ДНК.
- Пигментная ксеродерма представляет собой поражение с нарушением репарации ДНК, поврежденной внешними факторами, и значительно повышенной частотой возникновения рака, спровоцированного солнечным излучением.
- Хотя эти заболевания встречаются редко, гетерозиготные носители поврежденных генов, которые составляют вплоть до нескольких процентов от общей популяции, также могут иметь повышенный риск развития рака.

Так как основой контроля над функциями клеток является геном, для непрерывного функционирования клеток, тканей и организмов в целом необходимо поддержание его стабильности. ДНК является носителем генетической информации. Целостности ее структуры регулярно угрожают повреждающие агенты, к которым относятся окислительное воздействие, ультрафиолетовое (УФ) и рентгеновское излучение, а также химические вещества. Хотя большая часть повреждений восстанавливается, невозможность поддерживать целостность генома может приводить к нарушению клеточной функции или гибели клеток.
При делении клетки продукты ее деления могут накапливать дополнительное повреждение, и такое прогрессирующее накопление повреждения может приводить к малигнизации.
В статьях на сайте описываются основные заболевания кожи, связанные с нестабильностью генома и лежащими в основе дефектными механизмами репарации или поддержания структуры ДНК. При всех этих заболеваниях отмечаются выраженные кожные изменения, поэтому в постановке диагноза и лечении требуется участие дерматологов. Большинство, хотя и не все эти состояния характеризуются также повышенным риском развития злокачественных новообразований. Этот факт свидетельствует о том, что поддержание целостности генома имеет крайнюю важность для предотвращения злокачественного перерождения. Злокачественная трансформация требует накопления нескольких мутаций в специфических генах одной клетки, фенотип мутаторного гена часто расценивается как предпосылка канцерогенеза, ввиду того, что при отсутствии нестабильности генома возникновение всех этих мутаций в одной клетке было бы крайне маловероятно. Те же самые гены, которые поражаются при наследственных нарушениях, связанных с нестабильностью генома, могут также приводить к нестабильности генома в отдельных клетках при повреждении приобретенными мутациями, играя, таким образом, важную роль в раннем спонтанном канцерогенезе.
Кроме того, несмотря на то что эти наследственные болезни встречаются редко (порядка 10-5 или 10-6), носители пораженных генов могут составлять несколько процентов от общей популяции. У таких людей, как правило, не бывает клинических симптомов, так как большинство этих нарушений характеризуется аутосомно-рецессивным типом наследования. Так или иначе, эпидемиологические исследования позволяют предположить, что гетерозиготные носители также могут иметь повышенный риск развития новообразований.
Спонтанная нестабильность синдрома наблюдается при синдроме Блума (СБ), атаксии-телеангиэктазии, анемии Фанкони (АФ) и проявляется повышенной поломкой хромосом в первичных клетках крови и кожи. С другой стороны, нестабильность генома обнаруживается в клетках пациентов с пигментной ксеродермой (ПК) лишь только после воздействия повреждающими ДНК агентами, такими как УФ-излучение или другие канцерогены (например, бензапирен, который находится в сигаретном дыме). При ПК многие из тяжелых проявлений заболевания, такие как рак и рубцевание роговицы, приводящее к потере зрения, являются результатом взаимодействия между генетическими факторами риска и факторами внешней среды. Например, у пациентов с ПК, которые избегают УФ-об-лучения, резко снижается или полностью исчезает вероятность развития рака кожи и слепоты.
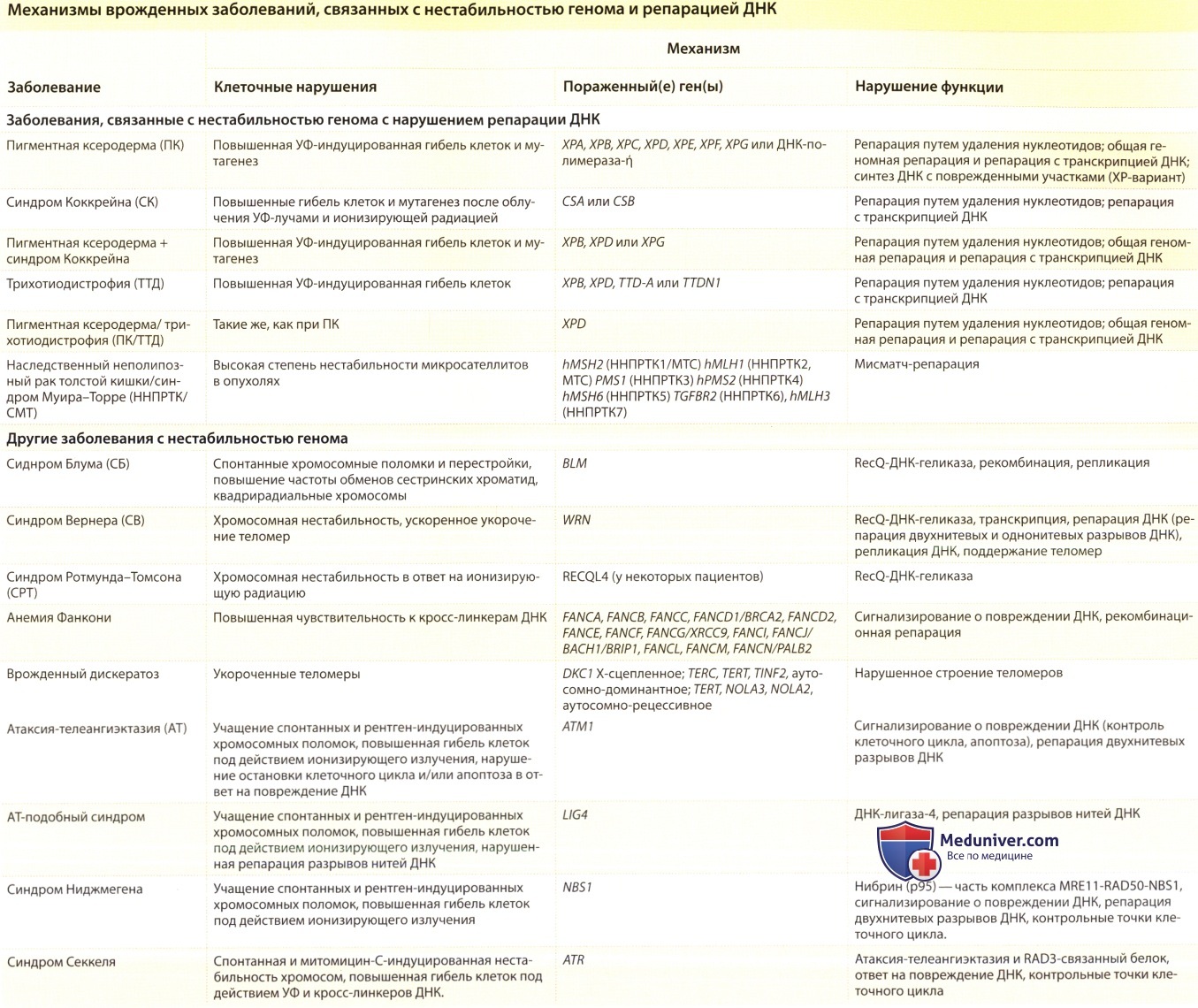
При некоторых описанных здесь заболеваниях нестабильность генома вызывается нарушенной способностью восстанавливать ДНК, поврежденную определенными физическими или химическими агентами. Клетки обладают различными механизмами репарации ДНК, при помощи которых восстанавливаются различные типы повреждения. Эксцизионная репарация путем удаления нуклеотидов (NER), восстанавливающая целостность ДНК после крупных повреждений, включая УФ-индуцированные фотопродукты, при ПК, синдроме Коккейна (СК) и трихотиодистрофии (ТТД) нарушена. Клетки пациентов, страдающих данными заболеваниями, характеризуются повышенной гибелью и образованием мутаций в ответ на воздействие УФ-излучения. Однако повышенный риск развития рака отмечается только у пациентов с ПК. Причина таких различий в риске развития рака неизвестна.
Белки, кодируемые некоторыми из пораженных генов при этих трех заболеваниях, не только вовлечены в процесс репарации ДНК, но также в процесс транскрипции и клеточных ответов на повреждение ДНК. Таким образом, мутации, повреждающие различные функции одного и того же гена, по-видимому, играют роль в развитии разнообразных фенотипов, которые напрямую не связаны с функциями репарации ДНК и лежат в основе нескольких синдромов, перекрещивающихся между тремя этими состояниями. Было выявлено множество клинических фенотипов заболеваний, связанных с репарацией ДНК и ассоциированные с ними дефекты генов. При этом с одним и тем же клиническим фенотипом могут быть ассоциированы мутации в разных генах репарации ДНК.
С другой стороны, разные мутации в одном и том же гене репарации ДНК могут приводить к разным клиническим фенотипам. Например, мутации в гене XPD(ERCC2) ассоциированы со следующими клиническими фенотипами: ПК, ПК с неврологическими нарушениями, сложный ПК — синдром Коккейна (ПК/СК), ПК/ТТД, ЦОСК (церебро-окуло-скелетный синдром) или СК/ ТТД. Вариантная ПК, которая клинически неотличима от ПК, представляет собой нарушение толерантности к повреждению ДНК. Хотя нормальные клетки могут претерпевать повреждения ДНК во время репликации (синтез ДНК с поврежденной матрицы), у пациентов с вариантной ПК этот процесс нарушен. Мисматч репарация ДНК повреждается при наследственном неполипозном раке толстой кишки (синдром Линча) и его подтипе — синдроме Муира-Торре, при котором отмечаются кожные признаки, включая опухоли сальных желез. Данные изменения рассматриваются в главе 153.
Хеликазы — это белки, которые раскручивают цепи ДНК и необходимы для множества метаболических процессов с вовлечением ДНК, таких как транскрипция, репликация, репарация и многие другие. Два гена, вовлеченные в NER, представляют собой хеликазы, которые также являются частью основного фактора транскрипции— TFIIH. Продукт гена ХРВ (ERCC3) раскручивает ДНК в направлении от 3’ до 5’ конца, в то время как продукт гена XPD (ERCC2) делает это в обратном направлении. Семейство ДНК-хеликаз RecQ оказалось чрезвычайно сохранным в процессе эволюции. Из пяти известных представителей семейства RecQ человека, три (BLM, WRN и RECQL4, вызывающие синдром Блума, синдром Вернера (СВ) и синдром Ротмунда-Томсона (СРТ), соответственно) мутируют при определенных клинических нарушениях, связанных с хромосомной нестабильностью, предрасположенностью к раку и/или преждевременным старением.
Генетическая нестабильность также может быть следствием нарушения функционирования теломеров. Теломеры представляют собой длинные повторяющиеся последовательности нуклеотидов (TTAGGG)n, играющие важную роль в поддержании хромосомной интегративности. С каждым клеточным делением теломерная последовательность укорачивается на определенное количество нуклеотидов. С этим явлением связан феномен «старения» клетки. Для пациентов с врожденным дискератозом, имеющим тенденцию к малигни-зации, специфично ускорение укорочения теломерной последовательности. Примерно у половины из этих пациентов были обнаружены мутации в одном из 6 генов, вовлеченных в регуляцию теломеров.
BASC (BRCA1-ассоциированный комплекс наблюдения за геномом [BRCA1-assiciated genome surveillance complex]) представляет собой мультиферментный комплекс, сконцентрированный вокруг белка BRCA1 в ядре. Он содержит важные белки ответа на повреждение ДНК, включая ATM, ATR, комплекс MRE11-RAD50-NBS1, BRCA1, BLM, FANCD2 и MLH1. Эти белки физически взаимодействуют друг с другом. Нестабильность генома может быть результатом дефекта в любом из этих белков и вызывает заболевания, связанные с нестабильностью генома — такие как атаксия-телеангиэктазия? синдром Секкеля, синдром Ниджмегена, наследственный рак молочной железы, СБ, АФ или наследственный рак толстой кишки. СБ и АФ рассматриваются в отдельных статьях на сайте.

- Рекомендуем далее ознакомиться со статьей "Пигментная ксеродерма (ПК) - встречаемость, этиология, клиника, диагностика"
Редактор: Искандер Милевски. Дата публикации: 17.12.2018

