Механизмы развития (патогенез) тромботической микроангиопатии
Термин «тромботическая микроангиопатия» охватывает спектр клинических синдромов, включая тромботическую тромбоцитопеническую пурпуру (ТТП) и гемолитико-уремический синдром (ГУС). Соответственно первоначальному описанию ТТП определяется как пентада симптомов: лихорадка, тромбоцитопения, микроангиопатическая гемолитическая анемия, преходящий неврологический дефицит и почечная недостаточность.
ГУС часто наблюдается у детей и тоже ассоциируется с микроангиопатической гемолитической анемией, однако отличается более выраженной почечной недостаточностью и отсутствием неврологических симптомов. По мере накопления опыта и выяснения механизмов различия между ТТП и ГУС стали не столь явными. У многих взрослых пациентов с ТТП отсутствует один или несколько из перечисленных симптомов, а у некоторых пациентов с ГУС есть лихорадка и неврологическая дисфункция.
В настоящее время считают, что и ГУС, и ТТП приводят к избыточной активации тромбоцитов, которые агрегируются в микрососудистом ложе. Эти внутрисосудистые тромбы вызывают микроангиопатическую гемолитическую анемию и распространенную дисфункцию органов, а потребление тромбоцитов приводит к тромбоцитопении. Считается, что различные клинические проявления ГУС и ТТП обусловлены неодинаковой предрасположенностью организма человека к образованию тромбов в тканях.
Некоторые признаки тромботических микроангиопатий одинаковы, но пусковой механизм патогенной активации тромбоцитов различен, что позволяет провести дифференциальную диагностику. ТТП обычно ассоциируется с дефицитом фермента плазмы ADAMTS13 (металлопротеиназой WF). В нормальных условиях ADAMTS13 расщепляет чрезвычайно высокомолекулярные мультимеры WF. Без него эти мультимеры накапливаются в плазме и способствуют активации и агрегации тромбоцитов.
Дополнительное повреждение эндотелия другими факторами может усиливать процесс образования микроагрегатов тромбоцитов, что инициирует или еще больше усиливает клинически выраженную ТТП.
Дефицит ADAMTS13 может быть наследственным или приобретенным. В случае приобретенной формы присутствуют аутоантитела, ингибирующие металлопротеазную активность ADAMTS13. Реже пациенты наследуют инактивирующую мутацию гена ADAMTS13. У лиц с наследственным дефицитом ADAMTS13 заболевание часто начинается в пубертатном периоде, симптомы появляются эпизодически.
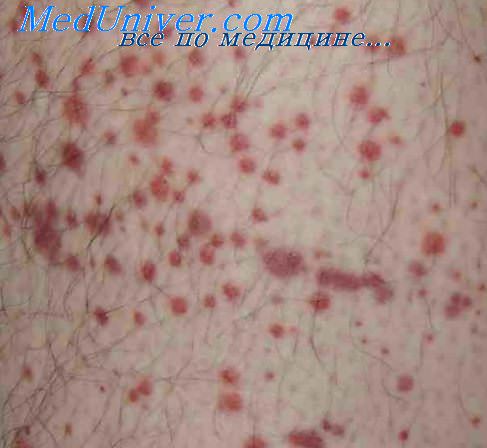
Для развития тромботической тромбоцитопенической пурпуры (ТТП) помимо дефицита ADAMTS13 необходимо участие других пусковых механизмов, например, дополнительных сосудистых повреждений или протромботического состояния.
Диагностика тромботической тромбоцитопенической пурпуры (ТТП) при обследовании любого пациента с тромбоцитопенией и микроангиопатической гемолитической анемией имеет большое значение, т.к. промедление может стать фатальным для пациента. С помощью замены плазмы, позволяющей удалить аутоантитела и возместить функциональный ADAMTS13, удается получить лечебный эффект более чем у 80% пациентов с ТТП, ранее неизбежно приводившей к летальному исходу.
В отличие от тромботической тромбоцитопенической пурпуры (ТТП) гемолитико-уремический синдром (ГУС) ассоциируется с нормальным уровнем ADAMTS13 и возникает в результате других дефектов.
Эпидемический (типичный) гемолитико-уремический синдром (ГУС) ассоциируется с инфекционным гастроэнтеритом, вызываемым штаммом 0157:Н7 Е. coli, вырабатывающим шигаподобный токсин. Этот токсин абсорбируется из воспаленной слизистой оболочки желудочно-кишечного тракта в кровоток, где изменяет функцию эндотелиальных клеток, в результате происходят активация и агрегация тромбоцитов. Наибольший риск имеют дети и пожилые люди. У заболевших появляется кровянистая диарея, а через несколько дней — ГУС.
При поддерживающей терапии возможно полное выздоровление, однако в тяжелых случаях вероятны необратимое поражение почек и смерть.
Неэпидемический (атипичный) гемолитико-уремический синдром (ГУС) часто ассоциируется с дефектами фактора Н системы комплемента, белкового мембранного кофактора CD46, или фактора I. В обычных условиях эти три белка предотвращают избыточную активацию альтернативного пути активации системы комплемента. Дефицит этих белков может быть вызван наследственными дефектами или обусловлен появлением ингибирующих аутоантител и ассоциируется с ремиттирующим, рецидивирующим течением заболевания.
Механизм активации тромбоцитов при гемолитико-уремическом синдроме (ГУС) остается неясным. Предположительно шигаподобный токсин, продуцируемый патогенной Е. coli, и дефекты белков-регуляторов системы комплемента каким-то образом изменяют функцию эндотелиальных клеток, что приводит к активации тромбоцитов.
Тромботические микроангиопатии, напоминающие гемолитико-уремический синдром (ГУС), могут возникать после воздействия других агентов, повреждающих эндотелиальные клетки (например, некоторых лекарственных средств и радиотерапии). В этих условиях прогноз должен быть осторожным, поскольку ГУС часто осложняется хроническими, угрожающими жизни заболеваниями.
ДВС и тромботические микроангиопатии имеют общие характеристики (в частности, наличие микрососудистой окклюзии и микроангиопатической гемолитической анемии), однако патогенетически они различаются. В отличие от ДВС при ТТП и ГУС активация каскада коагуляции не имеет первостепенного значения, в связи с чем лабораторная оценка гемостаза и коагуляции (протромбинового времени и частичного тромбопластинового времени) обычно дает результаты, не отклоняющиеся от нормы.

- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) кровотечений при нарушении функции тромбоцитов"
Оглавление темы "Патогенез болезней":- Механизмы развития (патогенез) тромботической микроангиопатии
- Механизмы развития (патогенез) кровотечений при нарушении функции тромбоцитов
- Механизмы развития (патогенез) кровотечений при дефиците факторов коагуляции
- Механизмы развития (патогенез) болезни Виллебранда
- Механизмы развития (патогенез) гемофилии А
- Механизмы развития (патогенез) гемофилии В
- Механизмы развития (патогенез) ДВС
- Строение и функция легких
- Виды врожденных аномалий легких
- Механизмы развития (патогенез) ателектаза легкого

