Механизмы развития (патогенез) ДВС
ДВС — это острое, подострое или хроническое тромбогеморрагическое заболевание, характеризующееся избыточной коагуляцией крови, приводящей к образованию тромбов в микрососудах. ДВС — вторичное осложнение многих расстройств. Иногда коагулопатия проявляется изолированно в специфическом органе или ткани. Вследствие тромбоза расходуется большое количество тромбоцитов, фибрина и факторов коагуляции и, как вторичное явление, происходит активация фибринолиза. Признаки и симптомы ДВС могут быть обусловлены гипоксией тканей и инфарктами, вызванными множеством микротромбов. Геморрагии возникают в результате истощения факторов, необходимых для гемостаза, или активации фибринолитических механизмов, или обоих процессов.
а) Этиология и патогенез. Необходимо подчеркнуть, что ДВС не является первичным заболеванием. Это коагулопатия, возникающая в ходе разнообразных клинических нарушений. Обсуждая общие механизмы, лежащие в основе ДВС, целесообразно кратко рассмотреть нормальные процессы коагуляции крови и удаления сгустка.
Процесс коагуляции может идти по одному из двух путей:
(1) по внешнему пути, запускаемому высвобождением тканевого фактора (тканевого тромбопластина);
(2) по внутреннему пути, связанному с активацией фактора XII при поверхностном контакте с коллагеном или другими веществами.
Оба пути через серию промежуточных этапов приводят к образованию тромбина, который, в свою очередь, превращает фибриноген в фибрин. Далее в месте повреждения тромбин усиливает местное отложение фибрина, непосредственно воздействуя на внутренний путь и факторы, ингибирующие фибринолиз.
После инициации процесса очень важно, чтобы коагуляция была ограничена местом повреждения (ранения). Примечательно, что тромбин, попадая в кровоток и нормальные сосуды, превращается в антикоагулянт благодаря связыванию с тромбомодулином — белком, присутствующим на поверхности эндотелиальных клеток. Комплекс тромбин-тромбомодулин активирует белок С, важный ингибитор двух прокоагулянтов — фактора V и фактора VIII. Другие активированные факторы коагуляции удаляются печенью. Напомним, что кровь также содержит несколько сильных фибринолитических факторов, например плазмин. Перечисленные и дополнительные механизмы контроля в норме сбалансированы таким образом, что обеспечивают необходимую коагуляцию в нужном месте и в нужное время.
Итак, ДВС возникает в результате патологической активации внешнего и/или внутреннего путей коагуляции либо нарушения механизмов ингибирования коагуляции. Поскольку последнее редко является первичным механизмом ДВС, сконцентрируем внимание на аномальной инициации коагуляции.
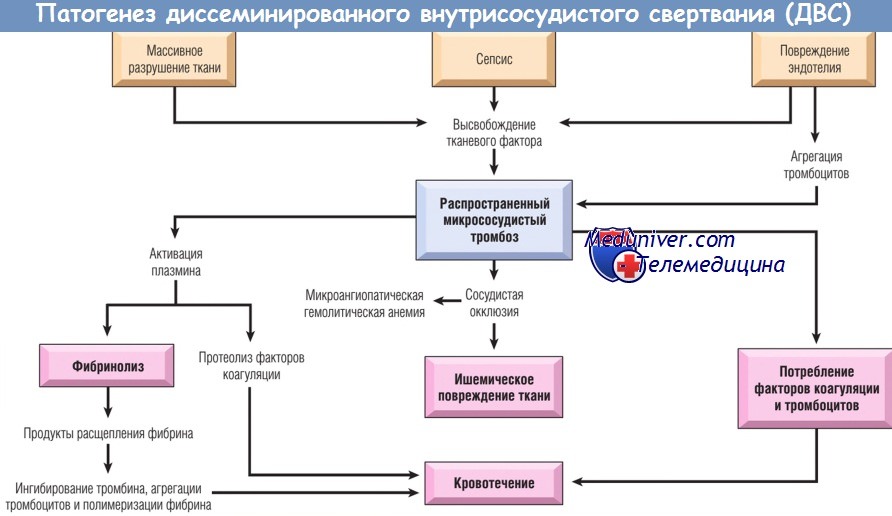
ДВС инициируют два основных механизма:
(1) высвобождение в кровоток тканевого фактора или тромбопластических веществ;
(2) распространенное повреждение эндотелиальных клеток.
Источники тромбопластических веществ весьма разнообразны. Это может быть плацента при осложнениях беременности или лейкозные клетки при острой промиелоцитарной лейкемии. Слизь, выделяемая некоторыми аденокарциномами, способна непосредственно активировать фактор X независимо от фактора VII.
Повреждение эндотелиальных клеток инициирует ДВС разными способами. В результате повреждений, приводящих к некрозу эндотелия, обнажается субэндотелиальный матрикс, что активирует тромбоциты и оба пути коагуляции. Одним из медиаторов подобных эффектов служит TNF, проявляющий свою функцию в случае ДВС при сепсисе. TNF индуцирует экспрессию тканевого фактора на поверхности эндотелиальных клеток и снижает экспрессию тромбомодулина, сдвигая баланс гемостаза в сторону коагуляции. Кроме того, TNF повышает экспрессию молекул адгезии эндотелиальными клетками, тем самым способствуя адгезии лейкоцитов, которые могут повреждать эндотелиальные клетки за счет высвобождения реактивных метаболитов кислорода и преформированных протеаз. Распространенное повреждение эндотелиальных клеток также может быть вызвано отложением комплексов антиген-антитело (например, при СКВ), воздействием экстремальных температур (в частности, тепловым ударом, ожогами), а также микроорганизмами (менингококками, риккетсиями). Инициировать про-коагулянтную активность могут даже небольшие повреждения эндотелиальных клеток, усиливая экспрессию тканевого фактора на клеточной мембране.
Вероятность ДВС наиболее высока при осложнениях беременности, злокачественных опухолях, сепсисе и обширных травмах. Пусковые механизмы в этих условиях часто множественные и взаимосвязанные. Так, при бактериальных инфекциях эндотоксины могут поражать эндотелиальные клетки и ингибировать экспрессию тромбомодулина прямо или посредством продукции TNF. Из воспалительных клеток высвобождаются тромбопластины, и активируется фактор XII. Комплексы антиген-антитело, формирующиеся в ответ на инфекцию, способны стимулировать классический путь активации системы комплемента с образованием фрагментов, активирующих тромбоциты и гранулоциты вторично. При обширных травмах, хирургических вмешательствах и ожогах главный индуктор — высвобождение тканевого тромбопластина. В случае осложнений беременности тромбопластин из плаценты, остатков мертвого плода или амниотической жидкости может попадать в кровоток. Гипоксия, ацидоз и шок, часто присутствующие совместно в случае очень тяжелых заболеваний, также могут вызвать распространенное повреждение эндотелиальных клеток, а присоединяющиеся инфекции ухудшают состояние. Из опухолей с ДВС чаще всего ассоциируются острая промиелоцитарная лейкемия и аденокарциномы легких, поджелудочной железы, толстой кишки и желудка.
Возможные последствия ДВС относят к двум категориям. Во-первых, происходит обширное отложение фибрина в микроциркуляторном русле. Это приводит к ишемии тяжело пораженных или более ранимых органов и микроангиопатической гемолитической анемии, возникающей в результате фрагментации эритроцитов, т.к. им приходится протискиваться через суженные микрососуды. Во-вторых, потребление тромбоцитов и факторов коагуляции и активация плазминогена приводят к геморрагическому заболеванию. Плазмин расщепляет не только фибрин, но и факторы V и VIII, тем самым еще больше снижая их концентрацию. Кроме того, продукты деградации фибрина, образующиеся при фибринолизе, ингибируют агрегацию тромбоцитов, полимеризацию фибрина и тромбин. Все эти нарушения способствуют недостаточному гемостазу при ДВС.
б) Морфология. Тромбы наиболее часто возникают в головном мозге, сердце, легких, почках, надпочечниках, селезенке и печени (в порядке убывания частоты), однако возможно поражение любой ткани. В поврежденных почках могут присутствовать небольшие тромбы в клубочках, вызывающие лишь реактивное набухание эндотелиальных клеток или микроинфаркты и даже двухсторонний кортикальный почечный некроз (в тяжелых случаях). В альвеолярных капиллярах обнаруживаются многочисленные фибриновые тромбы, иногда ассоциированные с отеком легких и экссудацией фибрина с формированием гиалиновых мембран, как при синдроме острого респираторного дистресса. В центральной нервной системе фибриновые тромбы могут вызвать инфаркты, нередко осложненные геморрагиями, с различными неврологическими признаками и симптомами. Значительный интерес представляют проявления со стороны эндокринных органов.
На фоне менингококковой септицемии фибриновые тромбы в микрососудах коры надпочечников, вероятно, служат причиной кровотечений в надпочечники (синдром Уотерхауса-Фридериксена). Послеродовой некроз передней доли гипофиза (синдром Шихена) представляет собой форму ДВС, осложняющую родовую деятельность и роды. При токсемии беременности в плаценте много микротромбов, что объясняет преждевременную атрофию цитотрофобласта и синцитиотрофобласта, встречающуюся в этих условиях. Необычная форма ДВС описана в связи с гигантскими гемангиомами, когда тромбы образуются внутри неоплазии вследствие стаза и повторных травм ломких кровеносных сосудов.
в) Клинические признаки. Начало может быть бурным, как это бывает при эндотоксическом шоке или эмболии околоплодными водами, или незаметным и хроническим, как в случаях карциноматоза или гибели плода внутриутробно с поздней диагностикой этого состояния. Около 50% пациенток имеют осложненную беременность. У этих пациенток ДВС может быть обратим после экстракции погибшего плода. Около 33% пациентов — это больные карциномато-зом. Оставшиеся случаи связаны с различными патологиями, перечисленными ранее.
Невозможно детализировать все клинические проявления, однако некоторые общие формы следует упомянуть. К ним относятся микроангиопатическая гемолитическая анемия, диспноэ, цианоз, дыхательная недостаточность, судороги, кома, олигурия, острая почечная недостаточность, внезапная или прогрессирующая недостаточность кровообращения и шок. В целом острое ДВС, ассоциированное с осложнениями беременности или обширной травмой, характеризуется преимущественно геморрагическим заболеванием, тогда как при хроническом ДВС, например у больных со злокачественными опухолями, на первый план выступают тромботические осложнения. Диагноз ставят по результатам клинического обследования и лабораторных исследований, включая определение уровня фибриногена, тромбоцитов, протромбинового времени, частичного тромбопластинового времени и продуктов деградации фибрина.
Прогноз вариабелен и зависит от основного заболевания. Единственный надежный метод терапии — устранение причины или лечение заболевания, вызвавшего ДВС. Здесь приходится с осторожностью лавировать между Сциллой (тромбозом) и Харибдой (геморрагией). В одних случаях показана антикоагулянтная терапия, в других — прокоагулянтная, однако сделать выбор непросто.
- Рекомендуем ознакомиться со следующей статьей "Строение и функция легких"
Оглавление темы "Патогенез болезней":- Механизмы развития (патогенез) тромботической микроангиопатии
- Механизмы развития (патогенез) кровотечений при нарушении функции тромбоцитов
- Механизмы развития (патогенез) кровотечений при дефиците факторов коагуляции
- Механизмы развития (патогенез) болезни Виллебранда
- Механизмы развития (патогенез) гемофилии А
- Механизмы развития (патогенез) гемофилии В
- Механизмы развития (патогенез) ДВС
- Строение и функция легких
- Виды врожденных аномалий легких
- Механизмы развития (патогенез) ателектаза легкого

