Схема развития хронической почечной недостаточности (ХПН)
Ряд заболеваний почек, сахарный диабет и/или гипертензия в конечном счете ведут к разрушению ткани почек. Если оставшаяся неповрежденная ткань не в состоянии адекватно выполнять свои задачи, разворачивается картина острой почечной недостаточности.
Решающую роль в течении заболевания играет снижение почечной экскреции. Из-за потери нефронов в оставшихся клубочкахувеличивается фильтрация. Уменьшение СКФ приводит к обратно пропорциональномуповышениюуровня креатинина в плазме. Плазменная концентрация реабсорбированных веществ также растет, но менее выраженно, т. к. при почечной недостаточности реабсорбция в почечных канальцах ослаблена.
При недостаточности функций почек реабсорбция Na+ и воды угнетается разнообразными факторами, включая натрийуретические пептиды и ПТГ.
Сниженная реабсорбция Na+ в проксимальных канальцах уменьшает всасывание и других веществ, таких как фосфаты, мочевая кислота, НСO3-, Са2+, мочевина, глюкоза и аминокислоты. ПТГ также угнетает реабсорбцию фосфатов.
Снижение реабсорбции NaCl в восходящей части петли Генле нарушает концентрационный механизм. Поступление большого объема жидкости и NaCI из проксимальных отделов нефрона активирует реабсорбцию Na+ в дистальных отделах нефрона и способствует секреции К+ и ГГ в дистальных отделах нефрона и собирательных трубочках.
В итоге концентрация электролитов в плазме остается практически нормальной даже при значительном снижении СКФ (компенсированная почечная недостаточность). Нарушения проявляются только при падении СКФ ниже 1/4 от нормального уровня. Однако эта компенсация дается ценой сужения регуляторного диапазона: поврежденная почка не в состоянии адекватно увеличить выведение воды, Na+, К+, Н+, фосфатов и т. д. (например, если увеличено их пероральное потребление).
При высоких концентрациях мочевая кислота может осаждаться в виде кристаллов, главным образом в суставах, вызывая подагру. Задержка почками оксидантов усиливает окислительный стресс и воспаление. Окислительный стресс и пониженная почечная элиминация оксидантов увеличивают концентрацию уремических токсинов в плазме (ацетон, диметиларгинин, 2,3-бутиленгликоль, гиппуровая, гуанидинянтарная кислота, метилгуанидин, метилглиоксаль, индолы, фенолы, диметиларгинин, алифатические и ароматические амины, гомоцистеин и т. д.), а также средних молекул (липиды или пептиды с молекулярной массой 300-2000 Да).
Эти вещества оказывают свое токсическое действие посредством различных механизмов. Диметиларгинин, например, ингибирует синтез NO, что приводит к ишемии и повышению АД. Метилглиоксаль вызывает гибель клеток и отрицательно влияет на состояние клеток крови (ускоренная деградация и угнетение функции эритроцитов). Высокая концентрация мочевины дестабилизирует белки и вызывает сморщивание клеток. Вместе стем этот эффект частично нейтрализуется поглощением клеткой веществ, стабилизирующих осмотическое давление (особенно бетаина, глицерофосфорилхолина).
Если мочевина разлагается бактериями, образуется аммиак, который вызывает неприятный залах изо рта (запах мочи) и нарушает работу ЖКТ (тошнота, пептические язвы, диарея). Мочевина и некоторые уремические токсины — продукты белкового метаболизма; следовательно, их концентрацию можно снизить ограничением потребления белка с пищей.
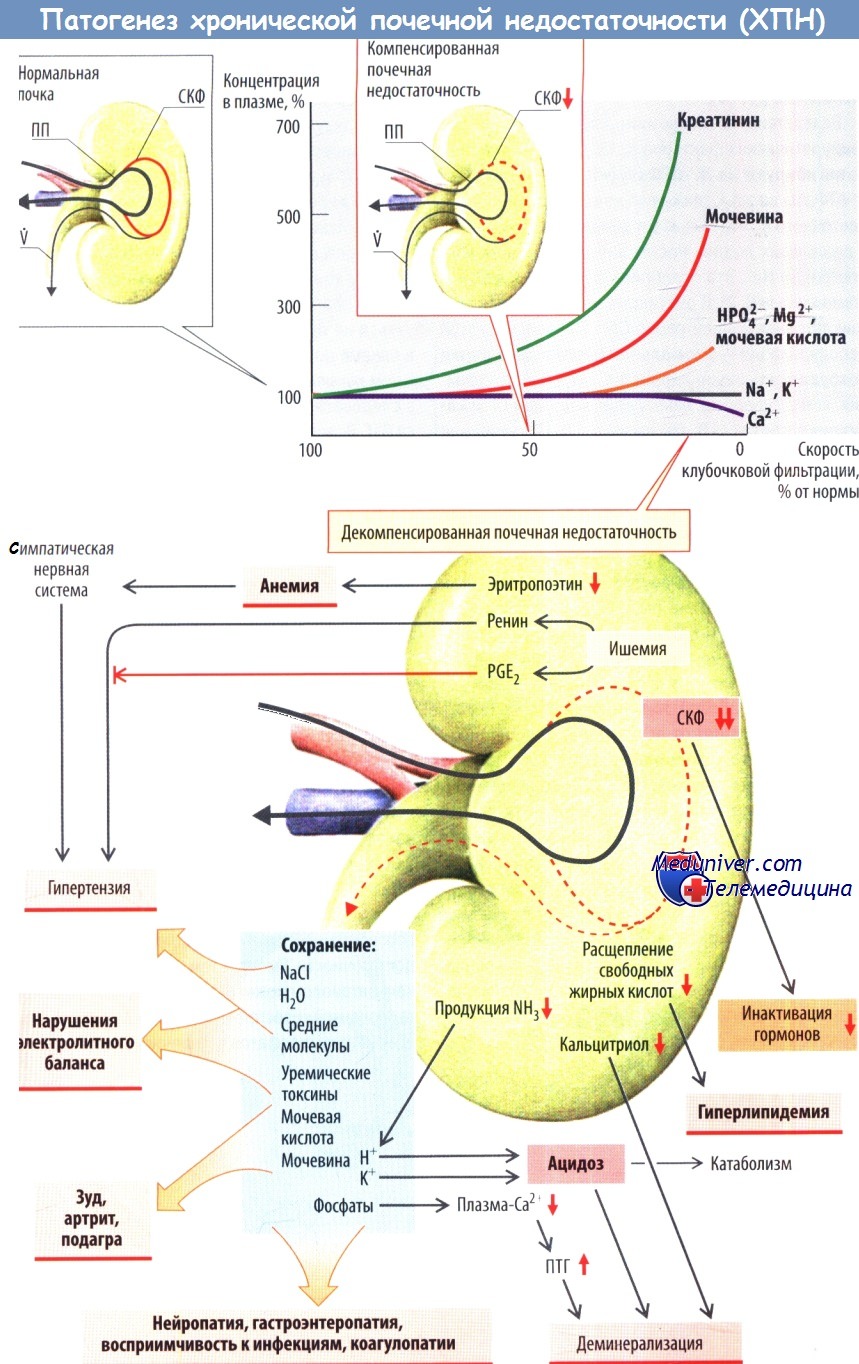
Уменьшение выделения почками эритропоэтина приводит к развитию нефрогенной анемии, что повышает тонус симпатической нервной системы. Внутрипочечное образование ренина и простагландинов может как увеличиваться (например, при ишемии), так и снижаться (гибель ренин- или простагландинпродуцирующих клеток). Увеличенное образование ренина может приводить к развитию гипертензии — частому спутнику почечной недостаточности, в то время как пониженное образование ренина или увеличенное образование простаглан-динов препятствуют ему.
Артериальная гипертензия способствует дальнейшему повреждению почек. При генетически обусловленном повышении активности ангиотензинпревращающего фермента (АПФ) прогрессирование хронической почечной недостаточности ускоряется.
Утрата способности почки инактивировать гормоны замедляет гормональные регуляторные циклы. Отсроченная элиминация инсулина, например, приводит к гипогликемии. Гиперпролактинемия ингибирует выброс гонадотропинов и тем самым понижает в плазме уровень эстрогенов и тестостерона. Последствия этого — аменорея и импотенция.
Пониженное потребление почкой жирных кислот способствует гиперлипидемии, в то время как ослабление глюконеогенеза благоприятствует развитию гипогликемии
Пониженное образование и выведение аммиака приводят к ацидозу, который, в свою очередь, стимулирует катаболизм белков.
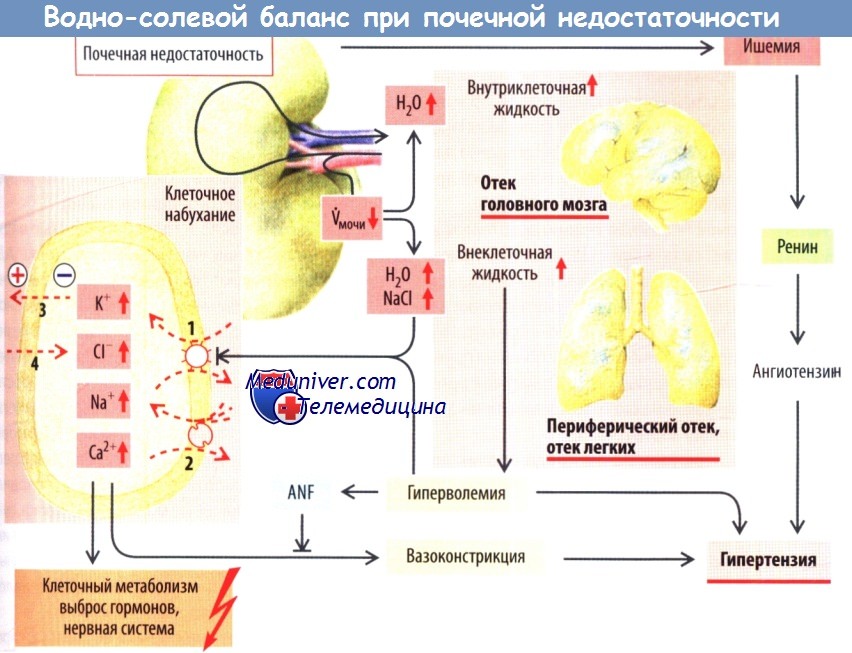
Избыток NaCI и воды обусловливает увеличение объема внеклеточной жидкости, развиваются гиперволемия и отеки; самое опасное осложнение — отек легких. Если отек развивается преимущественно из-за избытка воды, которая поступает в клетку по законам осмоса и увеличивает внутриклеточный объем, возникает опасность отека мозга.
Вследствие гиперволемии происходит выброс натрийуретических факторов, которые частично ингибируют Na+/К+-АТФазу. Угнетение Na+/К+-АТФазы ведет к снижению концентрации внутриклеточного К+, что вызывает деполяризацию клеток в различных тканях. Растет внутриклеточная концентрация Na+. Это ослабляет функцию 3Na+/Ca2+-обменника.
В результате увеличивается внутриклеточная концентрация Са2+. Последствия этой деполяризации — аномальная нервно-мышечная возбудимость (полинейропатия, спутанность сознания, кома, судороги), накопление клетками СП и набухание клеток. Повышенная концентрация внутриклеточного Са2+ вызывает вазоконстрикцию, а также усиливает выброс гормонов (например, гастрина, инсулина) и гормональные эффекты (например, эпинефрина).
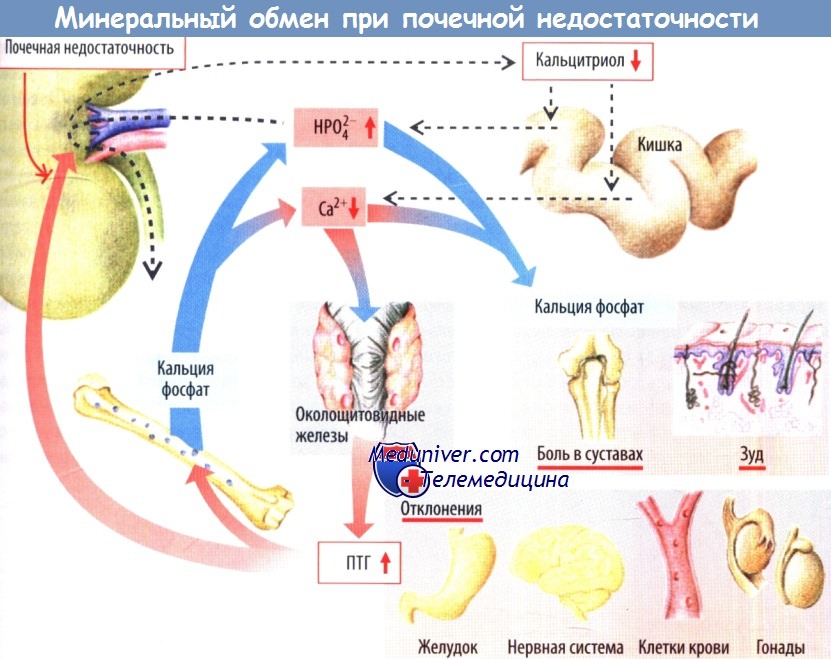
Проявления почечной недостаточности в значительной степени также обусловлены нарушениями минерального обмена. Если СКФ снижается до уровня менее 20 % от нормы, то фосфатов фильтруется меньше, чем всасывается в кишке. Даже если все количество фильтруемых фосфатов выводится, т. е. реабсорбция не происходит, почечная элиминация отстает от всасывания в кишечнике, вследствие чего концентрация фосфатов в плазме растет.
Фосфаты соединяются с Са2+ с образованием плохо растворимого фосфата кальция. Осажденный фосфат кальция (кальцифилаксия) накапливается в суставах (артрит) и коже. Отложение фосфата кальция в сосудистой стенке приводит к обызвествлению сосудов. СаНРO4 менее растворим по сравнению с Са(Н2РO4)2.
При ацидозе образуется преимущественно Са(Н2РO4)2, что препятствует осаждению СаНРO4. Таким образом, коррекция ацидоза при неустраненной гиперфосфатемии благоприятствует обызвествлению сосудов.
При образовании комплекса Са2+ с фосфатами его концентрация в плазме снижается. Гипокальциемия стимулирует выброс ПТГ паратиреоидными железами, который мобилизует фосфат кальция из костей. В результате этого ускоряется деградация костей (фиброзный остеит).
В норме ПТГ уменьшает концентрацию фосфатов в плазме, одновременно угнетая их реабсорбцию в почках, поэтому, несмотря на мобилизацию фосфатов кальция из костей, растворимость фосфатов в плазме не превышает норму, поэтому концентрация Са2+ увеличивается. При почечной недостаточности почечная экскреция увеличиться не может, поэтому концентрация фосфатов в плазме повышается, СаНРO4 осаждается, в связи с чем концентрация Са2+ в плазме остается низкой, а следовательно, продолжается стимуляция выброса ПТГ. Вследствие этой продолжающейся секреторной стимуляции паратиреоидные железы гипертрофируются, устанавливается порочный круг с выделением еще большего количества ПТГ.
Поскольку рецепторы ПТГ помимо почек и костей экспрессируются во многих других органах и тканях (нервной, желудке, клетках крови, железах), ПТГ, возможно, играет определенную роль в развитии изменений в этих органах.
При почечной недостаточности снижается образование кальцитриола, что также влияет на изменение минерального обмена. Обычно этот гормон стимулирует всасывание кальция и фосфатов в кишечнике. Несмотря на то что дефицит кальцитриола уменьшает всасывание фосфатов в кишечнике, гипокальциемия усугубляется. Дефицит кальцитриола способствует развитию почечной остеодистрофии и остеомаляции. Рецепторы кальцитриола имеются в различных органах.
Кальцитриол обладает и иммуносупрессивным свойством, а дефицит кальцитриола способствует усилению воспаления при почечной недостаточности. Вместе с тем заместительная терапия кальцитриолом может оказаться опасной для пациента с почечной недостаточностью вследствие стимуляции всасывания фосфатов в кишечнике.
- Рекомендуем ознакомиться со следующей статьей "Схема повышения давления при болезни почек"
Оглавление темы "Патогенез болезней в схемах":- Схема регуляции почечной экскреции и ее нарушения
- Схема развития нарушений почечного транспорта
- Схема нарушения концентрации мочи почками
- Схема развития поликистоза почек
- Схема развития гломерулонефрита
- Схема развития нефротического синдрома
- Схема развития пиелонефрита (интерстициального нефрита)
- Схема развития острой почечной недостаточности (ОПН)
- Схема развития хронической почечной недостаточности (ХПН)
- Схема повышения давления при болезни почек

