Физиология роста клетки и ее адаптации
В середине 19-го столетия Рудольф Вирхов первый сформулировал концепцию о клеточной патологии. Она заключалась в том, что болезнь есть результат нарушения нормальной жизнедеятельности клетки. Клетка — самая малая единица живого организма (Wilhelm Roux), т. е. именно клетка, а не более мелкая структурная единица способна выполнить основные функции организма: обмен веществ, движение, воспроизводство и наследование. Осуществление трех последних процессов возможно только за счет деления клетки, хотя клетки, которые больше не делятся, могут быть метаболически активными и частично подвижными.
За исключением половых клеток, в которых набор хромосом уменьшается наполовину во время мейотического деления (мейоза), большинство клеток делится после того, как хромосомный набор удваивается, т. е. в результате митоза (так называемого непрямого деления ядер), сопровождающегося делением клетки (цитокинезом). При этом процессе каждая клетка, способная к митозу, претерпевает цикл клеточного воспроизводства (=>А), при котором один эпизод митоза (длящийся около 0,5-2 ч) всегда отделен от следующего интерфазой (длящейся 6-36 ч в зависимости от частоты деления). Важно знать, что клеточный цикл регулируется определенными циклическими фазовоспецифичными белками, или циклина-ми. Они образуют комплекс с протеинкиназами cdc2 или p34cdc2, которые экспрессируются во время всех фаз клеточного цикла.
Когда цитокинез завершен (конец телофазы; =>А), клетки, которые непрерывно делятся (так называемые лабильные клетки), вступают в фазу G1, (Gap-фаза 1), в течение которой они достигают оптимального размера, дифференцируются и выполняют свои тканеспецифические задачи (активный синтез РНК, затем — активный синтез белков. За ней следует S-фаза, которая длится около 8 ч. В течение этой фазы удваивается набор хромосом (активный синтез ДНК). Следующая фаза, G2, длится около 1-2 ч (активный синтез белка и РНК, накопление энергии для последующего митоза, деление центриолей с образованием веретена). После нее начинается следующий митоз. За профазой (де-дифференцировка клеток, например потеря микроворсинок и аппарата Гольджи, спирализация хромосом) следует метафаза (ядерная оболочка разрушается, хромосомы располагаются в экваториальной плоскости).
Далее наступает анафаза (деление хромосом и расхождение их к полюсам), а за ней — телофаза (формирование ядерной оболочки).
Цитокинез начинается в поздней стадии анафазы с образования борозды деления в клеточной мембране. После этого начинается новая вгфаза.
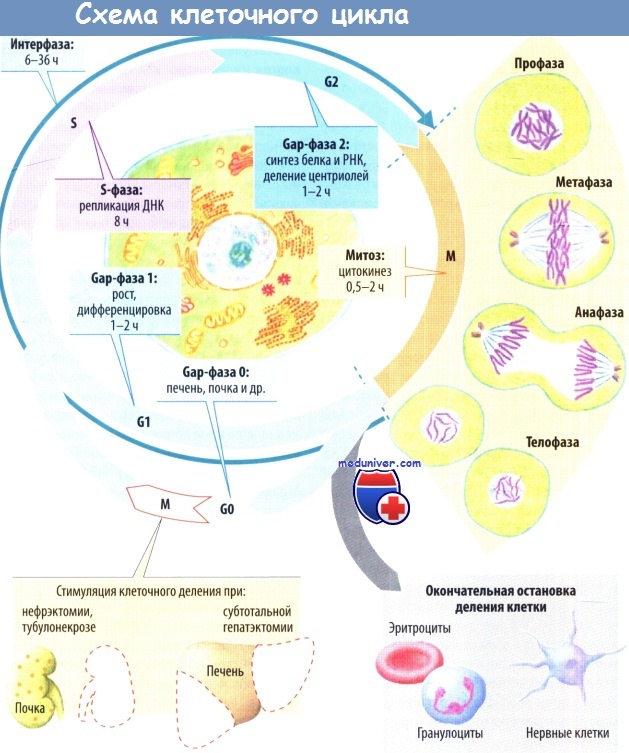
Клетки с короткой продолжительностью жизни (так называемые лабильные) постоянно проходят через этот клеточный цикл, замещая разрушенные клетки и поддерживая общее количество клеток постоянным. К тканям с лабильными клетками относится поверхностный эпителий, например эпителий кожи, слизистой оболочки полости рта, влагалища и шейки матки, эпителий слюнных желез, ЖКТ, желчных путей, матки и нижних отделов мочевых путей, а также клетки костного мозга. Новые клетки большинства этих тканей образуются путем деления недифференцированных стволовых клеток. Одна дочерняя клетка (стволовая клетка) обычно остается недифференцированной, в то время как другие созревают в клетки, не способные к делению, например эритроцит или гранулоцит (=>А). Сперматогенез, в частности, также характеризуется делением с дифференцировкой клеток.
Клетки некоторых органов и тканей в норме не пролиферируют. Такие стабильные, ил и покоящиеся, клетки после митоза вступают в фазу покоя — фазу G0. Примерами их являются паренхиматозные клетки печени, почек, поджелудочной железы, а также соединительной ткани и мезенхимы (фибробласты, эндотелиальные клетки, хондроциты, остеоциты, гладкомышечные клетки). Должны быть специальные стимулы, запускаемые функциональными потребностями, потерей ткани (например, односторонняя нефрэктомия или тубулонекроз, резекция или гибель части печени)или травматизацией ткани (например, повреждение кожи), до того как эти клетки повторно вступят в фазу G1 (=>А, В). В норме в печени делится менее1 %клеток. После резекции печени количество таких клеток составляет уже более 10 %.
Для перехода из фазы G0 в фазу G1 и в целом для запуска клеточной пролиферации необходимо, чтобы произошло связывание факторов роста и гормонов, ускоряющих рост (например, инсулина), со специфическими рецепторами, которые обычно расположены на поверхности клеток. Рецепторы стероидных гормонов находятся в цитоплазме или в ядре клетки (=>С).
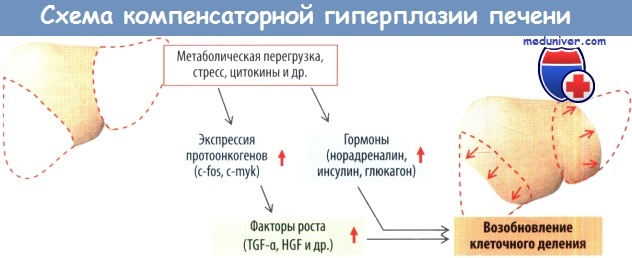
Активация рецепторов факторов роста (обычно под воздействием тирозинкиназы) приводит к фосфорилированию ряда белков. Наконец, сигнальный каскад достигает ядра, происходит стимуляция синтеза ДНК и клетка делится.
Кроме тканеспецифических факторов роста (например, печеночного фактора роста [HGF] в печени), имеются факторы с широким спектром действия: эпидермальный фактор роста (EGF), трансформирующий фактор роста (TGF), тромбоцитарный фактор роста (PDGF), фактор роста фибробластов (FGF), а также ряд цитокинов, таких как интерлейкин-1 (IL-1) и фактор некроза опухолей (TNF). Ингибирование роста возникает после контакта соседних клеток друг с другом, например, в эпителии, в котором дефект закрывается за счет деления клеток (контактное торможение процесса деления клеток). Даже компенсаторный рост печени останавливается (=>В), когда достигается исходная масса органа. Сигналами, отвечающими за регуляцию такого роста, служат TGF-b и интерферон-b.
Регенерация лабильных и стабильных клеток необязательно подразумевает восстановление исходной структуры ткани. Необходимым условием для этого является интактность внеклеточного матрикса, т. к. он служит направляющей системой для формы, роста, миграции и дифференцировки клеток (=>С). Внеклеточный матрикс состоит из волокнистых структурных белков (коллагены I, II и V, эластин) и межклеточного вещества в виде гликопротеидов (например, фибронектина и ламинина), которые погружены в гель из протеогликанов и гликозаминогликанов. Внеклеточный матрикс отграничивается от эпителия, эндотелия и гладкомышечных клеток базальной мембраной (=>Е).
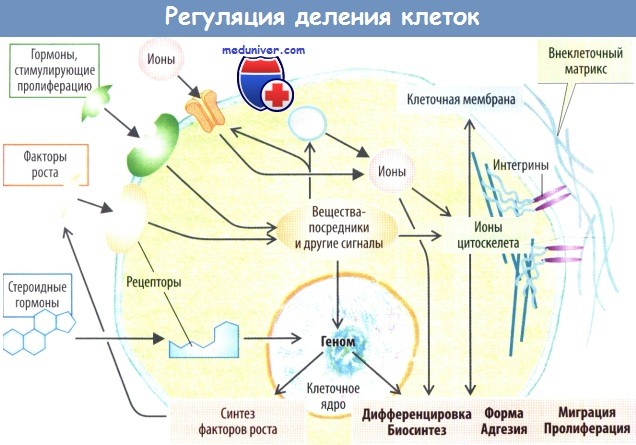
Связь внеклеточного матрикса с внутриклеточным цитоскелетом обеспечивают интегрины — белки клеточной мембраны, которые также передают сигналы для клеточного роста, миграции и дифференцировки во внутреннюю часть клетки (=>С). Если матрикс значительно поврежден, как это случается при выраженном разрушении ткани (например, глубокой язве желудка или обширном ранении кожи), исходная ткань замещается рубцовой. В этом случае пролиферируют покоящиеся в нормальных условиях клетки соединительной ткани и мезенхимы (см. выше).
Погибшие, так называемые перманентные, клетки не восстанавливаются, поскольку они не способны к делению. К таким клеткам, в частности, относятся нервные клетки взрослого человека. Способность к регенерации мышечных клеток сердца и скелетной мускулатуры также очень ограничена (например, см. инфаркт миокарда).
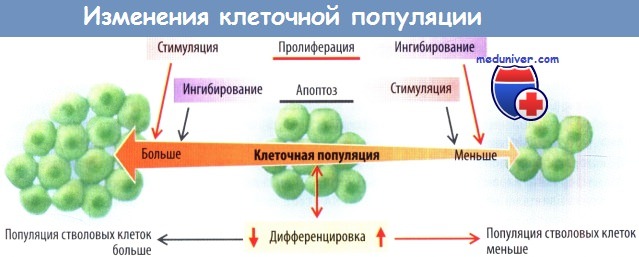
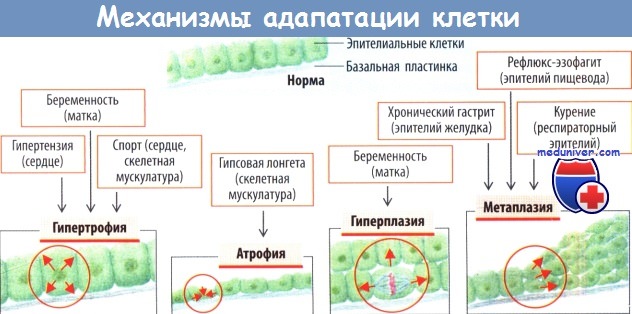
Адаптация к измененным физиологическим или нефизиологическим условиям может достигаться за счет увеличения или уменьшения количества клеток (гиперплазия или гипоплазия; => D. Е). Это может инициироваться гормонами (например, развитие вторичных половых признаков и рост эпителия молочных желез во время беременности) либо быть проявлением процесса компенсации, например, при заживлении ран или после резекции паренхимы печени (=>В). Размеры клеток могут либо увеличиваться (гипертрофия), либо уменьшаться (гипотрофия) (=>Е). Такой вид адаптации также может инициироваться гормонами или возросшими/сниженными потребностями.
Например, во время беременности матка увеличивается за счет гиперплазии и гипертрофии, а скелетная и сердечная мускулатура способна увеличиваться только за счет гипертрофии. Так развивается гипертрофия скелетных мышц в результате тренировок (бодибилдинг) и атрофия от бездействия (например, мышц конечности под гипсовой лонгетой после перелома или при нарушении мышечной иннервации). Гипертрофия сердца развивается в норме у атлетов из-за потребности в высоком сердечном выбросе (велосипедный спорт, лыжные гонки) и в условиях патологии, например у гипертоников. Атрофированные клетки не погибают, их активность может восстанавливаться, за исключением перманентных клеток (например, при атрофии головного мозга). Однако к атрофии и запрограммированной гибели клеток (апоптозу) ведут одинаковые сигнальные пути, поэтому в атрофированной ткани может погибать повышенное число клеток (=>D).
Метаплазия — это обратимая трансформация зрелых клеток одного типа в другой (=>Е). Она тоже развивается, как правило, в результате процессов адаптации. Например, переходный эпителий мочевого пузыря при травматизации почечными камнями подвергается метаплазии в плоский эпителий. То же наблюдается и при рефлюкс-эзофагите или в мерцательном эпителии респираторного тракта узаядлых курильщиков. Замещенный эпителий способен лучше выдерживать нефизиологические условия, однако стимулы, поддерживающие стойкую метаплазию, могут способствовать появлению опухолевых клеток.
- Рекомендуем ознакомиться со следующей статьей "Схема внутриклеточной передачи сигнала и его нарушений"
Оглавление темы "Патофизиология в схемах":- Физиология роста клетки и ее адаптации
- Схема внутриклеточной передачи сигнала и его нарушений
- Фосфатидилинозитол-3-киназа (PI3-киназа) зависимая передача сигнала
- Схема механизма некроза клетки
- Схема механизма апоптоза клетки
- Схема образования опухолевых клеток - онкогенеза
- Схема влияний опухоли на организм - паранеопластических синдромов
- Схема регуляции старения организма человека и длительности его жизни
- Схема повышения температуры тела - лихорадки
- Схема перегревания организма (теплового удара) и злокачественной гипертермии

