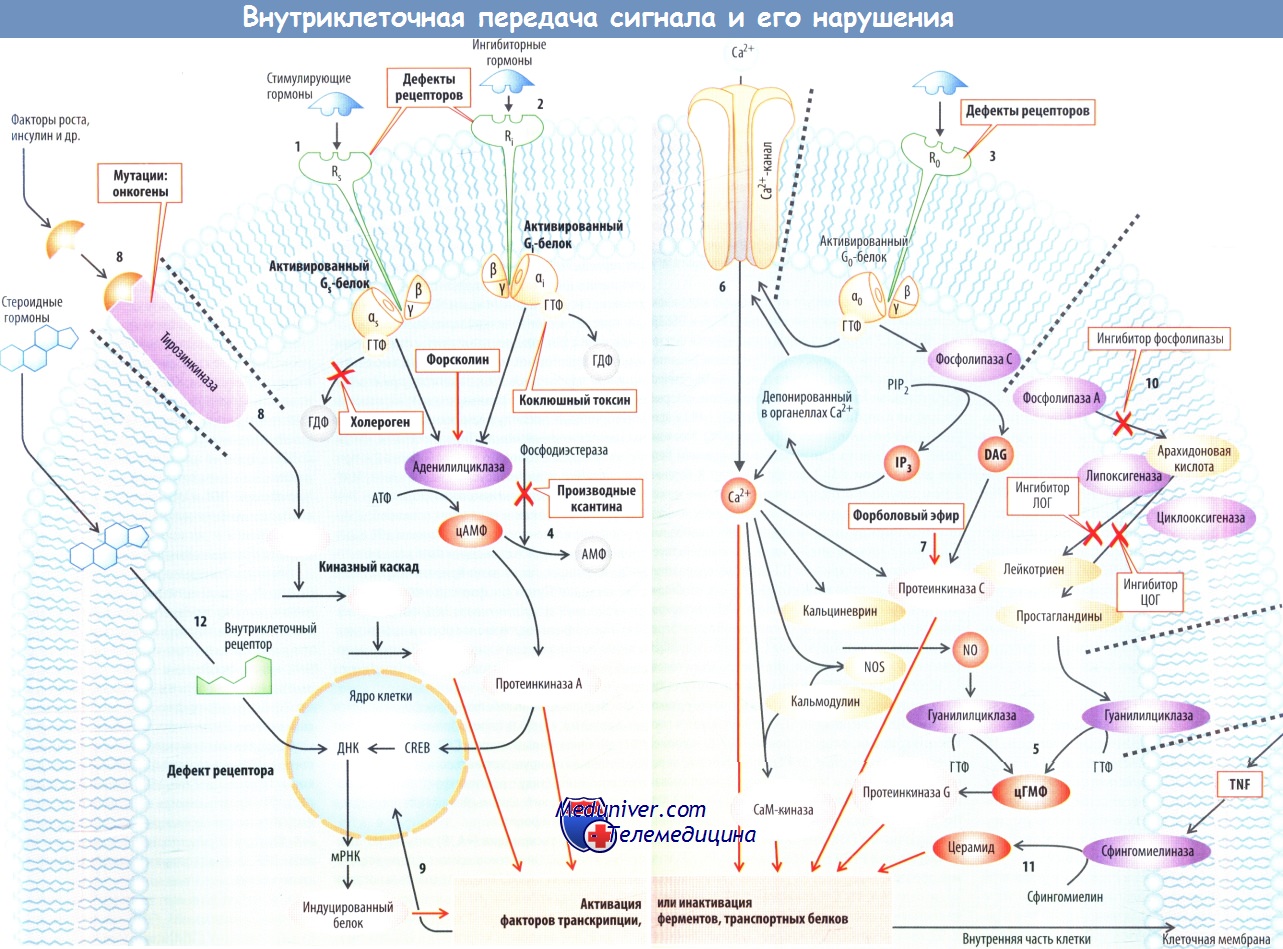
Схема внутриклеточной передачи сигнала и его нарушений
Большинство гормонов взаимодействует с рецепторами клеточных мембран. Взаимодействие гормона с рецептором, обычно через G-белки (белки, связывающие гуаниновые нуклеотиды), вызывает образование второго внутриклеточного посредника, который передает гормональный сигнал внутрь клетки.
Каждый конкретный гормон стимулирует образование различных вторичных внутриклеточных посредников. Нарушения могут возникать в тех случаях, когда снижается число рецепторов (например, при постоянно высоких концентрациях гормона), уменьшается сродство рецептора к гормону или нарушается связь с внутриклеточным сигнальным каскадом (дефекты рецепторов).
Гетеротримерные G-белки состоят из трех субъединиц: а, р и у. Когда гормон связывается с рецептором, гуанозин-5'-трифосфат (ГТФ) связывается с субъединицей а в обмен на гуанозин-5’-дифосфат (ГДФ), а субъединица а отсоединяется от субъединицы р. Активированная по такому пути субъединица а в последующем инактивируется за счет дефосфорилирования ГТФ в ГДФ (внутренняя ГТФаза) и в результате может повторно присоединяться к субъединицам β—у.
Многие пептидные гормоны через стимулятор-ный G-белок (Gs) активируют аденилатциклазу, которая образует циклический аденозинмонофосфат (цАМФ). цАМФ активирует протеинкиназу А (РКА), которая фосфорилируется и, соответственно, влияет на ферменты и транспортные молекулы. цАМФ также может влиять на экспрессию генов через РКА и фосфорилирование цАМФ-чувствительного элементсвязывающего белка (CREB). Внутриклеточные фосфодиэстеразы превращают цАМФ в нециклический АМФ, в результате чего сигнал прекращается.
Через увеличение концентрации внутриклеточного цАМФ действуют следующие гормоны: кортикотропин (адренокортикотропный гормон [АКТГ]), лютеотропин (лютеинизирующий гормон [ЛГ]), тиреотропин (тиреотропный гормон [ТТГ]), пролактин, соматотропин (соматотропный гормон [СТГ]), некоторые из либеринов (рилизинг-гормоны) и статины (рилизинг-ингибирующие гормоны), глюкагон, паратиреоидный гормон (ПТГ), кальцитонин, адиуретин (антидиуретический гормон [АДГ], V2-рецепторы), гастрин, секретин, вазоактивный интестинальный пептид (ВИП), окситоцин, аденозин (A2-рецептор), серотонин (S2-рецептор), дофамин (D1-рецептор), гистамин (Н2-рецептор) и простагландины.
Некоторые пептидные гормоны и нейротрансмиттеры, например соматостатин, аденозин (A1-рецептор), серотонин (S1α), ангиотензин II, ацетилхолин (М2-рецептор), действуют за счет подавления аденилатциклазы и тем самым уменьшают концентрацию внутриклеточного цАМФ через ингибирующий G-белок (Gi)). Ряд гормонов, связываясь с различными рецепторами, может как повышать концентрацию цАМФ (адреналин: b-рецептор; дофамин: D1-рецептор), так и понижать ее (адреналин: а2-рецептор; дофамин: D2-рецептор).
На сигнальный каскад цАМФ могут влиять токсины и лекарственные вещества, а именно холероген Vibrop cholerae и другие токсины, которые препятствуют деактивации αs-субъединицы. В результате происходит неконтролируемая активация аденилатци-клазы и впоследствии цАМФ-зависимых Cl--каналов, что из-за безудержной секреции NaCI в просвет кишки приводит к тяжелой диарее. Коклюшный токсин, выделяемый Hemophilus pertussis, блокирует Gi-белок и тем самым повышает, в частности, концентрацию цАМФ (растормаживаниеаденилатциклазы).
Форсколин непосредственно стимулирует аденилатциклазу, в то время как производные ксантина, например теофиллин или кофеин, ингибируют фосфодиэстеразу и, следовательно, распад цАМФ. Тем не менее действие производных ксантина преимущественно основано на ингибировании пуринергических рецепторов.
Помимо цАМФ внутриклеточным проводником является циклический гуанозинмонофосфат (цГМФ). цГМФ образуется при участии гуанилилциклазы. цГМФ достигает своего эффекта в первую очередь за счет активации протеинкиназы G (PKG). Предсердный натрийуретический фактор (ANF) и оксид азота (NO) наряду с некоторыми другими факторами также действуют через цГМФ.
К другим внутриклеточным медиаторам относятся 1,4,5-инозитолтрифосфат (IР3), 1,3,4,5-инозитол-тетракифосфат (IР4) и диацилглицерин (DAG). После активации G0-белком мембраносвязанная фосфолипаза С (PLC) расщепляет фосфатидилинозитолдифосфат (РIР2) до IР3 и DAG. Эта реакция запускается, в частности, адреналином (а1), ацетилхолином (М1-рецептор), гистамином (Н1-рецептор), АДГ (V1-рецептор), панкреозимином (ССК), ангиотензином II, тиреолиберином (ТТГ), веществом Р и серотонином (S1-рецептор). IP3 высвобождает Са2+ из внутриклеточных депо. Опорожнение депо открывает Са2+-каналы в клеточной мембране.
Са2+ также может входить в клетку через лигандзависимые Са2+-каналы. Са2+ частично связан с кальмодулином и посредством последующей активации кальмоду-линзависимой киназы (СаМ-киназы) влияет на множество клеточных функций, таких как эпителиальный транспорт, секреция гормонов и клеточная пролиферация. DAG и Са2+ стимулируют протеинкиназу С (РКС), которая, в свою очередь, регулирует другие киназы, факторы транскрипции (см. ниже) и цитоскелет. РКС также активирует Na+/H+-обменник, что приводит к ощелачиванию цитозоля и увеличению объема клетки. Этот путь влияет на многочисленные функции клеток, среди которых метаболизм, активация К'-каналов и клеточное деление. РКС активируется форболовыми эфирами.
Са2+ активирует эндотелиальную NO-синтазу (NOS), которая освобождает NO от аргинина. NO стимулирует PKG, например, в гладкомышечных клетках, что способствует выталкиванию Са2+ и уменьшению его концентрации в цитозоле, а следовательно, ведет к расширению сосудов. В дальнейшем NO проявляет свое действие за счет нитрозилирования белков.
Инсулин и факторы роста активируют тирозинкиназы, которые сами могут быть частью рецепторов или присоединяться к рецептору при его стимуляции. Киназы часто реализуют свою активность, фосфорилируя последующие киназы и вызывая тем самым киназный каскад. Тирозинкиназы, например, активируют с помощью малого G-белка Ras протеинкиназу Raf, которая запускает через киназу МАР-киназы МАР (митоген-активированную) киназу. Этот эффект «снежного кома» приводит к лавинообразному усилению клеточного сигнала. Киназы р38 и Jun, которые регулируют экспрессию генов через факторы транскрипции, также активируются посредством таких каскадов.
Путем фосфорилирования фактора транскрипции Stat тирозинкиназа Jak1 опосредует эффекты интерферонов, гормонов роста и пролактина. Активин, антимюллеров гормон и TGF-b сходным образом регулируют фактор транскрипции Smad через серин/треонинкиназу.
Фосфорилированные белки дефосфорилируются фосфатазами, которыетаким образом прекращают действие киназ. Кальциневрин, Са2+-активированная фосфатаза, активирует, кроме того, ядерный фактор NFAT, который наряду с другими факторами способствует гипертрофии гладкомышечных клеток сосудов и активации Т-лимфоцитов.
Факторы транскрипции регулируют синтез новых бел ков. Они перемещаются в ядро и связываются с соответствующими последовательностями ДНК, контролируя таким образом экспрессию генов. Факторы транскрипции могут регулироваться путем фосфорилирования.
Деградация белков также находится под строгим контролем. Убиквитинлигазы прикрепляют сигнальный пептид убиквитин к соответствующим белкам. Убиквитинированные белки разрушаются через протеосомный путь. Регулирование убиквитинлигаз происходит за счет фосфорилирования.
Арахидоновая кислота, являющаяся полиненасыщенной жирной кислотой, может отщепляться от липидов мембраны, включая DAG, фосфолипазой А. Сама по себе арахидоновая кислота оказывает ряд клеточных воздействий (например, на ионные каналы). В результате действия циклооксигеназы (ЦОГ) она может также превращаться в проста-гландины и тромбоксан, действие которых частично проявляется за счет активации аденилилциклазы и гуанилилциклазы. Кроме того, арахидоновая кислота может превращаться в лейкотриены под воздействием липоксигеназы (ЛОГ). Простагландины и лейкотриены играют большую роль в воспалении) и служат не только внутриклеточными посредниками, но и внеклеточными медиаторами.
Ингибиторы ЛОГ и ЦОГ, которые часто используют в терапевтических целях (например, для подавления воспаления и агрегации тромбоцитов), подавляют образование лейкотриенов и простагландинов.
Некоторые медиаторы (например, TNF и CD95 [Fas/Apo1] лиганд) активируют кислую сфингомиелиназу, которая образует церамид из сфингомиелина. Церамид запускает серию клеточных эффектов, таких как активация малых G-белков (например, Ras), киназ, фосфатаз и каспаз, т. е. протеаз, которые расщепляют белки в участках цистеин — аспартат. Эффекты церамида особенно важны в передаче сигнала при апоптотической гибели клетки.
Стероидные гормоны (глюкокортикоиды, альдостерон, половые гормоны), гормоны щитовидной железы (TR), кальцитриол (VDR), ретиноиды (RAR) и липиды (PPAR) связываются с внутриклеточными (цитоплазматическими или ядерными) рецепторами белков. Гормон-рецепторный комплекс присоединяется к ДНК клеточного ядра и таким образом регулирует синтез белка.
- Рекомендуем ознакомиться со следующей статьей "Фосфатидилинозитол-3-киназа (PI3-киназа) зависимая передача сигнала"
Оглавление темы "Патофизиология в схемах":- Физиология роста клетки и ее адаптации
- Схема внутриклеточной передачи сигнала и его нарушений
- Фосфатидилинозитол-3-киназа (PI3-киназа) зависимая передача сигнала
- Схема механизма некроза клетки
- Схема механизма апоптоза клетки
- Схема образования опухолевых клеток - онкогенеза
- Схема влияний опухоли на организм - паранеопластических синдромов
- Схема регуляции старения организма человека и длительности его жизни
- Схема повышения температуры тела - лихорадки
- Схема перегревания организма (теплового удара) и злокачественной гипертермии

