Схема регуляции старения организма человека и длительности его жизни
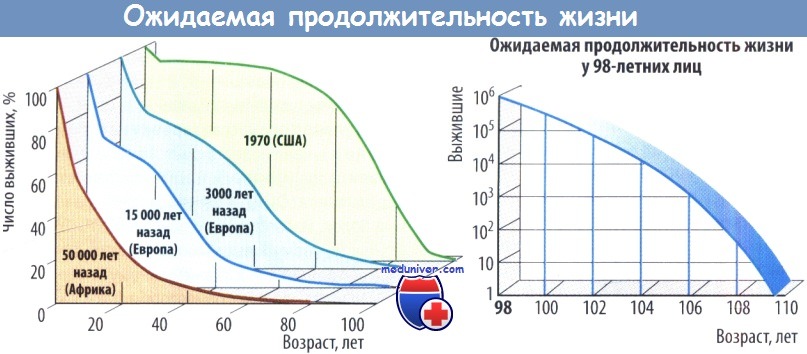
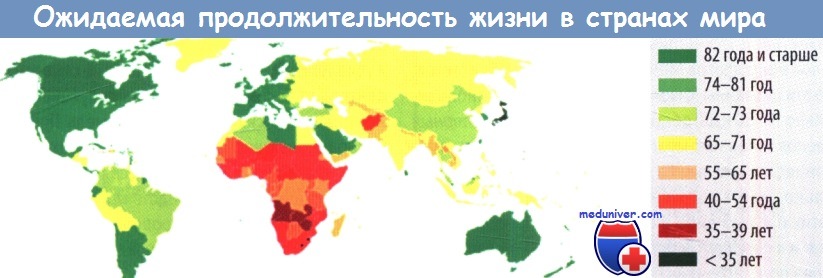
Старение — естественный, неизбежный процесс, который заканчивается смертью. Средняя ожидаемая продолжительность жизни новорожденного 50 000 лет тому назад составляла, по оценкам специалистов, около 10 лет, в древнем Риме — приблизительно 25 лет, в 2006 г. она составляла от 34 (Свазиленд) до 83 лет (Андорра).
Ожидаемая продолжительность жизни зависит от пола; так, в Германии она составляет 76,9 года для мужчин и 82,3 года для женщин. С возрастом средняя ожидаемая продолжительность жизни растет, поскольку человек, доживший до определенного возраста, никак не может умереть раньше этого возраста.
В Германии средняя ожидаемая продолжительность жизни в 2008 г. составляла 82 года для 70-летнего мужчины и 85 лет для 70-летней женщины. Рост средней ожидаемой продолжительности жизни обусловлен прежде всего снижением детской смертности и эффективным лечением инфекционных заболеваний (особенно у детей).
Именно эти факторы определили заметный рост продолжительности жизни в индустриально развитых странах за последние 100 лет (например, в США — с 42 до 74 лет у мужчин и до 80 лет у женщин). Основными причинами смерти стали болезни, характерные для пожилого возраста; приблизительно 50 % составляют болезни сердечнососудистой системы, 25 % — опухоли.
Эти болезни мешают человеку прожить максимальную продолжительность жизни, которая, как сейчас полагают, составляет около 100 лет. Так, среди доживших до 98 лет только 10 % будут живы через 3 года и всего 0,005 % — через 10 лет. Мировой рекорд (122 года) установлен француженкой Jeanne Calment, и это редчайшее исключение.
Многие наследственные болезни и наследственные (часто полигенные) факторы риска опосредованно влияют на продолжительность жизни, например спо-собствуя развитию некоторых опухолей. Однако исследования у монозиготных (однояйцовых) близнецов показали, что по крайней мере 2/3 вариабельности величины продолжительности жизни не являются генетически предопределенными.
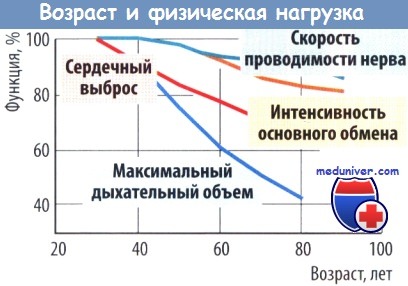
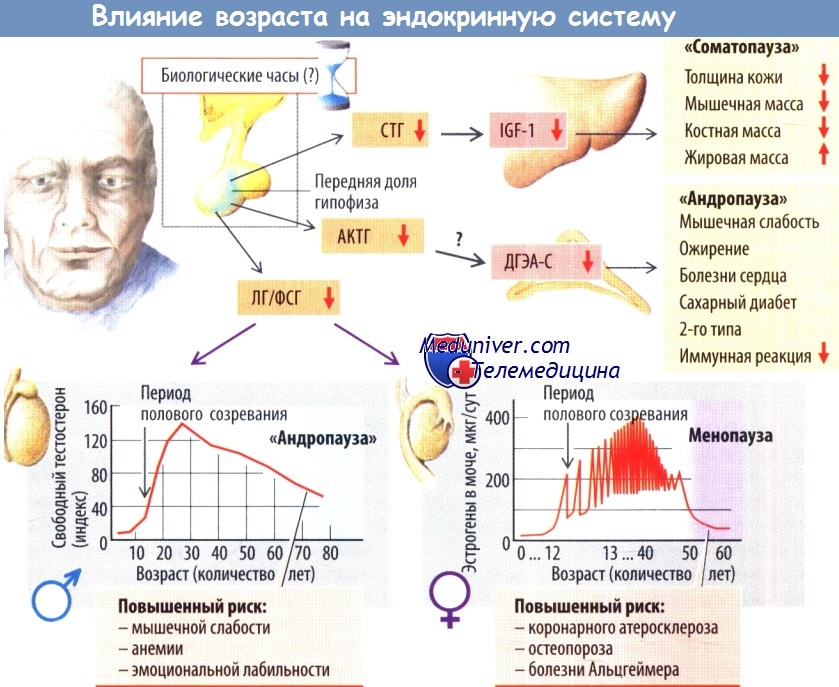
По мере старения происходит снижение витальных функций: уменьшается максимальная емкость легких, сердечный выброс, максимальное поглощение кислорода, скорость клубочковой фильтрации в почках и т. п. Уменьшается мышечная и костная масса, в то время как количество жира растет, в основном из-за эндокринных факторов.
Ввиду этого именно телесная дряхлость становится ограничивающим фактором для большинства очень старых людей, здоровых во всем остальном. Эта слабость пожилого возраста характеризуется уменьшением мышечной силы, замедлением рефлексов, сниженной подвижностью и равновесием, а также пониженной выносливостью. Результатом бывают падения, переломы, сниженная дневная физическая активность и потеря способности к самообслуживанию.
Мышечная слабость вызвана не только процессами физиологического старения и износа, проявлением чего служат, например, повреждения суставов, но и недостаточной подвижностью, что порождает порочный круг.
Старение иммунной системы (иммуносенильность) также способствует возрастным изменениям. С возрастом снижается эффективность механизмов как врожденного (естественные киллеры [NК], нейтрофилы, моноциты/макрофаги, дендритные клетки), так и приобретенного иммунного ответа (Т- и В-лимфоциты). У пожилых людей активация иммунного ответа замедляется; защита, обеспечиваемая вакцинацией, ухудшается, а восприимчивость к инфекционным заболеваниям, опухолевому росту и аутоиммунным болезням повышается. Соответственно, увеличивается заболеваемость и смертность.
Согласно результатам проведенного в Швеции исследования характеристик иммунного риска, у 80- и 90-летних людей установлен повышенный уровень Т-клеток CD8+ (характерный для ЦМВ-инфекции), сниженная концентрация Т-клеток CD4+ и В-клеток CD19+, а также недостаток CD28 — дополнительного стимулятора Т-клеточной активации. Установлена связь повышенного иммунного риска с персистирующей цитомегаловирусной (ЦМВ) инфекцией.
Было сделано заключение, что иммуносенильность развивается вследствие хронической стимуляции антигенами (например, ЦМВ).
Возрастные проблемы с памятью (особенно проблемы с ориентировкой в незнакомом окружении), вероятно, вызваны нарушениями долгосрочной потенциации нейронов в коре головного мозга и гиппокампе (сниженная плотность рецепторов глутамата типа NMDA в зубчатой извилине). В настоящее время точно не установлено, является ли существенное уменьшение количества нейронов (например, при болезни Альцгеймера или снижении церебрального кровотока, связанном с атеросклерозом) частью нормального процесса старения.
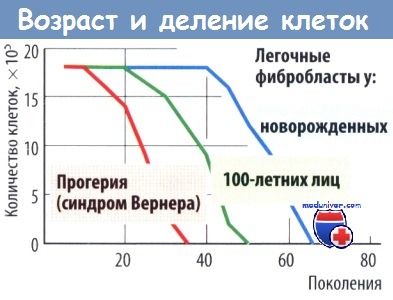
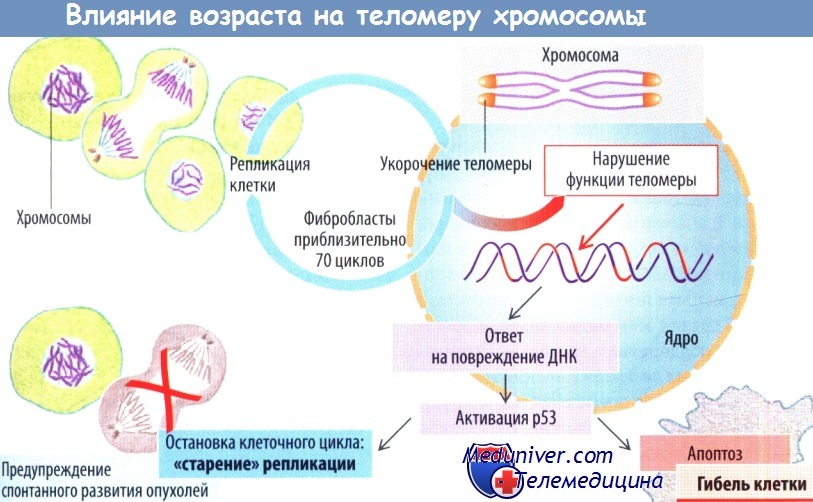
Причины старения остаются плохо изученными. Клетки в клеточных культурах также «стареют»; в частности, они прекращают делиться после определенного числа циклов репликации (например, фибробласты фетального легкого — после приблизительно 70 делений). Лишь некоторые клетки «бессмертны» (т. е. обладают неограниченной способностью к делению), например клетки гонад, гемопоэтические стволовые клетки, патологические опухолевые клетки.
Репликативное старение представляет собой нарушение клеточного деления, связанное с возрастом. Подобно апоптозу, репликативное старение предотвращает рост опухолей in vivo. Соматические мутации, поражающие клетки в массе пролиферирующих клеток, могут приводить к возникновению опухолей. Противоопухолевым барьером является теломера — специализированный нуклеопротеидный комплекс, расположенный на концах хромосом. В соматических клетках теломера укорачивается с каждым циклом клеточного деления.
Репликация клеток в течение нескольких поколений (например, для человеческих фибробластов — в течение примерно 70 циклов) приводит к постепенному укорочению теломеры, что в конечном итоге вызывает нестабильность генома и тем самым повышает риск развития опухолей. Этот риск снижается путем «автоматической» активации р53-пути при нарушении функции теломеры. Путь р53 останавливает дальнейшую репликацию клетки (репликативное старение) и/или стимулирует апоптоз пораженных клеток. Теломераза — фермент, восстанавливающий укороченную теломеру, препятствует старению. У людей теломераза активна в клетках гонад, но выключена в соматических клетках с низкой пролиферативной активностью.
В противоположность этому теломеразная активность делает стволовые клетки опухолей «бессмертными», позволяя им неограниченно делиться. Использование ингибиторов теломеразы, равно как и иммунизация против нее, служит, таким образом, новым терапевтическим подходом, позволяющим контролировать опухолевый рост.
Продолжительность жизни и старение отчасти генетически детерминированы. Многие врожденные болезни и наследуемые (часто полигенно) факторы риска оказывают опосредованное влияние на продолжительность жизни, например, способствуя формированию определенных опухолей. Однако исследования у монозиготных (однояйцовых) близнецов показали, что не менее 2/3 вариабельности срока продолжительности жизни не являются генетически детерминированными.
Некоторые генетические болезни приводят к значительному укорочению продолжительности жизни. Например, крайне редкая мутация в гене LMNA, локализованном на хромосоме 1, приводит к дефекту белка ламинина А (прогерина), который экспрессируется в оболочке клеточного ядра. Вызванное этим нарушение клеточного деления обусловливает прогерию типа I (синдром прогерииХатчинсона—Гилфорда), которая характеризуется преждевременным старением кожи, костей и сердечно-сосудистой системы с первого года жизни. В результате дети редко доживают до зрелого возраста.
Мутации в гене RECQL1, локализованном на хромосоме 8, который кодирует ДНК-хеликазу, приводят к нарушению процесса репарации ДНК. Развивается болезнь, ведущая к преждевременному старению взрослых лиц (так называемая progeria adultorum. прогерия взрослых = болезнь Вернера = прогерия типа II).
Известны некоторые мутации или делеции генов (например, age-1, sgk), которые приводят к возрастанию продолжительности жизни нематоды Caenorhabditis elegans в несколько раз. Мутация age-1 повышает устойчивость к оксидативному стрессу. У людей окислительные повреждения аналогичным образом способствуют старению, поскольку уровень повреждения липидов мембран, ДНК и белков радикалами O2 у пожилых лиц повышается, а активность ферментов, осуществляющих антиоксидантную защиту, снижается.
Регуляция процесса старения на молекулярном уровне изучена недостаточно. На интенсивность старения и продолжительность жизни оказывает выраженное влияние KLOTHO — однопроходной трансмембранный белок. Избыточная экспрессия KLOTHO приводит ксущественному повышению продолжительности жизни, а его делеция — к значительному ее укорочению.
KLOTHO связывается с рецептором фактора роста фибробластов (FGF23); данный комплекс подавляет образование 1,25(OH)2D3 (кальцитриола) и участвует в регуляции кальций/фосфатного гомеостаза. Недостаток KLOTHO или FGF23 приводит к гиперфосфатемии и ги-перкальциемии, что, в свою очередь, ведет к ускоренному старению. Дефицит витамина D повышает продолжительность жизни KLOTHO-дефицитных мышей. Таким образом, по крайней мере частично ускоренное старение KLOTHO-дефицитных мышей обусловлено избыточным образованием кальцитриола. У людей также был выявлен полиморфизм гена KLOTHO. связанный с феноменом долгожительства. Таким образом, ген KLOTHO может иметь столь же большое значение и для человека.
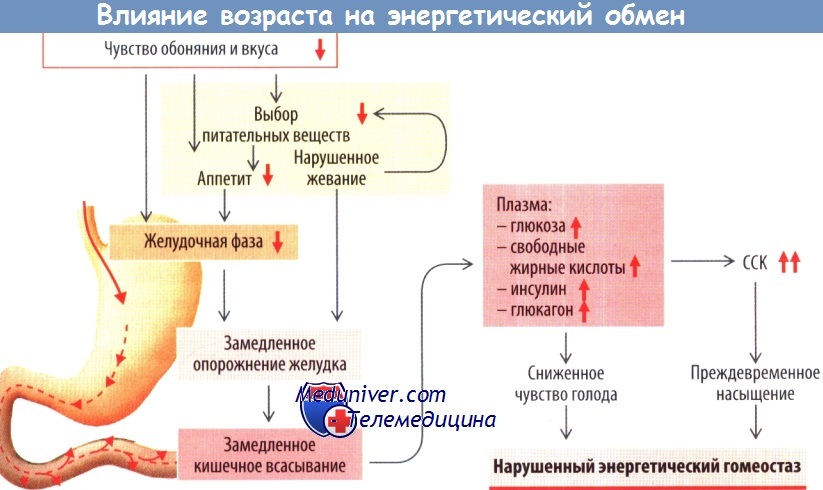
Низкокалорийная диета увеличивает продолжительность жизни как людей, так и животных. Данный эффект может быть обусловлен снижением концентрации глюкозы натощак в плазме, снижением уровня плазменного холестерина, повышением чувствительности к инсулину, уменьшением объема висцеральной жировой ткани, а также сниженным уровнем высвобождения адипокинов из указанной ткани. Все эти параметры известны как факторы риска ишемической болезни сердца.
Поскольку низкокалорийную диету трудно соблюдать, в настоящее время ведется поиск гормональных и метаболических механизмов, ответственных за влияние такой диеты на процессы старения, с целью воспроизвести ее положительное влияние на продолжительность жизни, не заставляя людей воздерживаться от своих пищевых предпочтений.
Благоприятный эффект от низкокалорийной диеты может быть обусловлен веществом из полифенольной группы — ресвератролом, который содержится в красном вине и, возможно, ответствен за так называемый французский парадокс, т. е. положительное влияние красного вина на продолжительность жизни. Ресвератрол активирует гены,кодирующие сиртуины (Sirtl-7) — NAD-зависимые деацетилазы. В некоторых случаях Sirtl повышали устойчивость к окислительному стрессу и продолжительность жизни. Влияние на продолжительность жизни частично обусловлено кардиопротективным эффектом данного фермента. Тем не менее до настоящего времени неясно, влияет ли экспрессия Sirtl на процессы старения у людей.
- Рекомендуем ознакомиться со следующей статьей "Схема повышения температуры тела - лихорадки"
Оглавление темы "Патофизиология в схемах":- Физиология роста клетки и ее адаптации
- Схема внутриклеточной передачи сигнала и его нарушений
- Фосфатидилинозитол-3-киназа (PI3-киназа) зависимая передача сигнала
- Схема механизма некроза клетки
- Схема механизма апоптоза клетки
- Схема образования опухолевых клеток - онкогенеза
- Схема влияний опухоли на организм - паранеопластических синдромов
- Схема регуляции старения организма человека и длительности его жизни
- Схема повышения температуры тела - лихорадки
- Схема перегревания организма (теплового удара) и злокачественной гипертермии

