Патогенез поражения ионизирующей радиацией
Радиация — это энергия, которая движется в форме волн или высокоскоростных частиц. У радиации широкий диапазон энергий, в рамках электромагнитного спектра. Выделяют неионизирующую и ионизирующую радиацию. Энергия неионизирующей радиации (ультрафиолетовое и инфракрасное излучение, микроволны и звуковые волны) может перемещать атомы в молекулах или заставить их колебаться, но ее недостаточно, чтобы оторвать электрон от атома.
Напротив, ионизирующая радиация обладает достаточной энергией, чтобы оторвать электрон. Столкновение электронов с другими молекулами запускает каскад реакций, называемых ионизацией. Основные источники ионизирующей радиации: рентгеновские лучи и у-лучи (электромагнитные волны высоких частот), высокоэнергетические нейтроны, а-частицы (состоят из двух протонов и двух нейтронов) и b-частицы (являются по существу электронами).
Около 25% суммарной дозы ионизирующей радиации, получаемой населением США, можно считать рукотворной, большей частью возникающей при использовании медицинского оборудования и радиоизотопов.
Ионизирующее излучение незаменимо в медицинской практике при лечении злокачественных опухолей, диагностической визуализации и в качестве терапевтических или диагностических радиоизотопов. Но оно также обладает неблагоприятными кратко- и долгосрочными эффектами, такими как фиброз, мутагенез, канцерогенез и тератогенез.
Единицы измерения радиации. Для описания дозы излучения используют три термина в зависимости от того, что измеряют:
- количество излучения, испускаемого источником, измеряют в кюри (Кю). Эта единица измерения определяет количество распадов в секунду самостоятельно распадающихся радиоизотопов. 1 Кю = 3,7 х 1010 распадов в секунду;
- дозу облучения, поглощенную телом человека, измеряют в греях (Гр). Эта единица отражает количество поглощенной тканью энергии на единицу ее массы. 1 Гр соответствует поглощению 104 эрг/г ткани. Сантигрей (сГр) — поглощение 100 эрг/г ткани — эквивалентен воздействию на ткани 100 рад, сокращенно R. В настоящее время единицу измерения сГр используют чаще всего;
- биологический эффект излучения измеряют в зивертах (Зв). Это единица эквивалентной дозы, зависящая от биологических, а не физических свойств облучения (заменила единицу измерения рем). При одинаковой поглощенной дозе разные типы облучения различаются по степени повреждения, которое они вызывают. Эквивалентная доза уравнивает это различие и обеспечивает однородность измерения.
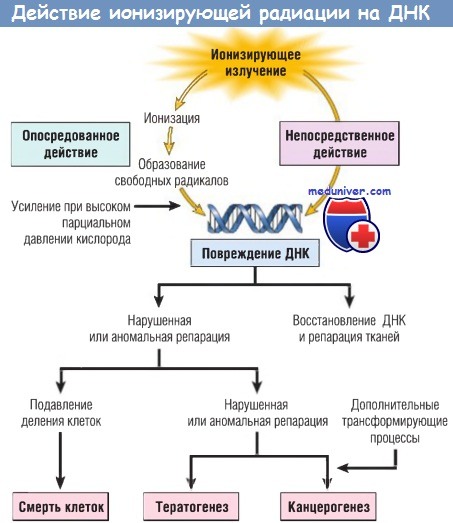
Воздействие на ДНК может быть непосредственным и опосредованным (за счет образования свободных радикалов).
ДНК — дезоксирибонуклеиновая кислота.
Эквивалентная доза (выраженная в Зв) соответствует поглощенной дозе (выраженной в Гр), умноженной на относительную биологическую эффективность радиации. Относительная биологическая эффективность зависит от вида излучения, типа и объема ткани, подвергнутой воздействию, продолжительности воздействия и некоторых других биологических факторов (см. далее). Эффективную дозу рентгеновских лучей при компьютерной томографии и других визуализирующих исследованиях обычно выражают в миллизивертах (мЗв). Для рентгеновского излучения 1 мЗв = 1 мГр.
Основные факторы, определяющие биологическое действие ионизирующей радиации. Помимо к физических свойств излучения биологические эффекты сильно зависят от:
- времени воздействия. Воздействие радиации кумулятивно, однако в промежутках между облучением фракционными дозами клетки могут устранить некоторые повреждения. Иначе говоря, фракционные дозы лучевой энергии обладают кумулятивным эффектом только в том случае, когда репарация между воздействиями неполная. При радиотерапии опухолей используют способность нормальных клеток к быстрой репарации (более быстрой, чем у опухолевых клеток), избегая большого кумулятивного радиационного поражения;
- площади облучения. Размер облученной области тела значительно влияет на последствия. Организм может переносить относительно высокие дозы облучения при поражении небольших, хорошо отграниченных областей, тогда как меньшие дозы, но действующие на большую площадь, могут привести к летальному исходу;
- клеточной пролиферации. Поскольку ионизирующая радиация повреждает ДНК, быстро делящиеся клетки более уязвимы для повреждения, чем неделящиеся. За исключением чрезвычайно высоких доз, ослабляющих транскрипцию ДНК, повреждение ДНК совместимо с выживанием неделящихся клеток. Однако после нанесения непоправимого ущерба ДНК во время митоза клетки умирают, т.к. хромосомные аномалии останавливают процесс деления. Именно поэтому ткани с высокой скоростью обмена клеток (гонады, костный мозг, лимфатическая ткань и слизистая оболочка ЖКТ) чрезвычайно уязвимы для радиации и повреждение их проявляется раньше других;
- эффектов кислорода и гипоксии. Важнейшим механизмом повреждения ДНК ионизирующей радиацией является образование АФК при радиолизе воды или взаимодействии с молекулярным кислородом (теория косвенной мишени). Плохо васкуляризованные ткани, находящиеся в состоянии гипоксии, например центральная часть быстрорастущих опухолей, менее устойчивы к лучевой терапии; - повреждения сосудов. Повреждение эндотелиальных клеток, умеренно чувствительных к радиации, может вызвать сужение или окклюзию кровеносных сосудов, привести к нарушению репаративных процессов, фиброзу и хронической ишемической атрофии.
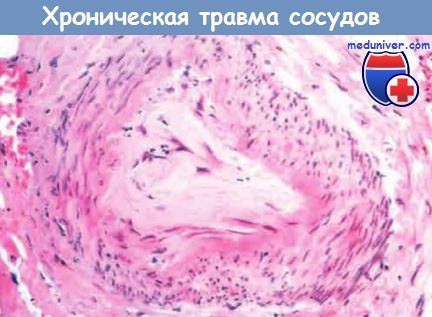
окклюзирующего просвет.
Эти изменения могут наблюдаться спустя месяцы или даже годы после воздействия. Поздними изменениями тканей с низким уровнем пролиферации, таких как мозг, почки, печень, мышцы и подкожная жировая клетчатка, могут быть смерть клеток, атрофия и фиброз. Эти эффекты связаны с поражением сосудов и высвобождением провоспалительных цитокинов в облученных областях тела.
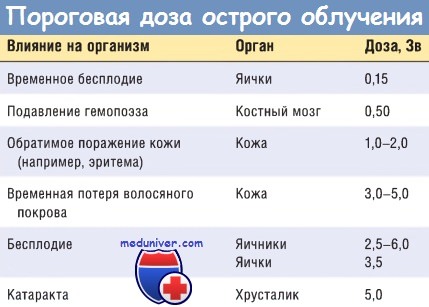
На рисунке ниже перечислены общие последствия радиационного облучения, варьирующие в зависимости от дозы излучения и вида воздействия. В таблицах ниже указаны приблизительные пороговые дозы для развития признаков острого воздействия облучения определенных органов; перечислены эффекты, вызванные воздействием различных доз облучения на весь организм.
Морфология. В клетках, выживших после поражения радиацией, происходят различные структурные изменения хромосом, включая делеции, разрывы, транслокации и фрагментации. Митотическое веретено часто становится беспорядочным, возможны полиплоидия и анеуплоидия. Нередко наблюдают отек ядра и конденсацию с группированием хроматина, иногда разрушается ядерная мембрана, может происходить апоптоз. Возможны все формы аномалий ядра. После воздействия радиации нередко появляются и существуют в течение длительного времени (годы) гигантские клетки с плеоморфными ядрами. При чрезвычайно высоких дозах радиации быстро начинается кариопикноз или лизис клетки (как показатели смерти клетки).
Кроме воздействия на ДНК и ядро радиация может вызвать множество изменений цитоплазмы, включая отек, разрушение митохондрий (дисторсию) и дегенерацию эндоплазматического ретикулума. Иногда происходят разрывы плазматической мембраны и возникают очаговые дефекты. Гистологическое сочетание клеточного плеоморфизма, образования гигантских клеток, изменений ядер и фигур митоза создает схожую картину между клетками, поврежденными радиацией, и опухолевыми клетками. Это представляет серьезную проблему для патологоанатомов, оценивающих ткани после облучения для исключения наличия в них клеток опухоли.
При световой микроскопии в облученных тканях заметны сосудистые изменения и интерстициальный фиброз. Непосредственно после облучения наблюдается только дилатация сосудов. Позже или при воздействии более высоких доз появляется множество дегенеративных изменений, включая отек клеток эндотелия и вакуолизацию или даже диссолюцию (растворение) с тотальным некрозом стенок мелких сосудов, таких как капилляры и венулы. Пораженные сосуды иногда разрываются или тромбируются.
Еще позднее в облученных сосудах происходят пролиферация клеток эндотелия и гиалинизация коллагена с утолщением медии, приводя к значительному сужению или даже облитерации просвета сосуда. К этому моменту обычно становится очевидным увеличение интерстициального коллагена в области облучения, приводящее к рубцеванию и контрактурам.
Облучение всего тела. Облучение больших участков тела даже очень маленькими дозами радиации может иметь разрушительные последствия. После облучения дозами менее 1 Зв симптомов поражения может не быть или они будут минимальными. Однако более высокие уровни радиации оказывают неблагоприятное воздействие на здоровье. Эти нарушения называют острыми лучевыми синдромами (прогрессирующее поражение системы кроветворения, ЖКТ и ЦНС при увеличении дозы облучения).
Острое воздействие на систему кроветворения и лимфатическую систему. Система кроветворения и лимфатическая система чрезвычайно восприимчивы к лучевому поражению и заслуживают специального упоминания. При высоких дозах и облучении большой площади через несколько часов после облучения может развиться тяжелая лимфопения наряду с уменьшением размеров лимфатических узлов и селезенки. Радиация непосредственно разрушает лимфоциты как в циркулирующей крови, так и в тканях (лимфатических узлах, селезенке, тимусе, кишечнике). При сублетальных дозах нормальное количество лимфоцитов восстанавливается в течение нескольких недель и месяцев за счет быстрой регенерации жизнеспособных клеток-предшественников.
Кроветворные клетки в костном мозге также весьма чувствительны к радиации, которая может вызвать дозозависимую аплазию костного мозга: высокие дозы радиации обусловливают смерть стволовых клеток и перманентную аплазию (апластическую анемию, в то время как при низких дозах радиации аплазия преходяща). Число циркулирующих гранулоцитов первоначально может увеличиться, но к концу первой недели начинает падать. В течение второй недели число гранулоцитов может уменьшиться до нуля. Если пациент выживает, восстановление нормального количества гранулоцитов происходит в течение 2-3 мес. Количество тромбоцитов также уменьшается (минимальное их число в циркулирующей крови регистрируют несколько позже, чем у гранулоцитов), и восстановление происходит позднее.
Количество эритроцитов падает через 2-3 нед, и может развиться анемия, сохраняющаяся в течение нескольких месяцев.
Фиброз. Частым осложнением лучевой терапии злокачественных опухолей является развитие фиброза в тканях, подвергнутых облучению. Фиброз может развиться через несколько недель или месяцев вследствие замещения погибших паренхиматозных клеток соединительной тканью, приводящего к образованию рубцов и спаек. Повреждение сосудов, смерть стволовых клеток ткани и выделение цитокинов и хемокинов, провоцирующих воспалительные реакции и активирующих фибробласты, — основные компоненты процесса формирования фиброза, вызванного облучением. Частыми локализациями фиброза после облучения всего тела являются легкие, после лучевой терапии рака головы и шеи — слюнные железы, после лечения рака предстательной железы — колоректальная и тазовая области.
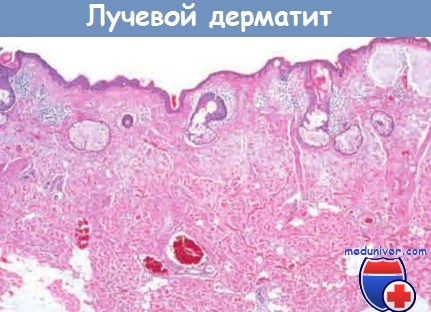
фиброз кожи и телеангиэктазии подкожных кровеносных сосудов.
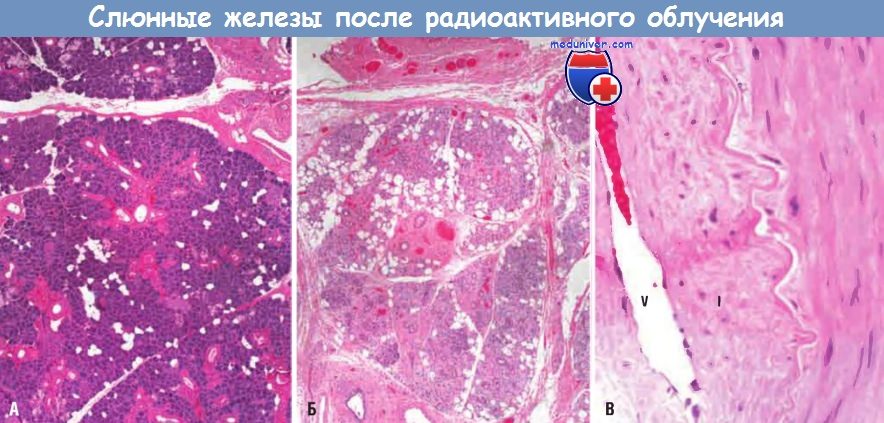
(А) Нормальная слюнная железа. (Б) Фиброз, вызванный облучением.
(В) Фиброз и сосудистые изменения, представленные фиброинтимальным утолщением и склерозом артериол.
I — утолщенная интима; V — просвет сосуда

Повреждение ДНК и канцерогенез. Ионизирующее излучение может вызывать различные типы повреждений ДНК, включая нарушение основы, одно- и двухцепочечные разрывы, формирование перекрестного сшивания между ДНК и белками. Несложные дефекты уцелевших клеток могут устраняться различными ферментами системы репарации, локализованными в клетках млекопитающих. Однако наиболее серьезные повреждения ДНК вызваны двухцепочечными разрывами. Существует два механизма устранения двухцепочечных разрывов в клетках млекопитающих: гомологичная рекомбинация и негомологичное соединение концов (наиболее распространенный). Восстановление ДНК путем негомологичного соединения концов часто приводит к мутациям, в т.ч. коротким делециям или дупликациям либо грубым хромосомным аберрациям, таким как транслокация и инверсия.
Если репликация клеток, содержащих двухцепочечные разрывы, не остановлена в точках контроля, клетки с хромосомными повреждениями сохраняются и могут инициировать канцерогенез через много лет. Недавно было обнаружено, что эти аномальные клетки также обеспечивают «эффект свидетеля», т.е. рост необлученных окружающих клеток путем продукции факторов роста и цитокинов. «Эффект свидетеля» еще называют нецелевым воздействием радиации.
Злокачественные опухоли после воздействия низких доз радиации. Любая клетка, способная к делению, после ее мутации может стать опухолевой. Таким образом, после воздействия ионизирующего излучения образование опухоли может произойти в любом органе. Установить уровень излучения, повышающий риск развития злокачественных опухолей, затруднительно, но установлено, что острое или длительное воздействие дозы более 100 мЗв приводит к серьезным последствиям, включая злокачественные опухоли.
Доказательствами этого послужили зафиксированное увеличение заболеваемости лейкемиями и опухолями различной локализации (раком щитовидной железы, молочной железы и легкого) у переживших атомные бомбежки в Хиросиме и Нагасаки, повышение заболеваемости раком щитовидной железы у оставшихся в живых после аварии на атомной электростанции в Чернобыле, у жителей Маршалловых островов, где выпали радиоактивные осадки, а также увеличение частоты вторичного рака (острой миелобластной лейкемии, миелодиспластического синдрома, лимфомы Ходжкина и солидных опухолей) у лиц, получавших лучевую терапию по поводу рака в детском возрасте. Долгосрочный риск развития злокачественных опухолей, вызванный облучением в дозе 5-100 мЗв, гораздо труднее установить, поскольку необходим анализ больших групп населения — от 50 тыс. до 5 млн человек.
Оценка риска развития злокачественных опухолей при действии низких доз ионизирующего излучения зависит отчасти от моделей оценки риска при более высоких дозах. Для рентгеновских лучей и у-лучей есть статистически значимые доказательства увеличения риска развития злокачественных опухолей при остром облучении дозой более 50 мЗв и обоснованные доказательства для доз более 5 мЗв. Для длительной экспозиции возможны приближенные значения: более 100 мЗв — статистически значимое увеличение риска, более 50 мЗв — обоснованные доказательства повышенного риска. Для сравнения: при единичной рентгенографии грудной клетки в заднепередней и боковой проекциях, а также компьютерной томографии грудной клетки легкие получают дозу 0,01, 0,15 и 10 мЗв соответственно.
Риск развития злокачественных опухолей, ассоциированных с профессиональными вредностями. Радон — продукт самопроизвольного распада урана. Канцерогенными веществами являются два побочных продукта распада радона — полоний-214 и полоний-218, испускающие а-частицы. Полоний-214 и полоний-218 откладываются в легких, и их постоянное воздействие на работников урановых шахт может инициировать развитие карциномы легких. Риски также увеличены у лиц, живущих в домах с уровнем радона, сопоставимым с уровнем в шахтах, однако данных о радоне как виновнике развития рака легкого в домашних условиях мало.
Еще один изотоп, полоний-210, привлек внимание мировой общественности в ноябре 2006 г. в связи с убийством в Англии, осуществленном с помощью полония-210. Также известны исторические факты развития остеогенной саркомы у химиков и радиологов после воздействия радия, а также у художников, наносивших краску на основе радия на циферблат часов, и пациентов, лечившихся радием от различных заболеваний в первой половине XX в.

Обратите внимание на заметно утолщенную кардию.
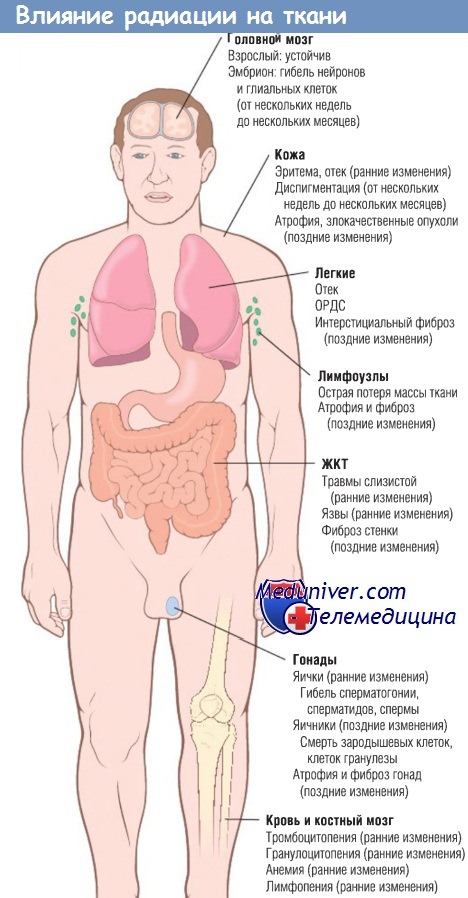
Ранние изменения отмечаются через несколько часов или недель, поздние развиваются в течение нескольких месяцев или лет.
Некоторые изменения могут возникать в период от нескольких недель до нескольких месяцев.
ЖКТ—желудочно-кишечный тракт; ОРДС — острый респираторный дистресс-синдром.
- Рекомендуем ознакомиться со следующей статьей "Причины недостаточного питания"
Оглавление темы "Патофизиология":- Патогенез и морфология термического ожога
- Патогенез и последствия гипертермии
- Патогенез и последствия гипотермии
- Механизмы развития (патогенез) электротравмы
- Патогенез поражения ионизирующей радиацией
- Причины недостаточного питания
- Патогенез, морфология маразма и квашиоркора
- Механизмы развития (патогенез) кахексии
- Механизмы развития (патогенез) анорексии и булимии
- Дефицит витамином (гиповитаминоз) и его причины

