Механизмы развития (патогенез) хронической миелоидной лейкемии
Хроническая миелоидная лейкемия отличается от других миелопролиферативных заболеваний наличием гибридного гена BCR-ABL, состоящего из гена BCR на 22-й хромосоме и гена ABL на 9-й хромосоме. BCR-ABL детерминирует синтез конститутивно активной тирозинкиназы BCR-ABL, которая при хронической миелоидной лейкемии обычно имеет размер 210 кДа. В 90% случаев BCR-ABL образуется в результате реципрокной транслокации t(9;22).
В оставшихся случаях гибридный ген BCR-ABL формируется в результате комплексных или скрытых цитогенетических перестроек, поэтому его следует определять другими методами, например с помощью флуоресцентной гибридизации in situ или полимеразной цепной реакции (ПЦР). Источником хронической миелоидной лейкемии служит плюрипотентная КСК.
а) Молекулярный патогенез. В нормальных условиях тирозинкиназы претерпевают опосредованную лигандом димеризацию и аутофосфорилирование, в результате чего образуются активированные киназы, способные фосфорилировать другие белковые субстраты.
Компонент BCR гибридного белка BCR-ABL содержит домен димеризации, который самоассоциируется, активируя компонент ABL тирозинкиназы. Последний, в свою очередь, фосфорилирует белки, индуцирующие пролиферацию и выживание клеток теми же путями, что и гемопоэтические факторы роста, включая пути RAS, JAK, STAT и АКТ. По неизвестным причинам BCR-ABL стимулирует пролиферацию преимущественно гранулоцитарных и мегакариоцитарных клеток-предшественников, а также вызывает аномальное высвобождение из костного мозга в кровь незрелых гранулоцитов.
б) Морфология. В костном мозге обнаруживается заметная гиперклеточность в результате значительного увеличения количества созревающих клеток-предшественников гранулоцитов, в первую очередь эозинофилов и базофилов. Мегакариоцитов также становится больше, обычно среди них присутствуют небольшие диспластические формы. Уровень эритроидных клеток-предшественников в норме или слегка снижен. Характерно присутствие рассеянных макрофагов с обильной складчатой сине-зеленой цитоплазмой (гистиоцитов цвета морской волны).
Типично повышенное отложение ретикулина, однако явный фиброз костного мозга на ранних стадиях встречается редко. В крови определяется лейкоцитоз, часто превышающий 100 тыс. клеток/мм3. Определяются преимущественно нейтрофилы, палочковидные формы, метамиелоциты, миелоциты, эозинофилы и базофилы. Бласты обычно составляют < 10% циркулирующих клеток.
Количество тромбоцитов повышено, иногда существенно. Селезенка часто сильно увеличена в результате обширного экстрамедуллярного гемопоэза, нередко в ней есть зоны инфарктов различной давности. Экстрамедуллярный гемопоэз может вызвать умеренные гепатомегалию и лимфаденопатию.
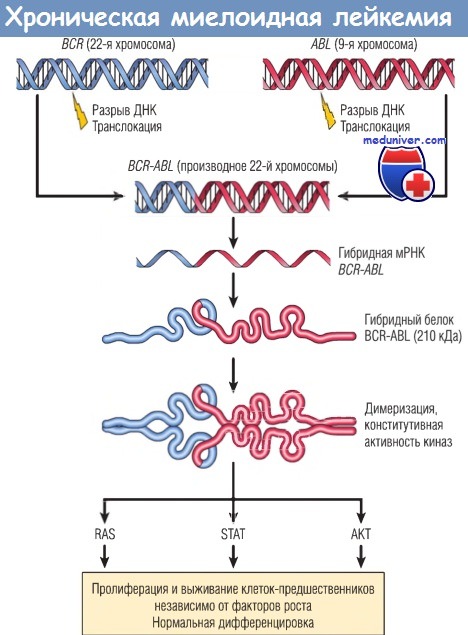
При разрыве ДНК и соединении генов BCR и ABL создается гибридный ген, кодирующий конститутивно активную тирозинкиназу BCR-ABL.
Эта киназа активирует множественные пути, опосредующие пролиферацию и выживаемость клеток-предшественников костного мозга независимо от факторов роста.
Поскольку BCR-ABL не препятствует дифференцировке, конечным результатом является увеличение количества зрелых клеток в периферической крови, особенно гранулоцитов и тромбоцитов.
ДНК — дезоксирибонуклеиновая кислота; мРНК — матричная рибонуклеиновая кислота.
в) Клинические признаки. Хроническая миелоидная лейкемия — это заболевание главным образом взрослых, однако также наблюдается у детей и подростков. Пик заболеваемости приходится на возраст 40-50 лет. В США ежегодно регистрируют 4500 новых случаев заболевания.
Заболевание манифестирует без явных симптомов. Анемия (слабая или умеренная) и повышенный метаболизм вследствие ускоренного клеточного обновления приводят к утомляемости, слабости, снижению массы тела и анорексии. Иногда первым симптомом является неприятное ощущение в животе вследствие спленомегалии, или внезапно появляется боль в левом верхнем квадранте живота в результате инфаркта селезенки. Хроническую миелоидную лейкемию надежнее всего отличать от других миелопролиферативных заболеваний с помощью хромосомного анализа (определения гибридного гена BCR-ABL) или ПЦР.
Хроническая миелоидная лейкемия прогрессирует медленно. В отсутствие лечения медиана выживаемости составляет 3 года. Через различные периоды времени (в среднем 3 года) в 50% случаев начинается фаза ускорения, характеризующаяся нарастанием анемии и тромбоцитопении, иногда сопровождающихся повышением количества базофилов. Часто обнаруживают дополнительные клональные цитогенетические нарушения: трисомию по 8-й хромосоме, изохромосому 17q или дупликацию филадельфийской хромосомы. Через 6-12 мес фаза ускорения завершается клинической картиной, напоминающей острую лейкемию (властный криз).
В других случаях фаза ускорения не наступает, и бластный криз происходит внезапно. В 70% случаев криза бласты имеют миелоидное происхождение (миелоидный бластный криз), тогда как у большей части оставшихся 30% обнаруживаются бласты пре-В-клеточного происхождения (лимфоидный бластный криз). Это обстоятельство указывает на то, что источником хронической миелоидной лейкемии является плюрипотентная стволовая клетка, обладающая как миелоидным, так и лимфоидным потенциалом. Недавно было обнаружено, что в 85% случаев хроническая миелоидная лейкемия ассоциируется с мутациями, нарушающими активность Ikaros (фактора транскрипции, регулирующего дифференцировку гемопоэтических клеток-предшественников).
Такие же мутации Ikaros обнаружены при BCR-ABL-положительной ОЛЛ, т.е. эти два варианта агрессивной лейкемии имеют сходную патогенетическую основу.
Выяснение молекулярного патогенеза хронической миелоидной лейкемии привело к использованию лекарственных средств, направленно действующих на BCR-ABL. Лечение с помощью ингибиторов BCR-ABL у 90% пациентов приводило к длительной гематологической ремиссии и сопровождалось лишь незначительными побочными эффектами. Иматиниб заметно снижает количество BCR-ABL-положительных клеток в костном мозге и других тканях организма, однако не влияет на стволовую клетку хронической миелоидной лейкемии — примитивную клетку, напоминающую нормальную КСК.
В связи с этим неясно, обладает ли иматиниб прямым терапевтическим эффектом, однако применение этого препарата нормализует количество клеток в крови и существенно снижает риск наступления фазы ускорения и бластного криза, представляющего наибольшую опасность для пациента. Предполагается, что благодаря снижению пролиферативной активности BCR-ABL-положительных клеток-предшественников иматиниб снижает частоту мутаций в этих клетках, приводящих к прогрессированию заболевания. Трансплантация аллогенного костного мозга сравнительно молодым пациентам, проводимая в фазе стабильности хронической миелоидной лейкемии, в 75% случаев дает хороший эффект и остается терапией выбора.
Результат гораздо менее благоприятен, если уже началась фаза ускорения или произошел бластный криз. В этой ситуации трансплантация оказывается неэффективной, и заболевание быстро становится резистентным к ингибиторам BCR-ABL, как при BCR-ABL-положительной ОЛЛ.
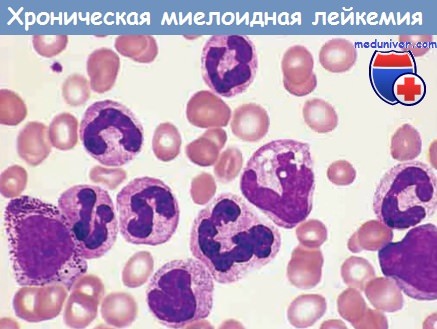
В мазке периферической крови присутствует много зрелых нейтрофилов,
несколько метамиелоцитов и миелоцит.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) истинной полицитемии"
Оглавление темы "Патогенез болезней крови":- Механизмы развития (патогенез) миелодиспластического синдрома
- Механизмы развития (патогенез) миелопролиферативного заболевания
- Механизмы развития (патогенез) хронической миелоидной лейкемии
- Механизмы развития (патогенез) истинной полицитемии
- Механизмы развития (патогенез) эссенциального тромбоцитоза
- Механизмы развития (патогенез) первичного миелофиброза
- Механизмы развития (патогенез) гистиоцитоза клеток Лангерганса
- Строение и физиология селезенки
- Классификация причин спленомегалии

