Механизмы развития (патогенез) первичного миелофиброза
Отличительный признак первичного миелофиброза — облитерирующий фиброз костного мозга. Замещение костного мозга фиброзной тканью подавляет гемопоэз в нем, приводя к цитопении и обширному неопластическому экстрамедуллярному гемопоэзу. Гистологическая картина идентична картине фазы истощения, возникающей на поздних стадиях других миелопролиферативных заболеваний.
а) Молекулярный патогенез. Активирующие мутации JAK2 присутствуют в 50-60% случаев, а дополняющие их активирующие мутации MPL — в 1-5% случаев. Главным патологическим признаком является обильное отложение коллагена в костном мозге, продуцируемого неопухолевыми фибробластами.
Фиброз вытесняет гемопоэтические элементы, включая стволовые клетки, из костного мозга и в конечном счете приводит к недостаточности костного мозга. Возможно, причиной служит неадекватное высвобождение фиброгенных факторов из неопластических мегакариоцитов. Эти клетки продуцируют два фактора: фактор роста тромбоцитов и TGF-b. Оба эти фактора являются митогенами для фибробластов.
Кроме того, TGF-b стимулирует отложение коллагена и вызывает ангиогенез. При миелофиброзе наблюдаются оба процесса. По мере развития фиброза костного мозга КСК накапливаются во вторичных гемопоэтических органах — селезенке, печени и лимфоузлах, приводя к развитию экстрамедуллярного гемопоэза. По непонятным причинам продукция клеток крови при экстрамедуллярном гемопоэзе нарушена. Этот фактор и сопутствующее подавление функции костного мозга приводят к цитопении, степень которой варьирует от умеренной до значительной.
Неясно, действительно ли первичный миелофиброз (особенно ассоциируемый с мутациями JAK2 или MPL) отличается от истинной полицитемии и эссенциального тромбоцитоза или просто отражает быстрое прогрессирование этих миелопролиферативных заболеваний, приводящее к фазе истощения.
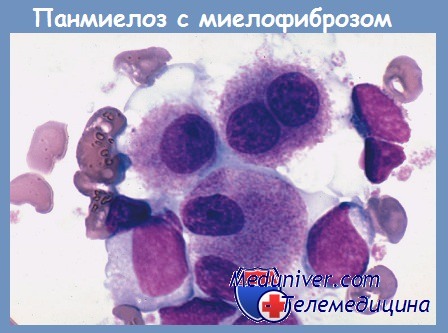
б) Морфология. На ранних стадиях клеточность костного мозга часто повышена вследствие увеличения количества созревающих клеток всех линий — признак, напоминающий истинную полицитемию. Морфологически эритроидные и гранулоцитарные клетки-предшественники выглядят нормальными, однако мегакариоциты крупные, диспластические и образуют аномальные скопления. На этой стадии фиброз минимален и в крови можно наблюдать лейкоцитоз и тромбоцитоз. По мере развития заболевания клеточность костного мозга снижается и он становится диффузно-фиброзным.
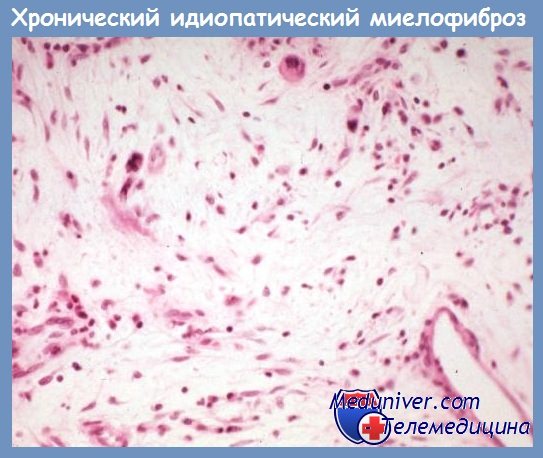
Видны скопления атипичных мегакариоцитов, гемопоэтические элементы часто обнаруживаются внутри расширенных синусоидов, что служит проявлением тяжелого нарушения структуры костного мозга, вызванного фиброзом. На очень поздней стадии пространство, занимаемое костным мозгом, может превратиться в кость. Такое изменение называют остеосклерозом. Эти признаки идентичны наблюдаемым в фазе истощения при других миелопролиферативных заболеваниях.
Фиброзная облитерация пространства костного мозга приводит к распространенному экстрамедуллярному гемопоэзу, главным образом в селезенке, которая обычно существенно увеличивается (иногда до 4000 г). Макроскопически такая селезенка плотная, имеет равномерно красный или серый цвет. Как и при хронической миелоидной лейкемии, часто наблюдаются зоны субкапсулярного инфаркта. Первоначально экстрамедуллярный гемопоэз ограничен синусоидами, однако позднее распространяется в селезоночные тяжи.
Из-за синусоидальных очагов экстрамедуллярного гемопоэза печень может быть умеренно увеличенной. Экстрамедуллярный гемопоэз может происходить также в лимфоузлах, однако значительная лимфаденопатия наблюдается редко.
Фиброз костного мозга отражается в особенностях картины крови. Нарушение приводит к преждевременному высвобождению эритроидных ядросодержащих и ранних гранулоцитарных клеток-предшественников (лейкоэритробластозу). Незрелые клетки поступают в кровоток также из участков экстрамедуллярного гемопоэза. Эритроциты, имеющие форму слезы (дакриоциты), вероятно, представляют собой клетки, повреждаемые в ходе образования в фиброзированном костном мозге. Лейкоэритробластоз и дакриоциты характерны для первичного миелофиброза, но наблюдаются и при многих инфильтративных заболеваниях костного мозга, включая гранулематозные заболевания и метастазирующие опухоли. Другие частые, но неспецифичные находки — аномально крупные тромбоциты и базофилия.
в) Клинические признаки. Первичный миелофиброз встречается реже, чем истинная полицитемия и эссенциальный тромбоцитоз, и обычно возникает у лиц старше 60 лет. За исключением случаев, когда данному заболеванию предшествует другое миелопролиферативное заболевание, первичный миелофиброз проявляется симптомами прогрессирующей анемии и спленомегалии с неприятным чувством распирания в левом верхнем квадранте живота. Неспецифические симптомы (повышенная утомляемость, снижение массы тела и ночное потоотделение) появляются в результате усиления метаболизма, связанного с увеличением количества кроветворных клеток. Клиническую картину могут осложнить гиперурикемия и вторичная подагра.
Типичной находкой при лабораторном исследовании является нормохромная нормоцитарная анемия (от умеренной до значительной), сопровождающаяся лейкоэритробластозом. Количество лейкоцитов обычно в норме или сниженное, однако на ранних стадиях может быть заметно повышенным (80-100 тыс. клеток/мм3). Количество тромбоцитов к моменту постановки диагноза, как правило, нормальное или повышенное, но по мере прогрессирования заболевания развивается тромбоцитопения. Такие изменения в крови неспецифичны. Диагностике помогает исследование биоптатов костного мозга.
Первичный миелофиброз вылечить труднее, чем истинную полицитемию или эссенциальный тромбоцитоз. Течение заболевания вариабельно, медиана выживаемости составляет 3-5 лет. Угрозу для жизни создают интеркуррентные инфекции, тромботические эпизоды, кровотечения, связанные с аномалиями тромбоцитов, и трансформация в ОМЛ, происходящая в 5-20% случаев. При распространенном первичном миелофиброзе ОМЛ иногда возникает в участках экстрамедуллярного гемопоэза, включая лимфоузлы и мягкие ткани. В некоторых случаях молодым пациентам проводят трансплантацию костного мозга. Применение ингибиторов киназ является перспективным методом таргетной терапии.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) гистиоцитоза клеток Лангерганса"
Оглавление темы "Патогенез болезней крови":- Механизмы развития (патогенез) миелодиспластического синдрома
- Механизмы развития (патогенез) миелопролиферативного заболевания
- Механизмы развития (патогенез) хронической миелоидной лейкемии
- Механизмы развития (патогенез) истинной полицитемии
- Механизмы развития (патогенез) эссенциального тромбоцитоза
- Механизмы развития (патогенез) первичного миелофиброза
- Механизмы развития (патогенез) гистиоцитоза клеток Лангерганса
- Строение и физиология селезенки
- Классификация причин спленомегалии

