Механизм действия аминохолиновых (антималярийных) препаратов
Аминохолиновые препараты - краткий обзор:
- Аминохинолиновые препараты применяются в клинической медицине более ста лет, прежде всего как антималярийные средства.
- Механизмы действия разнообразны, в том числе нарушение лизосомальной ацидификации антиген-представляющими клетками, подавление естественных киллеров и активация Т-клеток, а также угнетение липидных медиаторов воспаления.
- Обладают аффинностью к меланиновому пигменту, абсорбируют ультрафиолетовый свет и оказывают фотозащитное действие от повреждения кожи при воздействии ультрафиолета.
- Аминохинолиновые препараты, которые применяют для лечения дерматологических состояний, включают гидроксихлорохин, хлорохин и хинакрин.
- Из аминохинолинов для лечения заболеваний кожи чаще всего используется гидроксихлорохин, его применение при хронической кожной красной волчанке достаточно хорошо изучено.
- Другие заболевания, реагирующие на аминохинолины, включают позднюю кожную порфирию, полиморфный фотодерматит, кожный саркоидоз, дерматомиозит и другие состояния.
- Лабораторный контроль является обязательным во время аминохинолиновой терапии и осуществляется для выявления отклонений в показателях крови (гемолиз и медикаментозные цитопении), поражений печени и офтальмологических изменений (ретинопатии).
- Дети особенно подвержены токсическому воздействию аминохинолинов и поэтому им назначаются более низкие дозы, чем взрослым.
- Возможны лекарственные взаимодействия, курение сигарет снижает эффективность аминохинолиновых препаратов путем индуцирования ферментов цитохрома Р450.
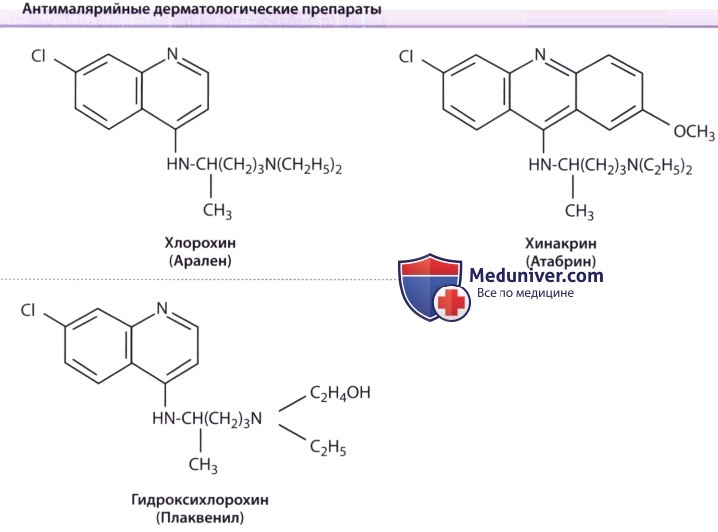
Антималярийные препараты применяются для лечения кожных заболеваний уже в течение столетия. Самыми изученными являются три препарата: хлорохин (ХРХ), гидроксихлорохин (ГХХ) и хинакрин (ХК). 4-Аминохи-нолины относятся к семейству производных хинина, встречающегося в природе алкалоида, который добывали из коры хинного дерева, произрастающего в Южной Америке.1 ХК, который классифицируется как акридин, также применяется в дерматологической терапии. Интересно отметить, что применение этих лекарств для лечения и профилактики малярии уменьшается вследствие возросшей резистентности.
а) Механизм действия. Точный механизм, посредством которого антималярийные препараты осуществляют свое действие, все еще остается неизвестным. Однако для каждого из веществ были определены несколько отдельных механизмов. При лечении малярии аминохинолины концентрируются в пищеварительной вакуоли Plasmodium и препятствуют полимеризации токсического гема, который высвобождается в ходе протеолиза гемоглобина. Механизмы, посредством которых эти вещества влияют на кожные болезни, разнообразны и включают, помимо прочего, воздействие на презентацию антигенов, цитокины, толл-подобные рецепторы и простагландины.
ХРХ и ГХХ являются слабыми двухосновными основаниями, которые присоединяют протоны, захватываются и аккумулируются внутри кислых везикул, таких как лизосомы, чем объясняется их воздействие на Plasmodium. ГХХ индуцирует признаки пермеабилизации лизосомальной и митохондриальной мембран. При повышении pH внутри лизосом от 4-6, протеазы инактивируются и последующий протеолиз блокируется. Как следствие, могут нарушаться процессинг и презентация антигенов дендритными клетками ввиду неспособности фагоцитировать эти чужеродные антигены в лизосомном компартменте. Вдобавок было показано, что ХРХ нарушает «загрузку» антигенных пептидов в молекулы МНС класса II и последующую презентацию Т-клетке. Угнетение кальциевой сигнализации в Т-клетке может быть дополнительным механизмом. В отличие от этого, было недавно показано, что ХРХ усиливает ответ Т-клеток фенотипа CD8+. ХК ингибирует активность Na-K-аденозинтрифосфатазы и стабилизирует клеточные мембраны. Он также концентрируется в лизосомах. Эти воздействия наиболее ощутимы в макрофагах и фагоцитирующих клетках, в которых нарушен фагоцитоз и хемотаксис. Кроме того, оказывается воздействие также на клеточные ферменты и рецепторы, функция или активация которых зависит от лизосом, что изменяет реактивность клеток на митогенные стимулы.
Антималярийные препараты уменьшают высвобождение Т-клетками интерлейкина-1 (ИЛ-1), ИЛ-6, фактора некроза опухоли-а и интерферона-γ. ИЛ-1, ИЛ-6, фактор некроза опухоли-а играют определенную роль в производстве печенью реактантов острой фазы. Низкие концентрации ХРХ и ХК угнетают про-ИЛ-6-стимулирующий эффект содержащих мотив «цитозин-фосфат-гуанин» олигодезоксинуклеоти-дов на мононуклеарные клетки периферической крови человека. Недавно было обнаружено, что ХРХ повышает экспрессию В7-2 (CD86, костимулирущего белка) и молекулы межклеточной адгезии 1 (CD54, молекула адгезии), увеличивая таким образом количество клеток, производящих ИЛ-10. XX участвует также в угнетении активности естественных клеток-киллеров, понижении производства ИЛ-2 из активированных лимфоцитов и в изменении комплексов антиген-антитело. ХК также подавляет естественные клетки-киллеры и блокирует первичный пролиферативный ответ цитотоксических Т-клеток на аллогенные, не-Т-клеточные антигены. И, наконец, антималярийные препараты влияют на механизм действия арахидоновой кислоты. ХРХ ингибирует фосфолипазы А2 и С. ХК также ингибирует производство фосфолипазы А, и увеличивает высвобождение окиси азота. Таким образом, понижаются все уровни: простагландинов, лейкотриенов, брадикининов и гистамина. ХК является антагонистом образования супероксидных анионов.
Недавно был выявлен новый механизм действия антималярийных веществ, связанный с блокировкой рецептора TLR9, представителя семейства толл-подобных рецепторов. Рецепторы семейства TLR относятся к внутриплазматическим рецепторам, которые, активируя систему врожденного иммунитета в ответ на микробные пептиды, индуцируют значительный воспалительный ответ. Дальнейшие исследования обнаружили вдобавок важность врожденного иммунного ответа для патогенеза системной красной волчанки (СКВ). После этого такие TLR, известные как класс «паттерн-распознающих» рецепторов (PRRs), стали предметом интенсивного исследования для выяснения их роли в патогенезе СКВ. Недавно было показано, что иммунные комплексы хозяина, содержащие ДНК или РНК, играют важную роль в активации эндогенных TLR (особенно TLR-9 и TLR-7), что приводит в итоге к активации врожденной иммунной системы, в которой решающая роль принадлежит интерферону альфа. Кроме того, экспрессия TLR-9 тесно связана с активностью СКВ. Эти TLR, взаимодействующие со специфическими нуклеиновыми кислотами, связываются с их лигандами в лизосоме, где кислая среда способствует такому связыванию. Поскольку антималярийные агенты целенаправленно воздействуют на микросомы, нарушая созревание эндосом и изменяя pH, они блокируют взаимодействие TLR (TLR-3,—7 и -9) с лигандами нуклеиновых кислот. Исследования in vitro показали, что наномолярные концентрации хлорохина являются особенно мощными ингибиторами производства ИЛ-6 моноцитами, а этот эффект, как сейчас известно, прямо опосредуется ингибицией рецептора TLR-9. Основными целями этих взаимодействий являются антиген-презентирующие клетки, чем объясняется клинически замедленный ответ, по мере того, как они инициируют и запускают последующие иммунные реакции.
4-Аминохинолины обладают аффинностью к меланиновому пигменту. В эпидермисе (а также сетчатке) они связываются в высоких концентрациях. В коже ХРХ поглощает ультрафиолетовый (УФ) свет в зависимости от концентрации. После приема хлорохина внутрь в течение 3 месяцев у пациентов с волчанкой наблюдается увеличение минимальных эритемных доз (МЭД) УФБ, что теоретически является результатом противовоспалительного и /или фотозащитного механизма действия лекарства. Местный ХРХ при нанесении до УФ-облучения защищает от индуцируемой УФБ и УФА эритемы. ХК также ингибирует фотодинамические действия. Предполагается, что благоприятный эффект ГХХ и ХРХ при различных фотодерматозах является результатом способности этих лекарств усиливать ранний защитный ответ на УФ.
ХРХ и ХК связывают клеточную ДНК путем интеркаляции между базовыми парами и таким образом стабилизируют ДНК. ГХХ улучшает липидный профиль, вызывая, в частности, 15%—20% понижение сывороточный уровней общего холестерина, триглицеридов и ЛПНП. ХРХ и ГХХ, оба улучшают профили глюкозы и ингибируют агрегацию тромбоцитов. Высокие дозы ХРХ могут оказывать антиоксидантное действие. Благодаря стабилизации мембраны, антималярийные препараты могут оказывать местный анестезирующий эффект. In vitro ГХХ индуцирует апоптоз в В- клетках хронической лимфоцитарной лейкемии. ХРХ, ГКХ и ХК — все препятствуют репликации и функциям вируса иммунодефицита человека типа 1, коронавируса SARS (или ТОРС, тяжелого острого респираторного синдрома) и вируса гриппа, возможно в результате нарушения гликозилирования белка.

б) Фармакокинетика антималярийных препаратов. Молекулярные структуры ХРХ, ГХХ и ХК являются близкородственными. Молекулярные структуры ХРХ, ГХХ и ХК являются близкородственными. ХРХ и ГХХ относятся к 4-аминохинолинам, при этом ГХХ отличается от ХРХ по наличию гидроксильной группы на конце боковой цепочки. Имеющий добавочное бензокольцо ХК классифицируется как акридин. Фармакокинетика и фармакология этих веществ похожи, но важно отметить, что отсутствует перекрестная реактивность между аминохинолонами и ХК. Все они имеют горький вкус, растворяются в воде, легко всасывается в желудочно-кишечном тракте со сравнительно хорошей биодоступностью и достигают пиковых концентраций в течение 8-12 часов. У ХРХ и ГХХ больший объем распределения (более 100 л) и более длительный период полураспада. Объем распределения у ХК может быть даже большим, чем у ХРХ и ГХХ. ХК широко связывается с протеинами плазмы, в то время как ХРХ и ГХХ связываются с ними лишь частично (60%). Период полураспада у ХК существенно меньше, чем у других препаратов. ХРХ метаболизируется (деалкилируется) в печени ферментами Р450 в дезэтилхлорохин и бисдезэтилхлорохин. Метаболический путь ХК менее известен. ХРХ и его метаболиты накапливаются в сравнительно высоких концентрациях в печени, селезенке, легких, надпочечниках и почках, причем максимальная концентрация обнаруживается в содержащих меланин клетках сетчатки и кожи.
Примерно 50% ХРХ выводится почками в неизмененном состоянии. ГХХ также метаболизируется в печени (N-деэтилирование) в три основных метаболита: (1) дезэтилгидроксихлорохин, (2) дезэтилхлорохин и (3) бисдезэтилхлорохин. Родительское вещество и метаболиты захватываются лизосомами и накапливаются в богатых лизосомами тканях. Почечный клиренс составляет 15-25% общего клиренса. Выделение ХРХ, ГХХ и ХК почками можно усилить путем ацидификации мочи. ХК выделяется с мочой, желчью, потом и слюной. Почечная экскреция составляет только около 11% клиренса. Максимальные концентрации ХК в тканях обнаружены в печени и селезенке. Эквивалентные дозы данных препаратов составляют 200 мг РХ, 400 мг ГХХ и 100 мг ХК. Курение может изменить фармакокинетику антималярийных препаратов, поскольку документально подтверждены клинические данные об уменьшении эффективности этих медикаментов у курильщиков. Понижение абсорбции, увеличение клиренса плазмы или индукция системы цитохрома Р450 могут быть теми механизмами, через которые курение воздействует на метаболизм этих веществ.
Недавнее исследование выявило связь между концентрациями ГХХ в цельной крови и активностью заболевания у пациентов с СКВ. Показатели уровня ГХХ в крови у 143 пациентов, которые получали препарат в дозе 400 мг/день в течение 6 месяцев, отличались высокой вариабельностью концентраций в крови (возможно по причине комплаентности). Средняя концентрация препарата в крови у пациентов с неактивным заболеванием составляла 1079 нг/мл, а средний уровень концентрации у пациентов с активным заболеванием равнялся 694 нг/мл. Кроме того, авторы установили, что низкий уровень концентрации ГХХ в крови ассоциировался с обострениями заболевания в период наблюдения. Был сделан вывод о том, что концентрация ГХХ в крови должна поддерживаться на уровне выше 1000 нг/мл, что указывает на необходимость регулярного анализа и индивидуальных схем дозировки для поддержания этого уровня.
Обычные дозы, применяющиеся в дерматологии, составляют 250-500 мг/день для ХРХ, 200-400 мг/день для ГХХ и 100-200 мг/день для ХК. Проявления эффективности обычно наблюдаются через 1-3 месяца, но для достижения максимальной клинической эффективности может потребоваться 3-6 месяцев. После чего дозу можно постепенно понижать до минимально эффективного уровня. Как уже указывалось, перекрестная реактивность между ХК и ХРХ, а также ГХХ отсутствует. Поэтому применение ХК в комбинации с ГХХ и/или ХРХ считается безопасным. В случае торпидных кожных заболеваний, добавление ХК к ГХХ или ХРХ считается благоприятным, и ответ может наблюдаться через 6-8 недель после добавления ХК. Если ХК добавляют к ХРХ, может потребоваться снижение дозы ХРХ для уменьшения потенциала токсичности. Трихин, комбинация ХРХ (65 мг), ГХХ (50 мг) и ХК (25 мг) применялись в начале 1970-х годов. Тем не менее, одновременное применение ХРХ и ГХХ повышает риск ретинопатии (см. раздел «Осложнения»). Таким образом, применение этой комбинации должно быть ограничено только тяжелыми случаями. ХК в настоящее время на рынке отсутствует, его производство прекратили в 1992 г. Порошок ХК (для ветеринарии, производства Sigma) может быть помещен в капсулы. Такие капсулы в ходе дополнительного процесса очищения изготавливает фирма Panorama Pharmacy в Калифорнии.
- Рекомендуем далее ознакомиться со статьей "Показания и дозы аминохолиновых (антималярийных) препаратов при лечении кожных болезней"
Редактор: Искандер Милевски. Дата публикации: 27.8.2019

