Геномная трансформация как причина развития опухоли
Хотя люди, образно говоря, окружены экологическими агентами, являющимися мутагенами (например, химикатами, радиацией, солнечным светом), злокачественные опухоли относительно редко развиваются после их воздействия. Такое положение дел — результат способности нормальных клеток устаранять повреждения ДНК, смерти клеток в случаях невозможности восстановления ДНК и действия других механизмов, например онкоген-зависимого старения и иммунного надзора.
Значимость восстановления ДНК в поддержании целостности генома видна на примере нескольких наследственных заболеваний, при которых гены, кодирующие белки, осуществляющие восстановление ДНК, являются дефектными. Лица с наследственными дефектами белков восстановления ДНК имеют повышенный риск развития злокачественных опухолей. Более того, дефекты белков восстановления ДНК выявлены и в спорадически возникающих злокачественных неоплазиях человека.
Гены восстановления ДНК не относятся к онкогенам, но нарушение их функционирования приводит к накоплению мутаций в других генах в ходе деления клеток. Как правило, геномная нестабильность является результатом утраты обеих копий гена. Однако результаты недавнего исследования позволяют сделать предположение, что по крайней мере одна подгруппа таких генов может способствовать развитию злокачественных опухолей в варианте гаплоидной недостаточности.
На образование различных видов злокачественных опухолей влияют дефекты трех типов восстановления ДНК — с нарушением комплементарности, с вырезанием нуклеотидов и с рекомбинацией нуклеотидов.
а) Синдром наследственного неполипозного рака толстой кишки. Синдром HNPCC характеризуется семейными карциномами толстой кишки, развивающимися преимущественно в слепой кишке и проксимальном отделе толстой кишки, и является следствием дефектов генов, вовлеченных в восстановление ДНК с ошибочным спариванием оснований.
Когда цепочка ДНК восстанавливается, эти гены работают как «корректоры», контролируя комплементарность нуклеотидов. Например, при ошибочном спаривании G с Т вместо нормального А с Т гены, контролирующие комплементарность нуклеотидов при восстановлении, исправляют этот дефект. Без таких «корректоров» ошибки постепенно накапливаются в нескольких генах, включая протоонкогены и гены-супрессоры злокачественных опухолей.
Одним из диагностических маркеров состояния ошибочного спаривания основания является микросателлитная нестабильность.
Микросателлиты представляют собой ряд тандемных повторений одного из шести нуклеотидов, располагающихся в разных участках генома. В норме микросателлиты имеют постоянную длину. Однако в опухолевых клетках больного синдромом HNPCC длина микросателлитов изменяется — они укорачиваются или удлиняются, в результате возникают новые аллели, не встречающиеся в нормальных клетках того же пациента.
Установлено, что в основе развития синдрома HNPCC лежат мутации по крайней мере четырех генов, контролирующих комплементарность нуклеотидов при восстановлении ДНК. При этом выявляются мутации в зародышевых клетках: в генах MSH2 (2р16) и MLH1 (3р21), в каждом 30% случаев. В оставшихся случаях обнаруживаются мутации в других генах восстановления ДНК с ошибочным спариванием оснований.
Каждый заболевший индивид наследует одну дефектную копию одного из нескольких генов, контролирующих комплементарность нуклеотидов при восстановлении ДНК, а впоследствии приобретает второй дефектный ген в клетках эпителия толстой кишки.
Таким образом, по способу наследования гены, контролирующие комплементарность нуклеотидов при восстановлении ДНК, ведут себя как гены-супрессоры злокачественных опухолей, но в отличие от генов-супрессоров и онкогенов влияют на рост клетки только опосредованно, способствуя мутации других генов во время нормального клеточного деления. Распространенность синдрома HNPCC составляет только 2-4% всех опухолевых образований толстой кишки, но микросателлитная нестабильность может быть обнаружена в 15% случаев спорадического рака.
Мутации в генах, регулирующих рост опухоли, у пациентов с синдромом HNPCC пока еще полностью не охарактеризованы, но известно, что к ним причисляют рецептор TGF-b типа II, b-катенин, ВАХ и другие онкогены и гены-супрессоры.
б) Пигментная ксеродерма. Пациенты с другим наследственным заболеванием — пигментной ксеродермой — имеют повышенный риск развития новообразований на коже при ее экспозиции УФ-лучами, входящими в состав солнечного света. В основе данной патологии лежит нарушение процесса восстановления ДНК. УФ-лучи вызывают перекрестное сшивание пиримидиновых оснований, препятствуя нормальной репликации ДНК. Такие повреждения ДНК устраняются путем вырезания дефектного нуклеотида особыми ферментами системы восстановления ДНК.
В процесс вырезания дефектных нуклеотидов вовлечены несколько белков, наследуемая потеря любого из них может дать начало развитию пигментной ксеродермы.
в) Болезни с нарушениями процесса восстановления ДНК вследствие гомологичной рекомбинации. Группа аутосомно-рецессивных заболеваний, включающих синдром Блума, атаксию-телеангиэктазию и анемию Фанкони, характеризуется гиперчувствительностью к таким повреждающим ДНК агентам, как ионизирующая радиация (синдром Блума и атаксия-телеангиэктазия), или агентам, вызывающим перекрестное сшивание ДНК, например азотистому иприту (анемия Фанкони).
Фенотип этих заболеваний сложен. Он включает помимо предрасположенности к злокачественным опухолям неврологические проявления (атаксия-телеангиэктазия), анемии (анемия Фанкони) и врожденные уродства (синдром Блума). Как полагают, ген ATM, мутантный при атаксии-телеангиэктазии, важен для распознавания и ответа на повреждение ДНК, вызванное ионизирующей радиацией. Пациенты с синдромом Блума отличаются предрасположенностью к развитию широкого спектра опухолей. Дефектный ген располагается на 15-й хромосоме и регулирует восстановление ДНК путем гомологичной рекомбинации. При анемии Фанкони описан комплекс из 13 генов, мутация в любом из них приводит к развитию заболевания.
Интересно, что мутации BRCA2, характерные для семейного рака молочной железы, выявляются и в субпопуляции пациентов с анемией Фанкони.
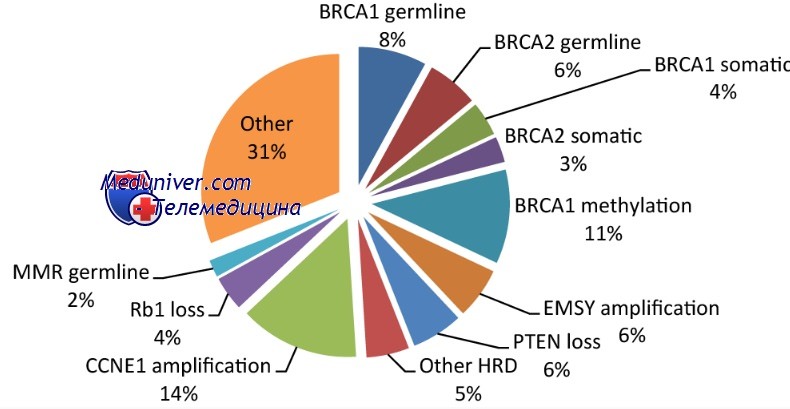
Свидетельства о роли генов восстановления ДНК в происхождении злокачественных опухолей получены также при исследовании наследственного рака молочной железы. Мутации в двух генах, BRCA1 (хромосома 17q21) и BRCA2 (хромосома 13q12—13), выявляются в 25% случаев семейного рака молочной железы. Помимо рака молочной железы у женщин с мутациями BRCA1 есть существенно более высокий риск развития карцином яичников, а у мужчин — рака предстательной железы. Аналогично мутации гена BRCA2 увеличивают риск рака молочной железы у женщин и мужчин, рака яичника, предстательной железы, поджелудочной железы, желчных протоков, желудка, а также меланомы.
Функции этих генов не установлены полностью, но известно, что клетки с отсутствием этих генов имеют хромосомные разрывы и выраженную анеуплоидию. Как полагают, оба гена функционируют, по крайней мере частично, в гомологичном рекомбинационном восстановлении ДНК.
Белки при анемии Фанкони и белки BRCA участвуют в образовании сети «ответ на повреждение ДНК», в функции которой входят распознавание и восстановление внутрицепочечных и межцепочечных связей ДНК, индуцированных сшивающими агентами. Неудачные попытки распознавания таких связей до разделения двух цепей ДНК будут приводить к разрывам хромосом и обнажению их концов. Образование таких концов, а также коротких теломер активирует запасной путь негомологичного присоединения концов хромосом, формирование дицентрических хромосом, цикла разрушения мостовидных связей и массивной анеуплоидии.
Подобно другим генам-супрессорам злокачественных опухолей, чтобы появилась злокачественная опухоль, должны быть инактивированы обе копии BRCA1 и BRCA2. Хотя связь BRCA1 и BRCA2 с семейным раком молочной железы установлена, но в спорадических случаях рака молочной железы эти гены редко инактивируются. В этом отношении BRCA1 и BRCA2 отличаются от других генов-супрессоров злокачественных опухолей, например АРС и р53, которые инактивированы как в семейных, так и в спорадических новообразованиях.
- Рекомендуем ознакомиться со следующей статьей "Влияние стромы на развитие опухоли"
Оглавление темы "Патогенез опухоли":- Молекулярная генетика метастазирования опухоли
- Геномная трансформация как причина развития опухоли
- Влияние стромы на развитие опухоли
- Эффект Варбурга в метаболизме опухоли
- Хромосомные изменения при опухоли
- Амплификация генов при опухоли
- Эпигенетические изменения как причина опухоли
- МикроРНК как причина злокачественной опухоли
- Молекулярные механизмы многоступенчатого канцерогенеза
- Механизмы и фазы химического канцерогенеза

