Результаты гибридизации цитопрепаратов. Специфичность гибридизации цитопрепаратов
Возможность интерпретации результатов гибридизации на цитологических препаратах зависит не только от чувствительности системы детекции и специфичности зонда, но и от установления локализации сигнала.
Недостатком двойных систем детекции является то, что при контрастировании всегда происходит маскирование гибридизационного сигнала. Ядерные и цитоплазматические мембраны можно локализовать с помощью фазовоконтрастного микроскопа, но это существенно усложняет анализ. Можно использовать систему детекции одного зонда, описанную в протоколе; в этом случае контрастирование не влияет на гибридизационный сигнал. Преимущество этого способа состоит в том, что существует прямая корреляция между наличием определенных нуклеотид-ных последовательностей и морфологическими структурами.
Что касается обнаружения HPV в обычных мазках шейки матки, то гибридизационный сигнал может обнаруживаться в нормальных, койлоцитных и безъядерных клетках.
Поскольку для гибридизации используется только смесь зондов, точное типирование в этом случае оказывается невозможным.
Чувствительность системы детекции с одним зондом, описанной в протоколе, составляет менее 10 копий ДНК HPV, т. е. по меньшей мере 80 т.н. интегрированной ДНК-мишени на клетку. У одноэтапной системы детекции двух зондов чувствительность меньше: примерно 40 копий ДНК HPV на клетку, но она позволяет дифференцировать разные типы HPV в одном мазке. Двойная система детекции с амплификацией объединяет системы с низкой и высокой чувствительностью, позволяя проводить высокочувствительное определение HPV и не требующую высокой чувствительности детекцию последовательностей ДНК с большим числом повторов.
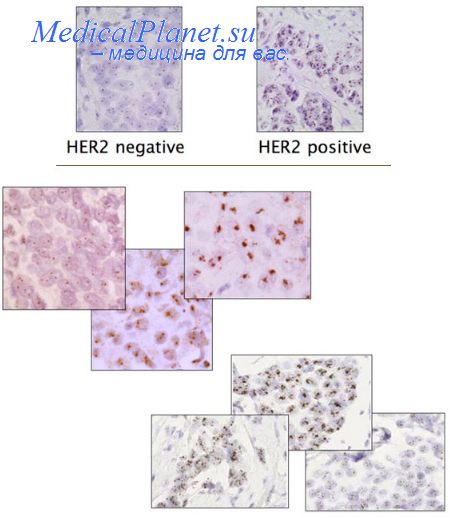
Точность ГИС определяется специфичностью гибридизации при условии, что регистрируемый сигнал обусловлен именно гибридизацией зонда. Неспецифическое связывание зонда можно исключить с помощью соответствующего контроля. Специфичность гибридизации зависит от жесткости условий, в которых она проводится, при этом условия нельзя найти из уравнений кинетики реассоциации в растворе, их приходится подбирать опытным путем. При гибридизации с хромосомоспецифичными зондами для этого сравнивают полученные результаты с локализацией гибридизационного сигнала на метафазных хромосомах.
В тех случаях, когда нужно различить близкородственные последовательности, например ДНК одного и того же вируса разных типов, условия гибридизации нужно подбирать, используя материал, инфицированный вирусом заведомо известного типа. Если это HPV-инфекция, то используют клеточные линии, содержащие ДНК HPV 16 и 18, или анализируют биоптаты с помощью других молекулярных методов, например ПЦР. При этом полученные результаты нельзя прямо экстраполировать на другие типы. Предположим, что в условиях, описанных в протоколе, удается различить HPV 6 и 11, HPV 16 и 18 или HPV 16 и 18. Отсюда не следует, что в этих же условиях можно различить HPV 16 и 33.
Практическое применение гибридизации in situ. Теоретически метод гибридизации in situ пригоден для анализа любого цитологического материала, однако на практике он пока применяется не очень широко. Самый большой опыт накоплен в выявлении этим методом вирусных геномов, особенно в мазках шейки матки. Методики, описанные в данной главе, были разработаны для рутинного выявления HVP в этих мазках и применялись для разграничения типов HPV с высокой и низкой патогенностью (17—20). В принципе они применимы для обнаружения других ДНК-содержащих вирусов, в частности вируса герпеса, и уже использовались для анализа клеточных культур, аспиратов и мазков шейки матки.
С помощью хромосомоспецифичных зондов можно определить как принадлежность цитологических образцов к определенному полу, так и их хромосомный состав. В клинике эти методы еще не освоены, однако возможность сопоставления данных по клеточной морфологии и по локализации гибридизационного сигнала и наличие методики, позволяющей провести анализ в течение рабочего дня, позволяют надеяться, что со временем ГИС станет обычным методом клинических исследований.
- Читать далее "Район ядрышкового организатора. Методы выявления ядрышкового организатора"
Оглавление темы "Исследование цитопрепаратов":1. Выбор неизотопной метки. Денатурация и гибридизация мРНК
2. Отмывание после неизотопной гибридизации. Обнаружение специфических мРНК
3. Транскрипция in situ мРНК. Неизотопная транскрипция in situ мРНК
4. Гибридизация in situ для диагностики цитопатологий. Получение материала и подготовка цитопрепаратов
5. Фиксация нуклеиновых кислот. Демаскирование нуклеиновых кислот
6. Денатурация цитопрепаратов. Гибридизация цитопрепаратов<
7. Отмывание цитопрепаратов. Детекция гибридизовавшегося зонда цитопрепаратов
8. Детекция двух разных зондов в цитопрепаратах. Контроли гибридизации цитопрепаратов
9. Результаты гибридизации цитопрепаратов. Специфичность гибридизации цитопрепаратов
10. Район ядрышкового организатора. Методы выявления ядрышкового организатора

