Отмывание цитопрепаратов. Детекция гибридизовавшегося зонда цитопрепаратов
Компоненты, не прореагировавшие при гибридизации, удаляют промыванием в растворе, не дестабилизирующем двухцепочечные гибриды зонд/мишень. Для этого определяют условия, при которых обеспечивается максимальное удаление «неправильных» гибридов. Чтобы уменьшить неспецифическое окрашивание, блокируют участки связывания антитела и авидина и ингибируют эндогенные ферменты. Это очень важно для повышения специфичности и чувствительности неизотопной гибридизации in situ, особенно при работе с цитологическими препаратами. . Ингибировать эндогенные ферменты можно на любой стадии до нанесения субстрата. В случае иммуноцитохимической детекции с помощью пероксидазы ингибирование обычно проводят после инкубации препаратов с первыми антителами, чтобы предотвратить разрушение антигенов в блокирующем растворе. При гибридизации in situ такой проблемы не возникает, поскольку молекулы-свидетели достаточно стабильны. Однако, если используется комплекс пероксид/азид натрия, в принципе может происходить химическая модификация зондов и мишеней, поэтому мы проводим блокирование пероксидазы до демаскирования. Это обеспечивает эффективное ингибирование пероксидазы эритроцитов и нейтрофилов в мазках шейки матки. Детально соответствующая процедура описана в протоколе.
Для детекции иммуномеченых зондов применяются те же подходы, что и для иммуноцитохимической локализации антигенов. Один момент, на который очень важно обратить внимание, — это повышение чувствительности при выявлении вирусных последовательностей в мазках шейки матки; для этого прибегают к процедуре наслаивания антител, описанной в протоколе для зондов, меченных дигоксигенином. Показано, что это позволяет обнаружить в клеточном материале всего 10 еномных копий вируса папилломы при длине каждой из копий тримерно 8 т.н.. Чтобы повысить чувствительность еще больше, проводят повторные инкубации с антителами. В результате удается обнаружить 1—2 геномные копии вируса HPV 16 в культуре клеток линии SiHa. Однако при рутинном анализе мазков этот метод может дать слишком большой фон,и в этом случае лучше использовать процедуру, описанную в ч. А фотокола.
Отмывание препаратов после гибридизации и детекция одного зонда
Эти протоколы применимы как для одного зонда, так и для смеси зондов, меченных дигоксигенином. Биотинилирован-ные зонды можно детектировать таким же способом, заменив в п. 3, ч. А антитела к дигоксигенину моноклональными антителами к биотину.
Материалы
• 20 х SSC: 3 М NaCl, 0,3 М цитрат натрия, рН 7,0. Этот буфер разводят до нужной концентрации дистиллированной водой
• Трис-солевой буфер (ТСБ): 50 мМ трис-НС1, 100 мМ NaCl, рН 7,2
• Трис-БСА-тритон (ТБТ): ТСБ, содержащий 3% (в/о) БСА, 0,05% (о/о) тритон-100
• Моноклональные антитела к дигоксину (Sigma, UK), биотини-лированные кроличьи антитела к иммуноглобулину мыши [фрагмент F(abh] (Dako, UK), авидин, конъюгированный с пероксидазой (Dako, UK)
• Субстрат 3-амино-9-этилкарбазол/пероксид водорода (АЭК/ Н2О2): можно получить готовый субстрат в составе набора (Zymed, USA) или в виде таблеток (Dako, UK) либо приготовить раствор из твердого субстрата
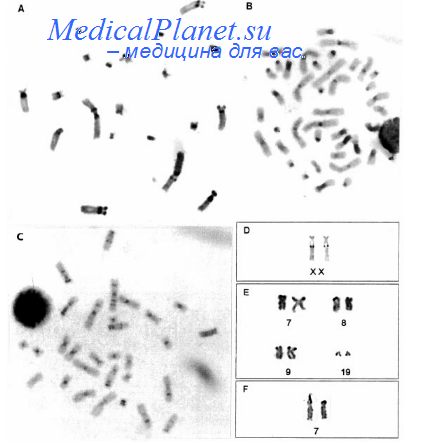
А. Стандартная процедура обработки препаратов
1. Промывают препараты в 4 х SSC при комнатной температуре, дважды по 5 мин, для отделения покровных стекол.
2. Инкубируют препараты в ТБТ в течение 10 мин при комнатной температуре.
3. Инкубируют препараты с моноклональными антителами к дигоксигенину, разведенными в ТБТ в отношении 1:10 000, в течение 30 мин при комнатной температуре; промывают в двух сменах ТСБ, по 5 мин в каждой.
4. Инкубируют препараты с биотинилированными кроличьими антителами к иммуноглобулину мыши [фрагмент F(ab)2], разведенными ТБТ в отношении 1:200, в течение 30 мин при комнатной температуре; промывают препараты в двух сменах ТСБ, по 5 мин в каждой.
5. Инкубируют препараты 30 мин при комнатной температуре с авидином, конъюгированным с пероксидазой; конъюгат разведен в ТБТ, содержащем 5% (в/о) обезжиренное молоко (Cadbury, UK), в отношении 1:75. Затем промывают препараты в двух сменах ТСБ, по 5 мин в каждой.
6. Инкубируют препараты в АЭК/Н202 в течение 15 мин при комнатной температуре.
7. Промывают препараты в дистиллированной воде и высушивают их на воздухе.
8. Контрастируют препараты в гематоксилине (обычно в течение 5—20 с), промывают в дистиллированной воде и высушивают на воздухе.
9. Заключают препараты в водорастворимую среду, например глицерин с желатиной.
Б. Обработка препаратов, повышающая чувствительность
1. Проводят процедуры
2. Инкубируют препараты с моноклональными антителами к биотину (Dako, UK), разведенными в ТБТ в отношении 1:50, в течение 30 мин при комнатной температуре.
3. Дважды по 5 мин промывают препараты в ТСБ.
4. Проводят операции.
- Для детекции биотинилированных зондов используют моноклональ-ные антитела к биотину, разведенные в ТБТ в отношении 1:50.
- Читать далее "Детекция двух разных зондов в цитопрепаратах. Контроли гибридизации цитопрепаратов"
Оглавление темы "Исследование цитопрепаратов":1. Выбор неизотопной метки. Денатурация и гибридизация мРНК
2. Отмывание после неизотопной гибридизации. Обнаружение специфических мРНК
3. Транскрипция in situ мРНК. Неизотопная транскрипция in situ мРНК
4. Гибридизация in situ для диагностики цитопатологий. Получение материала и подготовка цитопрепаратов
5. Фиксация нуклеиновых кислот. Демаскирование нуклеиновых кислот
6. Денатурация цитопрепаратов. Гибридизация цитопрепаратов<
7. Отмывание цитопрепаратов. Детекция гибридизовавшегося зонда цитопрепаратов
8. Детекция двух разных зондов в цитопрепаратах. Контроли гибридизации цитопрепаратов
9. Результаты гибридизации цитопрепаратов. Специфичность гибридизации цитопрепаратов
10. Район ядрышкового организатора. Методы выявления ядрышкового организатора

