Гибридизация in situ для диагностики цитопатологий. Получение материала и подготовка цитопрепаратов
Для обнаружения в цитологическом материале нуклеиновых кислот разработано множество разнообразных методов. Большинство из них предполагает выделение нуклеиновых кислот, а следовательно, разрушение клеток, и в последнее время все большее применение находят недеструктивные методы, прежде всего гибридизация in situ. В первую очередь это касается генетического материала вирусов. Преимущество гибридизации in situ состоит в том, что специфические нуклеотидные последовательности можно локализовать микроскопическими методами непосредственно в клетке. Большинство имеющихся на сегодня данных получено на ДНК, поэтому мы остановимся на применении метода ГИС только к нуклеиновым кислотам этого типа. Здесь речь пойдет о более подходящих для рутинной диагностики цитопатологий неизотопных методах.
Цитологический материал можно получить и подготовить разными способами, при этом лучше по возможности не вносить в отработанную процедуру никаких изменений. Цитологические препараты бывают двух основных типов:
• нативные мазки;
• мазки, полученные методом капли или осаждением клеток на стекло центрифугированием клеточной суспензии.
Первый, наиболее распространенный способ не предусматривает никакой предварительной очистки препаратов. Это создает проблемы при анализе, например, аспиратов или вышелушивающихся клеток шейки матки, когда эпителиальные клетки перемешаны с клетками из очага воспаления, слизистым секретом и бактериями. Как правило, цитологического материала для анализа бывает очень мало, поэтому препараты лучше всего готовить из клеточных суспензий с последующей их очисткой и нанесением на стекла центрифугированием или методом капли. Следует помнить, что в цитологическом препарате клетки не связаны друг с другом, и, работая с мазками шейки матки, нежелательно использовать центрифугирование, при котором клетки могут слипаться и смазывать всю картину; если есть хоть какая-то возможность получить мазки, окрашенные пероксидазой—антипероксидазой, лучше воспользоваться этим методом.
Как показывает наш опыт, мазки шейки матки можно готовить обычным способом. Другой цитологический материал, в частности клеточные линии и очищенные препараты лимфоцитов, лучше использовать в виде суспензий, полученных путем инокуляции клеток либо в изотонический физиологический раствор, либо в среду RPMI 1640 без добавок. Препараты из этих суспензий готовят методом капли или осаждения клеток на стекло центрифугированием суспензии с использованием, например, центрифуги фирмы Shandon, UK. При этом клетки на стекле могут образовывать сгустки, что мешает анализу. Мазки можно получить, либо раскапав на стекла саму культуральную среду, либо проведя сначала фиксацию, а затем обработку, аналогичную той, которая используется для приготовления препаратов распластанных метафазных хромосом. Этот последний способ описан в протоколе. По нашим данным, он позволяет получать препараты с лучшей морфологией и распределением клеток.
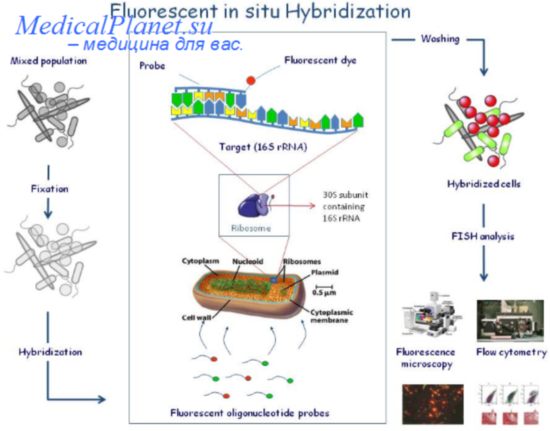
Приготовление цитологических препаратов
1. Готовят следующий раствор:
Метанол : уксусная кислота (МУК), 3:1 (о/о): сливают в вытяжном шкафу 25 мл ледяной уксусной кислоты и 75 мл метанола и перемешивают. Хранят раствор во льду не более 4 ч; для более длительного хранения держат его при -20 0С]).
2. Осаждают клетки центрифугированием при 600 g в течение 5—10 мин.
3. Удаляют по возможности весь супернатант, поставив пробирку в перевернутом виде на чистый лист бумаги.
4. Добавляют к осадку примерно такой же объем холодного МУК и аккуратно ресуспендируют клетки пипетированием.
5. Добавляют еще 10 объемов МУК, перемешивают содержимое пробирки, переворачивая ее несколько раз, и фиксируют клетки на льду в течение 20 мин.
6. Осаждают клетки центрифугированием при 600 g в течение 5 мин (осадок увеличивается в объеме за счет разбухания клеток), удаляют фиксатор и ресуспендируют осадок в 10 объемах МУК.
7. Повторяют этап 6 дважды, чтобы максимально дегидратировать суспензию. Такую суспензию клеток можно хранить при -20 С до 1 года.
8. Осаждают клетки центрифугированием при 600 g в течение 5 мин и ресуспендируют их в свежеприготовленном холодном МУК до получения молочно-белой суспензии.
9. Раскапывают по 5—20 мкл суспензии (в зависимости от ее плотности) на чистые предметные стекла. По мере испарения фиксатора клетки сами распределяются по стеклу.
- Этот раствор гигроскопичен, поэтому его следует хранить при -20 С.
- Не следует ресуспендировать клетки повторно, поскольку это приводит к потере нуклеиновых кислот. Если все же повторное ресуспендирова-ние необходимо, то осадок хранят при -20 С в 70% этаноле.
- В большинстве случаев подходят обычные предметные стекла, не покрытые адгезивами. Если клетки разрушены плохо, то стекла можно силиконировать.
- Когда суспензия дегидратирована, клетки распределяются по стеклу ровным слоем. Если в суспензии образуются капельки воды, повторяют этап 6, пока клетки не распределятся равномерно.
- Читать далее "Фиксация нуклеиновых кислот. Демаскирование нуклеиновых кислот"
Оглавление темы "Исследование цитопрепаратов":1. Выбор неизотопной метки. Денатурация и гибридизация мРНК
2. Отмывание после неизотопной гибридизации. Обнаружение специфических мРНК
3. Транскрипция in situ мРНК. Неизотопная транскрипция in situ мРНК
4. Гибридизация in situ для диагностики цитопатологий. Получение материала и подготовка цитопрепаратов
5. Фиксация нуклеиновых кислот. Демаскирование нуклеиновых кислот
6. Денатурация цитопрепаратов. Гибридизация цитопрепаратов<
7. Отмывание цитопрепаратов. Детекция гибридизовавшегося зонда цитопрепаратов
8. Детекция двух разных зондов в цитопрепаратах. Контроли гибридизации цитопрепаратов
9. Результаты гибридизации цитопрепаратов. Специфичность гибридизации цитопрепаратов
10. Район ядрышкового организатора. Методы выявления ядрышкового организатора

