Механизм развития (патогенез) воспалительных болезней кишечника
Воспалительная болезнь кишечника (ВБК) — хроническое заболевание, возникающее в результате неадекватной активации компонентов иммунной защиты слизистой оболочки кишки. ВБК представлена двумя заболеваниями — болезнью Крона и неспецифическим язвенным колитом (НЯК). Первые описания НЯК и болезни Крона относятся еще к периоду античности и XVI в. соответственно, однако для исключения инфекционной природы этих заболеваний понадобились современные бактериологические методы. Определенную роль в патогенезе воспалительных болезней кишечника (ВБК) играют, вероятно, микроорганизмы-комменсалы, в норме присутствующие в просвете кишки.
Различие между НЯК и болезнью Крона заключается прежде всего в локализации поражений и морфологических проявлениях заболевания. НЯК является тяжелым воспалительным заболеванием, которое ограничено ободочной кишкой и прямой кишкой и вовлекает в патологический процесс только их слизистую оболочку и подслизистый слой. Напротив, болезнь Крона, которую также называют регионарным энтеритом (поскольку в процесс часто вовлекается подвздошная кишка), может поражать любой сегмент Ж КТ, при этом поражение имеет трансмуральный характер.
а) Эпидемиология. И болезнь Крона, и НЯК чаще наблюдаются у подростков женского пола, а также у лиц в возрасте 20-30 лет. В развитых странах Запада ВБК распространена среди коренных жителей, а в США в 3-5 раз чаще наблюдается у евреев ашкенази. Отчасти это обусловлено генетическими факторами.
Заболеваемость ВБК в разных странах значительно варьирует: самая высокая частота — в Северной Америке, Северной Европе и Австралии. Заболеваемость ВБК продолжает расти во всем мире, ВБК все чаще регистрируют в регионах с исторически низкой распространенностью, таких как Африка, Южная Америка и Азия. Согласно гигиенической гипотезе, повышение заболеваемости может быть обусловлено улучшением условий хранения продуктов и снижением обсемененности пищи микроорганизмами.
В соответствии с этой гипотезой, снижение частоты кишечных инфекций приводит к нарушению регуляции иммунного ответа, позволяя повреждающим факторам, обычно вызывающим самостоятельно разрешающиеся заболевания, запускать чрезмерный иммунный ответ и хроническое воспаление у восприимчивых лиц. Хотя некоторые детали гигиенической гипотезы пока не выяснены, есть многочисленные наблюдения, подтверждающие ее. Так, глистные инвазии, эндемичные в регионах с низкой заболеваемостью ВБК, предотвращают развитие ВБК в эксперименте и уменьшают выраженность симптомов заболевания в клинике. Наблюдения у некоторых лиц эпизодов острого инфекционного гастроэнтерита, предшествующих началу ВБК, также согласуются с гигиенической гипотезой.
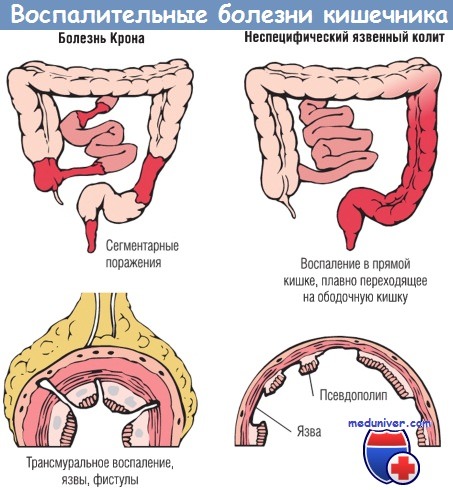
Различия между болезнью Крона и неспецифическим язвенным колитом основаны главным образом на морфологических изменениях.
б) Патогенез. ВБК является идиопатическим заболеванием, его причины и патогенез пока не совсем понятны. Установлена ограниченная эпидемиологическая связь ВБК с аутоиммунными процессами, однако ни болезнь Крона, ни НЯК не рассматриваются как аутоиммунные заболевания. Большинство исследователей предполагают, что эти заболевания являются результатом различных нарушений взаимодействия организма человека и кишечной микрофлоры, а также кишечной эпителиальной дисфункции и аномального иммунного ответа слизистой оболочки. Эта точка зрения подтверждается результатами эпидемиологических, генетических и клинических исследований, а также данными, полученными при изучении животных моделей ВБК.
в) Генетика. В патогенезе ВБК определенную роль играют генетические факторы. Риск развития заболевания увеличивается при наличии семейного анамнеза, а при болезни Крона конкордантность среди монозиготных близнецов достигает 50%. Генетические факторы также могут влиять на клинические особенности заболевания. Например, у близнецов, страдающих болезнью Крона, заболевание развивается с разницей около 2 лет и поражаются сходные участки ЖКТ. При НЯК конкордантность у монозиготных близнецов составляет только 16%, позволяя предполагать меньшее влияние генетических факторов, чем при болезни Крона. Конкордантность у дизиготных близнецов составляет менее 10% как для болезни Крона, так и для НЯК.
При анализе молекулярно-генетических нарушений у членов семей, страдающих болезнью Крона, был выявлен ген NOD2 (нуклеотидсвязывающего домена олигомеризации 2-го типа), который и рассматривают в качестве причины этого заболевания. Специфические полиморфизмы гена NOD2 связаны как минимум с 4-кратным увеличением риска развития болезни Крона у коренных жителей Европы. NOD2 кодирует синтез белка, связывающегося с внутриклеточными пептидогликанами бактерий, активируя NF-кВ. Было высказано предположение, что при заболеваниях, ассоциированных с полиморфизмами NOD2, организм человека сложнее распознает и уничтожает патогенную кишечную микрофлору. Это приводит к проникновению микроорганизмов в собственную пластинку слизистой оболочки кишки и запускает воспалительную реакцию.
Другие данные свидетельствуют о том, что NOD2 может регулировать иммунные реакции, предотвращая их избыточную активацию в ответ на патогенную кишечную микрофлору. Однако каким бы образом полиморфизмы NOD2 ни влияли на патогенез болезни Крона, заболевание развивается только у 10% лиц с мутациями NOD2. Кроме того, мутации NOD2 редко наблюдаются у лиц с болезнью Крона, проживающих в Африке и Азии. Таким образом, нарушения сигнальной системы NOD2 являются лишь одним из множества генетических факторов, вносящих свой вклад в патогенез болезни Крона.
Поиск ассоциированных с ВБК генов был проведен при исследовании полногеномных ассоциаций (GWAS), позволяющем выявить однонуклеотидные полиморфизмы. Число генов, выявленных при GWAS, быстро увеличивается (к 2010 г. было описано 30 генов). Наряду с NOD2 были описаны 2 гена, связанные с болезнью Крона и привлекающие наибольшее внимание исследователей:
(1) ген ATG16L1, связанный с аутофагией и являющийся частью аутофагосомального пути, играющий критическую роль в регуляции ответа клеток на внутриклеточные бактерии, а также, возможно, влияющий на процессы поддержания гомеостаза эпителиальных клеток;
(2) ген IRGM, кодирующий иммунозависимую ГТФазу М, а также регулирующий процессы аутофагии и уничтожения внутриклеточных бактерий. Точная роль NOD2, ATG16L1 и IRGM, экспрессируемых различными типами клеток, в развитии болезни Крона пока неясна. Однако факт, что NOD2, ATG16L1 и IRGM участвуют в распознавании и уничтожении внутриклеточных патогенов, поддерживает гипотезу о том, что неадекватный иммунный ответ на кишечную микрофлору является важным компонентом патогенеза ВБК. Ни один из указанных генов не ассоциируется с НЯК, но некоторые полиморфизмы рецептора IL-23 предотвращают развитие и болезни Крона, и НЯК.
- Иммунный ответ слизистой оболочки кишечника. Механизмы, посредством которых компоненты иммунной системы слизистой оболочки участвуют в патогенезе НЯК и болезни Крона, в настоящее время неизвестны. Главным методом лечения ВБК остается иммуносупрессия. При болезни Крона четко установлен факт поляризации хелперных Т-клеток в Тн1-клетки, но некоторые данные позволяют предположить, что в патогенезе заболевания также участвуют Тн17-клетки, поскольку на их развитие и выживание влияет IL-23, а некоторые полиморфизмы рецептора IL-23 обеспечивают защиту от болезни Крона и НЯК за счет ослабления провоспалительного ответа Тн17-клеток.
Роль Тн1- и Тн17-клеток в патогенезе заболевания доказывает и эффективность анти-TNF-терапии у некоторых пациентов с НЯК. Некоторые данные указывают на то, что НЯК является Тн2-опосредованным заболеванием, что согласуется с наблюдениями повышения концентрации IL-13 в слизистой оболочке у пациентов с НЯК. Сцепленные полиморфизмы в участках рядом с геном IL-10 при НЯК (но не при болезни Крона) указывают на важность системы иммунной регуляции в патогенезе ВБК [96]. Вероятно, существуют комбинации нарушений, активирующих иммунитет слизистой оболочки и подавляющих иммунорегуляторные воздействия, что и приводит к развитию НЯК и болезни Крона. В настоящее время объектом пристального внимания является изучение возможной роли нарушений врожденного и приобретенного иммунитета при ВБК.
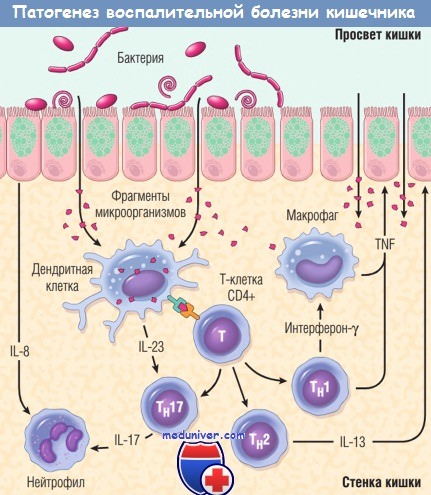
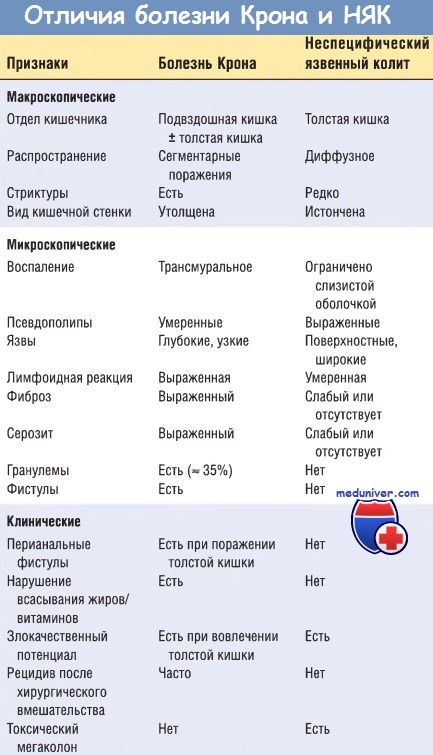
Представлены особенности болезни Крона и неспецифического язвенного колита.
Нарушение эпителиального барьера приводит к проникновению фрагментов микроорганизмов в стенку кишки.
IL — интерлейкин; TNF — фактор некроза опухоли.
- Дефекты эпителиальных клеток. При болезни Крона и НЯК описаны различные дефекты эпителиальных клеток. Например, у лиц с болезнью Крона, а также у большинства их здоровых родственников первой степени родства есть нарушения барьерной функции плотных контактов кишечных эпителиоцитов, сочетающиеся с полиморфизмами NOD2. В экспериментах показано, что барьерная дисфункция активирует врожденный и приобретенный иммунитет слизистой оболочки и повышает восприимчивость к заболеванию. Кроме того, наличие при болезни Крона мутации гена SLC22A4 (транспортера органических катионов) позволяет предположить участие в патогенезе ВБК нарушения трансэпителиального транспорта. Также в развитии заболевания могут играть определенную роль дефекты внеклеточного барьера, образованного секретируемой слизью. Интересно, что полиморфизмы гена ЕСМ1, который связан с матриксной металлопротеиназой 9, ассоциируются с НЯК, но не с болезнью Крона.
В настоящее время патогенетическая значимость мутаций ЕСМ1 не ясна, однако в эксперименте установлено, что подавление активности матриксной металлопротеиназы 9 уменьшает тяжесть проявлений НЯК. В заключение необходимо отметить, что у пациентов с болезнью Крона, имеющих мутации гена ATG16L1, есть аномалии гранул клеток Панета, содержащих антибактериальные пептиды дефенсины, что позволяет предположить роль нарушений антимикробной функции эпителия в патогенезе ВБК. Итак, несмотря на то что еще не до конца определены детали патогенеза и вероятные различия между болезнью Крона и НЯК, очевидно, что нарушение функции эпителия — один из важнейших компонентов патогенеза ВБК.
- Кишечная микрофлора. Количество микроорганизмов в толстой кишке насчитывает 1012 микробных тел на 1 мм ее длины. Кроме того, микроорганизмы составляют до 50% объема каловых масс. Количество кишечных микроорганизмов намного превосходит количество клеток нашего организма, т.е. на клеточном уровне мы только на 10% являемся собственно человеком. Состав кишечной микрофлоры у каждого человека стабилен, по крайней мере в течение нескольких лет, однако может меняться при изменении рациона питания и значительно различается у разных людей. Кроме микрофлоры, обитающей в просвете кишки, существует ограниченная популяция микроорганизмов, обитающих в слизистой оболочке кишки и, возможно, имеющих огромное влияние на здоровье человека.
Несмотря на растущее число доказательств роли кишечной микрофлоры в патогенезе ВБК, ее точная роль остается неизвестной и, скорее всего, различается при НЯК и болезни Крона. Так, у пациентов с болезнью Крона наличие антител к бактериальному белку флагеллину связано с полиморфизмами NOD2, а также с образованием стриктур, перфораций и вовлечением в процесс тонкой кишки, однако эта связь редко наблюдается у пациентов с НЯК. Кроме того, при болезни Крона могут быть эффективными некоторые антибиотики, например метронидазол, а антибиотики широкого спектра предотвращают развитие заболевания в экспериментальных моделях ВБК. Проведенные к настоящему времени исследования выявили, что некоторые препараты, содержащие пробиотики (полезные бактерии), эффективны для лечения болезни как в эксперименте, так и у пациентов с ВБК, хотя механизм действия пробиотиков недостаточно ясен.
В одной из животных моделей заболевания, учитывающей роли кишечной микрофлоры, нарушения функции эпителия и иммунного ответа слизистой оболочки, исследовали наличие циклического процесса, при котором трансэпителиальный переход бактерий из просвета кишки активирует врожденный и при обретенный иммунитет. У лиц с генетической предрасположенностью выделение эпителием TNF и других иммуноопосредованных сигнальных молекул повышает проницаемость плотных контактов, что увеличивает количество проникающих через эпителий микроорганизмов. Такие изменения могут приводить к формированию порочного круга, в котором стимуляция любого из патогенетических звеньев вызывает развитие ВБК.
Данная модель помогает понять патогенез ВБК, однако необходимо помнить, что в развитии заболевания участвуют очень многие факторы. Например, после аппендэктомии риск развития НЯК снижается. Курение также изменяет эпидемиологию ВБК, но парадоксальным образом: риск болезни Крона повышается, а риск НЯК снижается.
- Рекомендуем ознакомиться со следующей статьей "Механизм развития (патогенез) болезни Крона"
Оглавление темы "Патогенез болезней кишечника":- Механизм развития (патогенез) синдрома раздраженного кишечника
- Механизм развития (патогенез) воспалительных болезней кишечника
- Механизм развития (патогенез) болезни Крона
- Механизм развития (патогенез) неспецифического язвенного колита
- Механизм развития (патогенез) неопределенного колита
- Механизм развития (патогенез) опухоли при воспалительной болезни кишечника
- Механизм развития (патогенез) колита в отключенном сегменте кишечника
- Механизм развития (патогенез) микроскопического колита
- Механизм развития (патогенез) дивертикулов толстой кишки
- Механизм развития (патогенез) полипов желудочно-кишечного тракта

