Схема возникновения и проведения возбуждения в сердце
Сердце содержит мышечные клетки (волокна), генерирующие и проводящие импульсы возбуждения [проводящая система), а также «рабочий» миокард, отвечающий сокращением в ответ на возбуждение. В отличие от скелетных мышц, возбуждение возникает в самом сердце (ауторитмичность, или автономность, сердца). Миоциты предсердий и желудочков ветвятся, образуя пучки.
Располагаются они не изолированно, а соединяются друге другом посредством щелевидных контактов (нексусов). В результате стимул, возникающий в предсердиях или желудочках, всегда вызывает полноценное сокращение либо обоих предсердий, л ибо обоих желудочков (сокращение по типу «все или ничего»),
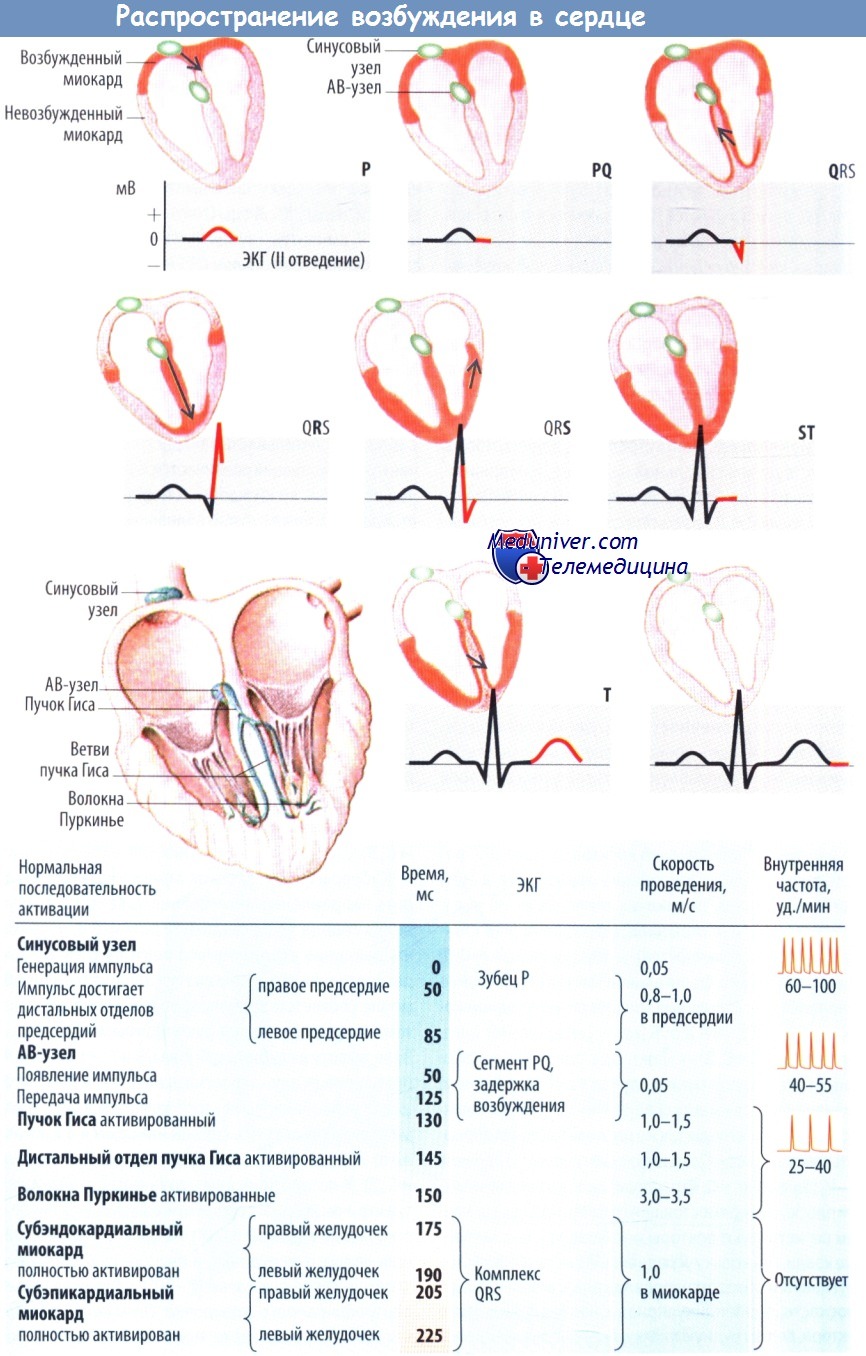
В норме стимулы, возбуждающие сердце, генерируются синусовым узлом, являющимся водителем сердечного ритма. Отсюда стимул распространяется по обоим предсердиям к атриовентрикулярному (АВ) узлу, откуда по пучку Гиса и двум его ножкам (Тавары) достигает волокон Пуркинье, передающих стимул в миокард желудочков.
В миокарде стимул распространяется в направлении изнутри наружу (от эндокарда к эпикарду) и от верхушки к основанию сердца. Процесс распространения стимула можно проследить с помощью ЭКГ, при этом не требуется вмешательство в организм.
Потенциал, генерируемый клетками синусового узла, является управляющим (пейсмекерным). Мембрана этих клеток не имеет постоянного потенциала покоя. После каждой реполяризации его значение возрастает. Наибольшее отрицательное значение потенциала их мембраны (около —70 мВ) называют максимальным диастолическим потенциалом (МДП).
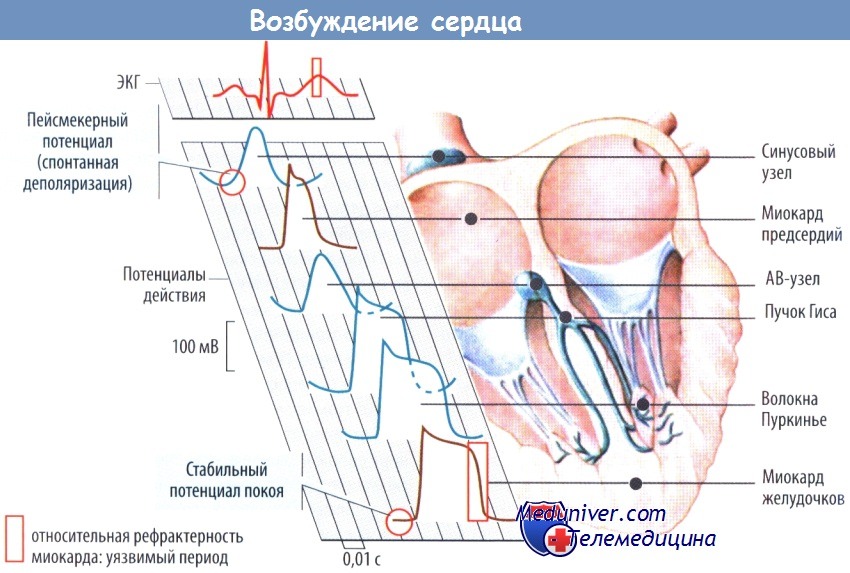
Постепенно мембранный потенциал возрастает, пока не достигнет порогового значения (пороговый потенциал), равного -40 мВ. В этот момент возникает потенциал действия (ПД).
Эти потенциалы возникают вследствие описанных ниже изменений ионной проводимости (д) плазматической мембраны, а следовательно, и ионных токов (I). Начиная с МДП возрастает неселективная проводимость, и поток катионов внутрь клетки (If; f = поток) приводит к медленной деполяризации ее мембраны (предпотенциал).
После достижения порогового потенциала относительно быстро возрастает дСа, величина потенциала повышается настолько быстро, что возросший приток ионов Са2+ (ICa) в клетку приводит к возникновению ПД, имеющего положительное значение. После того как потенциал мембраны клетки изменится сотрицательного на положительный, возникает поток ионов К+ из клетки (Ik). Мембрана пейсме-керной клетки вновь реполяризуется до МДП.
Каждый ПД, возникающий в синусовом узле в норме вызывает сокращение сердца, т. е. частот; импульсов, генерируемых водителем ритма, определяет ЧСС.
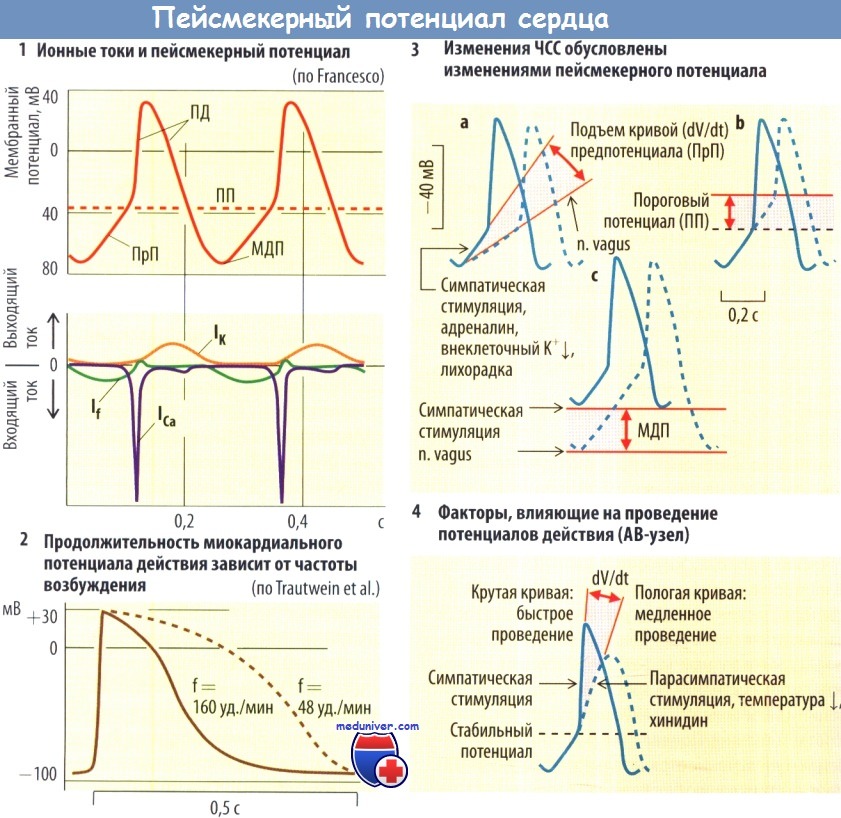
Частота импульсов уменьшается в cледующих ситуациях:
- более медленный рост потенциала в фазу медленной деполяризации;
- пороговый потенциал становится менее отрицательным (отрицательный батмотропный эффект) МДП становится более отрицательным, в результате чего спонтанная деполяризация начинается с более низкого уровня;
- реполяризация в фазу ПД начинается позже илb протекает медленнее.
Общим для первых трех ситуаций является то, что в их случае пороговое значение мембранногс потенциала достигается быстрее.
Все компоненты проводящей системы обладают способностью к спонтанной деполяризации, но синусовый узел играет ведущую роль в нормальном возбуждении сердца (синусовый ритм равен 70-80 уд./мин). Причина этого кроется в том, что по сравнению с синусовым узлом остальные компоненты проводящей системы обладают менее выраженной способностью к автоматизму. Таким образом, стимул, возникший в синусовом узле, достигнет дистальных отделов проводящей системы раньше, чем их спонтанная деполяризация достигнет величины порогового потенциала.
Однако при нарушении проведения стимулов от синусового узла активируется автоматизм АВ-узла, расположенного дистальнее, и сердце станет работать в ритме АВ-узла (40-60 уд./мин) или, при определенных обстоятельствах, в ритме так называемых пейсмекеров третьего порядка (желудочковых), расположенных еще более дистально, с частотой 20-40 уд./мин.
Кроме синусового и АВ-узла с их относительно медленно нарастающим ПД, во многом обусловленным потоком ионов Са2+ внутрь клетки, в работающем миокарде имеются так называемые быстрые потенциалзависимые Na+-каналы, которые в начале ПД обеспечивают кратковременный мощный поток ионов Na+ внутрь клетки и, таким образом, в отличие от пейсмекерного потенциала, сравнительно быстрый подъем ПД.
Относительно большая длительность (по сравнению со скелетными мышцами) миокардиального ПД, придающая ему вытянутую форму, имеет важное значение, поскольку препятствует возникновению замкнутых кругов циркуляции стимулов, возбуждающих миокард (механизм повторного входа, или реэнтри). Также это верно и для ситуаций с очень высокой или низкой ЧСС, поскольку длительность ПД подстраивается под ЧСС.
ПД приводит к активации потенциалзависимых Са2+-каналов, чувствительных к дигидропиридину, благодаря чему ионы Са2+ перемещаются из внеклеточного пространства внутрь клетки. В результате возникает локальное повышение концентрации ионов Са2+ в цитоплазме (Са2+-«скачок»), после чего открываются лигандзависимые и рианодин-чувствительные Са2+-каналы саркоплазматического ретикулума (так называемый триггерный эффект), играющего роль депо ионов Са2+. Ионы Са2+, поступающие из саркоплазматического ретикулума в цитоплазму, в конечном итоге запускают электромеханический процесс, приводящий к сокращению сердца.
Концентрация ионов Са2+ в цитоплазме также зависит от скорости их накопления в депо (при участии транспортной Са2+-АТФазы сарко-эндоплазматического ретикулума [SERCA —Са2+-насос]) и отскорости транспорта ионов Са2+ во внеклеточное пространство. Последний осуществляется посредством Са2+-АТФазы (перемещающей 1 ион Са2+ в обмен на 2 иона Н+) и Na+-Са2+-обменника, перемещающего 1 ион Са2+ в обмен на 3 иона Na+, работающего под влиянием электрохимического градиента, создаваемого разностью концентраций ионов Na+ (в свою очередь, формируемой действием Na+/К+-АТФазы) по обе стороны клеточной мембраны.
Хотя сердце и сокращается автономно, адаптация сердечной деятельности к потребностям организма в основном осуществляется посредством эфферентных сердечных нервов. С помощью нервных влияний могут изменяться следующие качественные характеристики сердечной деятельности:
- частота формирования импульсов водителем ритма и, соответственно, ЧСС (хронотропизм); скорость проведения импульсов, особенно по АВ-узлу (дромотропизм);
- сила сокращений миокарда при данной степени его растяжения, т. е. сократительная способность сердца (инотропизм);
- скорость расслабления за счет изменения активности SERCA (лузитропизм); - возбудимость сердца, т. е. изменение порога возбудимости (батмотропизм).
Указанные изменения сердечной деятельности развиваются под влиянием парасимпатических (ветви блуждающего нерва) и симпатических стимулов. ЧСС возрастает при увеличении активности симпатических волокон синусового узла (положительный инотропный эффект, реализующийся через b1-рецепторы) и снижается при увеличении активности парасимпатических мускариновых волокон (отрицательный хронотропный эффект). Реализуются эти эффекты путем изменения скорости медленной деполяризации и величины МДП синусового узла.
Подавление медленной деполяризации и увеличение отрицательного значения МДП в ответ на стимуляцию блуждающего нерва обусловлено увеличением gk, в то время как увеличение скорости медленной деполяризации, возникающее в ответ на симпатическую стимуляцию или под влиянием адреналина, — увеличением gCa, а при определенных обстоятельствах и снижением gk. Более дистальные (периферические) отделы проводящей системы отвечают хронотропным эффектом только на симпатические стимулы, и именно эти стимулы играют решающую роль в возможности захвата ритмоводителя АВ-узлом или пейсмекерами третьего порядка.
Парасимпатические волокна левого блуждающего нерва замедляют проведение импульса по АВ-узлу, а симпатические волокна ускоряют его (соответственно отрицательное и положительное дромотропные влияния). При этом в основном изменяется МДП и скорость нарастания ПД. Также важную роль в этом играют изменения gk и gCa.
В отличие от хронотропного и дромотропного влияний положительное инотропное влияние симпатической нервной системы на работающий миокард является непрямым. Повышение сократительной способности обусловлено увеличением потока ионов Са2+ внутрь клетки, опосредуемого b1-адренорецепторами, в результате чего в цитоплазме клеток миокарда повышается концентрация ионов Са2+. Это увеличение потока ионов Са2+ можно подавить фармакологически путем блокирования Са2+-каналов (так называемыми блокаторами Са2+-каналов).
Стимуляция b1-адренорецепторов сердца приводит к фосфорилированию фосфоламбана, что сопровождается увеличением активности SERCA и последующим расслаблением миокарда (положительное лузитропное действие).
Сократительная способность миокарда также увеличивается вследствие удлинения ПД (поток ионов Са2+ внутрь клетки будет осуществляться более длительно) или подавления Na+/K+-АТФазы, например, под влиянием сердечных гликозидов. таких как дигоксин и дигитоксин (уменьшение градиента ионов Na+ по обе стороны клеточной мембраны => уменьшение эффективности обмена 3 ионов Na+ на 1 ион Са2+=>уменьшение выброса ионов Са2+=>увеличение концентрации ионов Са2+ в цитоплазме).
При снижении ЧСС со временем уменьшается поток ионов Са2+ в клетку (уменьшение числа ПД), в результате между ПД имеется относительно длинный промежуток, во время которого может осуществляться поток ионов Са2+ из клетки. Таким образом, средняя концентрация ионов Са2+ в цитоплазме снижается, а следовательно, поддерживается низкая сократительная способность миокарда. Регулирующие влияния блуждающего нерва реализуются с помощью такого же механизма; однако он действует опосредованно, за счет отрицательного инотропного влияния (частотный инотропизм). Симпатическая стимуляция сопровождается противоположными эффектами.
Учебное видео расшифровки ЭКГ в норме
- Рекомендуем ознакомиться со следующей статьей "Схема образования зубцов и интервалов электрокардиограммы (ЭКГ)"
Оглавление темы "Патофизиология в схемах":- Схема фаз сердечного цикла
- Схема возникновения и проведения возбуждения в сердце
- Схема образования зубцов и интервалов электрокардиограммы (ЭКГ)
- Схема развития тахикардии
- Схема развития экстрасистол
- Схема развития АВ-блокады
- Схема развития реэнтри в миокарде
- Схема развития реэнтри в АВ-узле
- Схема развития синдрома Вольфа—Паркинсона—Уайта (WPW синдрома)
- Схема развития митрального стеноза

