Механизмы развития (патофизиология) гипертрофии сердца
Усиленная механическая работа при постоянной перегрузке сердца давлением или объемом (например, в случае артериальной гипертензии или аортального стеноза) либо трофические сигналы (в частности, опосредованные активацией b-адренергических рецепторов) увеличивают размер кардиомиоцитов. Постепенно это приводит к увеличению толщины стенок (гипертрофии) и массы сердца.
Гипертрофия обусловлена повышенным синтезом белка, что приводит к накоплению дополнительных саркомеров. Гипертрофированные кардиомиоциты содержат также повышенное количество митохондрий и увеличенные ядра. Последнее обусловлено, по-видимому, повышенной плоидностью дезоксирибонуклеиновой кислоты (ДНК), поскольку репликация ДНК происходит в отсутствие клеточного деления.
Тип гипертрофии отражает природу стимула. Гипертрофия желудочков может быть следствием перегрузки давлением, что приводит к концентрическому увеличению толщины их стенки. При повышенном давлении новые саркомеры располагаются преимущественно параллельно длинной оси кардиомиоцитов, увеличивая их площадь поперечного сечения. В отличие от этого гипертрофия вследствие перегрузки объемом происходит дилатация желудочков. В этой ситуации новые саркомеры располагаются последовательно по отношению к уже существующим.
В результате толщина стенки может быть увеличенной или уменьшенной по сравнению с нормой либо нормальной, поэтому наиболее верным критерием гипертрофии, обусловленной перегрузкой объемом, служит масса сердца, а не толщина его стенок.
Гипертрофия сердца нередко достигает значительной степени при клинически выраженной болезни сердца. У пациентов с артериальной гипертензией, ИБС, аортальным стенозом, митральной регургитацией или дилатационной кардиомиопатией масса сердца может превышать норму в 2-3 раза, а у пациентов с аортальной регургитацией или гипертрофической кардиомиопатией — в 3-4 раза.
При гипертрофии сердца происходят важные изменения на уровне тканей и клеток. Увеличение размера кардиомиоцитов не сопровождается пропорциональным возрастанием числа капилляров, в результате доставка кислорода и питательных веществ гипертрофированному сердцу, особенно при гипертрофии, обусловленной перегрузкой давлением, уменьшена по сравнению с доставкой в нормальном сердце. В то же время потребление кислорода гипертрофированным сердцем повышено вследствие усиленной нагрузки, являющейся причиной патологического процесса.
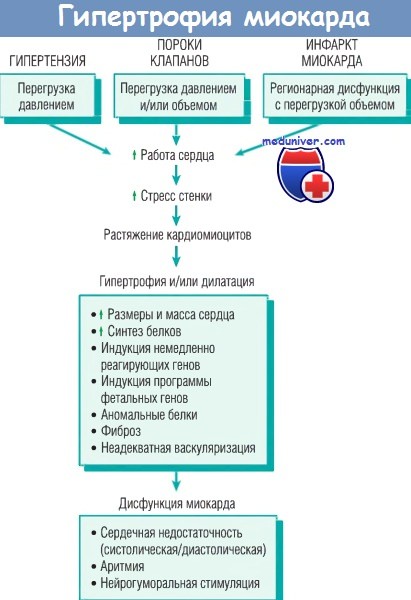
Гипертрофия сердца также часто сопровождается разрастанием фиброзной ткани. Молекулярные изменения включают экспрессию немедленно реагирующих генов, например c-FOS, c-MYC, c-JUN и EGR1. При продолжительной гемодинамической перегрузке может произойти сдвиг экспрессии генов, которая становится сходной с экспрессией, наблюдаемой в течение развития сердца у плода (включая избирательную экспрессию эмбриональной/фетальной форм тяжелой цепи b-миозина, натрийуретических пептидов и коллагена).
На функциональном уровне гипертрофия сердца ассоциируется с повышенными метаболическими потребностями вследствие увеличения напряжения стенки, ЧСС и сократимости (инотропное состояние, или сила сокращения). Все это повышает потребление кислорода миокардом. В результате гипертрофированное сердце склонно к декомпенсации, которая может перейти в сердечную недостаточность, а со временем привести к смерти. Последовательность первоначально благоприятных, а затем патологических процессов в ответ на усиленную работу сердца представлена на рисунке ниже.
Молекулярные и клеточные изменения в гипертрофированном сердце, опосредующие вначале усиление функции, могут способствовать развитию сердечной недостаточности. Причинами могут быть:
(1) аномальный метаболизм миокарда;
(2) изменения внутриклеточного перемещения ионов кальция;
(3) апоптоз кардиомиоцитов;
(4) репрограммирование экспрессии генов.
Последнее происходит отчасти в результате изменений экспрессии маленьких молекул рибонуклеиновой кислоты (микроРНК) — некодирующих РНК, ингибирующих экспрессию белков на уровне стабильности или трансляции матричной РНК (мРНК). Гипертрофия сердца ассоциируется с понижающей регуляцией микроРНК-208 и повышающей регуляцией микроРНК-195. Следует отметить, что у мышей усиленная гиперэкспрессия микроРНК-195 может вызвать гипертрофию и дилатацию сердца, тогда как гиперэкспрессия микроРНК-208 обладает защитным действием даже в условиях повышенного давления.
Степень структурного нарушения сердца при ХСН не всегда отражает уровень дисфункции, и структурные, биохимические и молекулярные основы сократительной дисфункции миокарда могут быть неясными. На практике бывает невозможно на основании морфологического исследования отличить поврежденное, но сохранившее свою функцию сердце от сердца с нарушенной функцией. При аутопсии сердце пациентов с ХСН тяжелое, расширенное, имеет тонкую стенку, и при микроскопическом исследовании обнаруживаются признаки гипертрофии.
Степень этих изменений крайне вариабельна. При инфаркте миокарда утрата насосной функции вследствие гибели кардиомиоцитов приводит к связанной с нагрузкой гипертрофии окружающего жизнеспособного миокарда. В случае болезни клапанов сердца повышенные давление или объем обусловливают общую перегрузку миокарда.
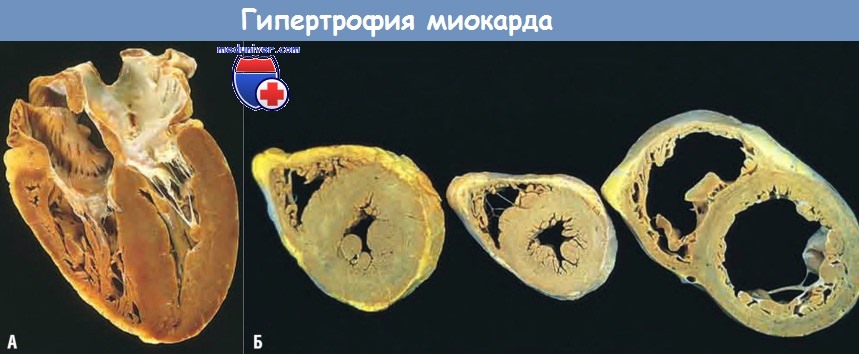
(А) Гипертрофия вследствие перегрузки давлением, обусловленной обструкцией выводного тракта левого желудочка.
Продольный срез через все 4 камеры сердца, левый желудочек — внизу справа.
(Б) Гипертрофия с дилатацией (справа) и без нее (слева) полости левого желудочка.
Поперечный срез, в центре — нормальное сердце.
Сердце, гипертрофированное вследствие перегрузки давлением (слева и на А),
имеет увеличенную массу и толщину стенки левого желудочка, тогда как масса гипертрофированного и дилатированного сердца (справа) увеличена, но его стенка имеет нормальную толщину.
Увеличение массы сердца коррелирует с повышенной заболеваемостью и смертностью от болезней сердца, а кардиомегалия служит независимым фактором риска внезапной смерти. В отличие от патологической гипертрофии (часто ассоциированной с нарушением сократимости миокарда) гипертрофия, индуцированная регулярной интенсивной физической нагрузкой, оказывает различный эффект на сердце в зависимости от типа нагрузки.
Аэробная нагрузка (например, бег на длинные дистанции) может ассоциироваться с гипертрофией на фоне перегрузки объемом и сопровождаться увеличением числа (плотности) капилляров. Такая гипертрофия претерпевает обратное развитие после продолжительного отдыха от нагрузок. Подобные изменения миокарда называют физиологической гипертрофией. Статическая нагрузка (например, поднятие тяжестей) связана с гипертрофией вследствие давления и с большей вероятностью ассоциирована с неблагоприятными изменениями.
Независимо от причины развития ХСН характеризуется различной степенью снижения сердечного выброса и перфузии тканей (антеградная сердечная недостаточность), а также скоплением крови в венозной системе (хроническая сердечная недостаточность). Последняя может стать причиной отека легких и периферического отека. Многие из важных клинических признаков и морфологических изменений, отмечаемых при ХСН, являются вторичными по отношению к повреждениям, индуцированным гипоксией и венозным полнокровием тканей, отдаленных от сердца.
Сердечно-сосудистая система обеспечивает кровообращение по закрытому контуру. Левожелудочковая и правожелудочковая недостаточность могут возникать независимо друг от друга, однако недостаточность одного круга кровообращения (особенно большого) часто вызывает избыточное напряжение в другом круге, приводя в конечном итоге к тотальной сердечной недостаточности. Несмотря на эту взаимозависимость, для лучшего понимания патологии сердечной недостаточности целесообразно рассмотреть левожелудочковую и правожелудочковую недостаточность по отдельности.
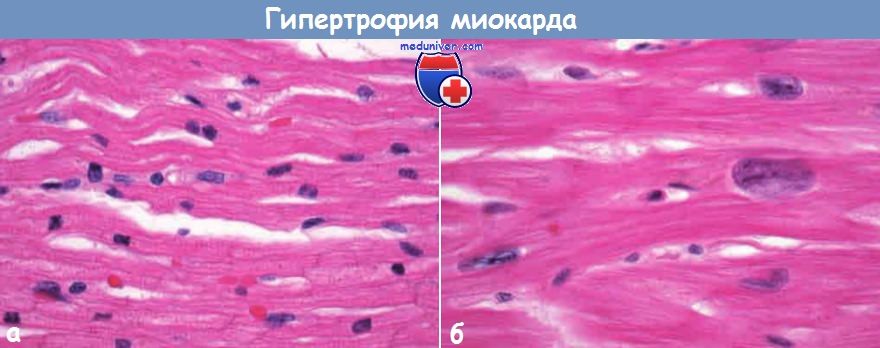
(а) Нормальный миокард.
(б) Гипертрофированный миокард: увеличен размер клеток и их ядер
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патофизиология) левожелудочковой сердечной недостаточности"
Оглавление темы "Патогенез болезней сердца":- Строение сердца и его физиология
- Возрастные изменения сердца
- Общие механизмы развития болезней сердца
- Механизмы развития (патофизиология) сердечной недостаточности
- Механизмы развития (патофизиология) гипертрофии сердца
- Механизмы развития (патофизиология) левожелудочковой сердечной недостаточности
- Механизмы развития (патофизиология) правожелудочковой сердечной недостаточности
- Механизмы развития (патофизиология) врожденных пороков сердца
- Клиника врожденного порока сердца
- Механизмы развития (патофизиология) дефекта межпредсердной перегородки (ДМПП)

