Механизмы развития (патофизиология) врожденных пороков сердца
Врожденные пороки сердца — это термин, используемый для описания врожденных дефектов развития сердца или крупных сосудов. Большинство таких дефектов возникает в результате нарушений эмбриогенеза в течение 3-8-й недель беременности, когда формируются и начинают функционировать основные структуры сердечно-сосудистой системы. Тяжелые аномалии в большинстве случаев несовместимы с вынашиванием беременности.
Врожденные дефекты сердца, совместимые с эмбриональным развитием и рождением, затрагивают отдельные камеры или области сердца, тогда как оставшаяся часть сердца развивается относительно нормально. Примером могут служить дети, рождающиеся с дефектами септации (с «отверстием в сердце»), например с дефектом межпредсердной перегородки (ДМПП) или дефектом межжелудочковой перегородки (ДМЖП), стенозирующими поражениями клапанов или аномалиями коронарных артерий.
Некоторые формы врожденных пороков сердца проявляются клинически вскоре после рождения, что часто обусловлено переходом от фетального типа кровообращения к постнатальному (связанному с оксигенацией крови в легких, а не доставкой крови через плаценту). В 50% случаев врожденные пороки сердечно-сосудистой системы диагностируют в течение первого года жизни, однако некоторые менее серьезные формы пороков (например, ДМПП) могут проявиться лишь у взрослых.
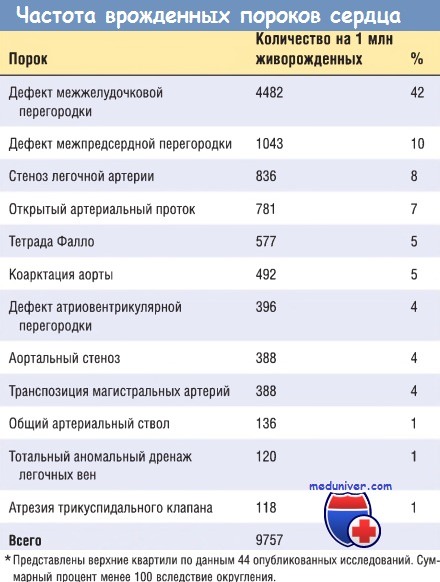
а) Распространение. Врожденные пороки сердечнососудистой системы — наиболее распространенные пороки развития (1%, или 4-50 случаев на 1000 живорождений) и наиболее частый тип болезней сердца у детей. Частота таких пороков выше у недоношенных детей по сравнению с родившимися в срок. Основные врожденные пороки сердца, составляющие 85% всех случаев, и их частота перечислены в таблице ниже.
Количество лиц с врожденными пороками сердца, доживающих до зрелого возраста, быстро увеличивается. В настоящее время в США насчитывают 1 млн таких людей. Это результат усовершенствования хирургических техник и «агрессивных» методов лечения различных структурных дефектов сердца. Тем не менее подобные репаративные меры не возвращают сердце в нормальное состояние. У таких пациентов в дальнейшем возможно развитие аритмий и нарушений функции желудочков, что приводит к необходимости дополнительного хирургического вмешательства.
К другим факторам, способным повлиять на отдаленные результаты, относят риск, связанный с применением материалов и устройств для протезирования, например искусственных клапанов или заменителей участков миокарда, а также риск со стороны матери, ассоциированный с родами.
б) Развитие сердца. Врожденные пороки сердца обусловлены дефектами, возникающими во время закладки и развития сердца как органа. В связи с этим, прежде чем рассматривать специфические расстройства, кратко опишем процесс развития сердца в нормальных условиях. Самые ранние зачатки сердца возникают в латеральной мезодерме и перемещаются к срединной линии посредством двух волн миграции, образуя серповидный слой клеток, составляющих первое и второе поля сердца, примерно к 15-му дню развития. Каждое поле сердца характеризуется экспрессией различных наборов генов.
Так, первое поле сердца экспрессирует факторы транскрипции ТВХ5 и Handl, тогда как второе поле — Hand2 и фактор роста фибробластов 10. Оба поля содержат мультипотентные клетки-предшественники, способные к образованию всех основных типов клеток сердца: эндокардиальных, миокардиальных и гладкомышечных. Эти ранние клетки-предшественники привлекают внимание исследователей в связи с возможным использованием этих клеток для восстановления поврежденных отделов сформированного сердца или утративших функцию по другим причинам.
Даже на очень ранней стадии развития каждое поле сердца уже предназначено для формирования определенных частей сердца. Из клеток первого поля в основном образуется левый желудочек, из клеток второго поля — выводной тракт, правый желудочек и большая часть предсердий. К 20-му дню первоначальный разрастающийся клеточный слой превращается в пульсирующую трубку, которая петлеобразно изгибается направо, и на 28-й день начинают формироваться камеры сердца. Примерно в это же время происходят два других важных события: (1) клетки нервного гребешка мигрируют в выводной тракт, где участвуют в его септации и формировании дуги аорты; (2) ВКМ, из которого в дальнейшем образуются АВ-канал и выводной тракт, увеличивается, образуя утолщения — эндокардиальные подушки.
Этот процесс зависит от разделения субпопуляции эндокардиальных клеток, проникающих в ВКМ, а затем пролиферирующих и дифференцирующихся в мезенхимальные клетки, ответственные за развитие клапанов. К 50-му дню происходят септация желудочков, предсердий и разделение АВ-клапанов, что приводит к образованию четырехкамерного сердца.
Координация всех этих процессов трансформации зависит от активности факторов транскрипции, регулируемых сигналами, источником которых служат такие агенты, как Wnt, VEGF, фактор морфогенеза костей, TGF-P, фактор роста фибробластов и Notch. Необходимо также иметь в виду, что сердце — механический орган, подвергающийся действию кровотока уже на самых ранних стадиях развития. Возможно, что гемодинамические силы имеют такое же важное влияние на развитие сердца, какое они оказывают на адаптацию сформированного сердца, в частности на гипертрофию и дилатацию.
Кроме того, важнейшее значение в развитии сердца имеют специфические микроРНК, координирующие формы и уровень экспрессии факторов транскрипции.
Многие из генетических дефектов, нарушающих процесс развития сердца, обусловлены аутосомно-доминантными мутациями, приводящими к частичной утрате функции того или иного фактора транскрипции (см. далее). Таким образом, даже относительно слабые изменения активности одного из многих факторов транскрипции, необходимых для нормального развития сердца, могут привести к дефектам, обнаруживаемым затем в полностью сформированном сердце. Возможно, преходящее экзогенное стрессорное воздействие в I триместре беременности способно повлиять на гены и вызвать дефекты, напоминающие таковые при наследственных мутациях.
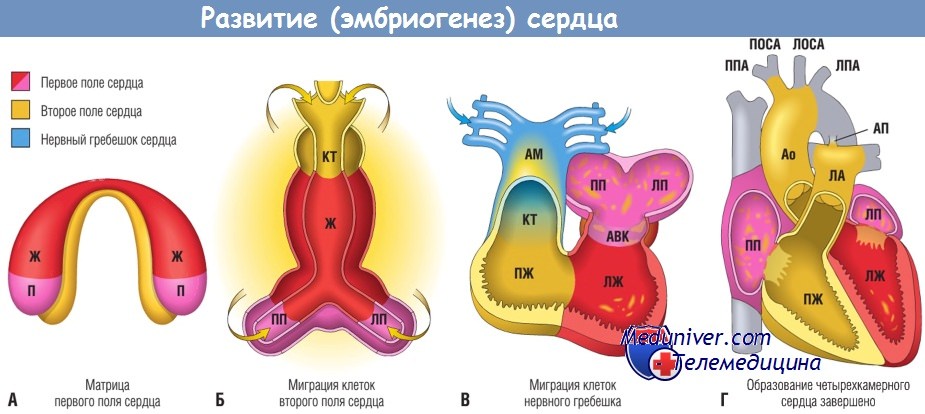
(А) День 15-й. В передней части эмбриона находятся первое поле сердца полулунной конфигурации и клетки второго поля сердца.
(Б) День 21-й. Клетки второго поля сердца лежат дорсально по отношению к прямой сердечной трубке и начинают мигрировать (стрелки) в передний и задний концы трубки,
образуя желудочек (Ж), конотрункус (КТ) и часть правого предсердия (ПП) и левого предсердия (ЛП).
(В) День 28-й. После петлеобразного изгибания сердечной трубки направо клетки нервного гребешка сердца также мигрируют (стрелки) из нервного валика в выводной тракт и участвуют в образовании его перегородки и билатерально симметричных артериальных дуг (III, IV и VI).
(Г) День 50-й. Формирование межпредсердной и межжелудочковой перегородок, а также АВ-клапанов приводит к образованию четырехкамерного сердца с конфигурацией, соответствующей изгибу сердечной трубки.
АВК — атриовентрикулярный канал; AM — аортальный мешок; Ао — аорта;
АП — артериальный проток; ЛА — легочная артерия; ЛЖ — левый желудочек;
ЛОСА — левая общая сонная артерия; ЛПА — левая подключичная артерия; П — предсердие;
ПЖ — правый желудочек; ПОСА — правая общая сонная артерия; ППА — правая подключичная артерия.
в) Этиология и патогенез врожденных пороков сердца. Основной установленной причиной врожденных пороков сердца являются спорадические генетические нарушения: мутации одиночного гена, небольшие хромосомные делеции и вставки или делеции целых хромосом (трисомии и моносомии). В случае мутаций одиночного гена речь идет о генах, кодирующих белки, которые относятся к различным функциональным классам. Многие из этих мутаций затрагивают гены, кодирующие факторы транскрипции, необходимые для нормального развития сердца. Поскольку такие пациенты гетерозиготны по этим мутациям, снижения активности данных факторов на 50%, вероятно, достаточно для нарушения развития сердца.
Некоторые из мутантных факторов транскрипции функционируют вместе в составе крупных белковых комплексов. Это объясняет, почему мутация любого из них вызывает сходные эффекты. Например, три фактора транскрипции, GATA-4, ТВХ5 и NKX2-5, мутировавшие у некоторых пациентов с ДМЖП и ДМПП, связаны друг с другом и совместно регулируют экспрессию генов-мишеней, необходимых для правильного развития сердца. Следует отметить, что GATA-4 и ТВХ20 являются мутантными в случае редких видов кардиомиопатии, возникающих у взрослых (см. далее), указывая на то, что эти факторы транскрипции не только играют важную роль в развитии, но и необходимы для поддержания функции сердца в постнатальном периоде.
Другие мутации одиночных генов, ассоциированные с врожденными пороками сердца, изменяют свойства белков сигнальных путей или выполняющих структурную функцию. Мутации генов, кодирующих различные компоненты Notch, например JAGGED 1, NOTCH 1 и NOTCH2, ассоциируются с различными врожденными пороками сердца, включая двухстворчатый аортальный клапан (NOTCH 1) и тетраду Фалло (JAGGED1 и NOTCH2). Мутации фибриллина лежат в основе синдрома Марфана, ассоциированного с дефектами клапанов и аневризмами аорты. Первоначально фибриллин был описан как структурный белок, однако он служит также важным регулятором TGF-b-сигнализации, усиление которой ответственно, по крайней мере частично, за аномалии сердечно-сосудистой системы при синдроме Марфана.
Характерным примером небольшой хромосомной аномалии как причины врожденных пороков сердца может служить делеция хромосомы 22q11.2, которую имеют до 50% пациентов с синдромом Ди Джорджи. При этом синдроме нарушается развитие 4-й жаберной дуги и производных 3-го и 4-го жаберных карманов, связанных с образованием тимуса, околощитовидных желез и сердца. Геном-кандидатом в делетированной области является ТВХ1, кодирующий фактор транскрипции, который регулирует экспансию клеток-предшественников во второе поле сердца. Другие генетические аномалии, играющие важную роль в развитии врожденных пороков сердца, — это хромосомные анеуплоидии, в частности при синдроме Тернера (моносомия X) и трисомиях по 13, 18 и 21-й хромосомам.
Наиболее частой генетической причиной врожденных пороков сердца служит трисомия по 21-й хромосоме (синдром Дауна), при которой 40% пациентов имеют порок сердца (один или несколько), чаще поражающий структуры, развивающиеся из эндокардиальных подушек (т.е. АВ-перегородки и АВ-клапаны). Механизмы, посредством которых анеуплоидия приводит к развитию врожденных пороков сердца, еще недостаточно изучены, однако возможна нерегулируемая экспрессия множества генов.
Наряду с этими известными ассоциациями развитию врожденных пороков сердца также способствуют менее выраженные формы генетических вариативностей. Такое утверждение отчасти основано на том факте, что родственники первой линии больных имеют повышенный риск врожденных пороков сердца по сравнению с общей популяцией. Так, для ребенка от отца с ДМЖП риск равен 2%, если же ДМЖП имеет мать, риск для потомства составляет от 6 до 10%.
Следует признать, что наши знания о механизмах развития пороков сердца все еще находятся в зачаточном состоянии. У большинства пациентов генетические факторы риска не определены, а если они и установлены, то природа и тяжесть дефекта сильно варьируют. В результате предполагают, что экзогенные факторы, сами по себе или в сочетании с генетическими факторами, также способствуют развитию врожденных пороков сердца и в некоторых случаях могут стать их главной причиной. Примерами служат врожденная краснуха, сахарный диабет у матери во время беременности и действие тератогенов (включая некоторые лекарства). Большой интерес представляют некоторые пищевые факторы, способные влиять на риск развития пороков сердца. Например, употребление поливитаминных добавок, содержащих фолаты, может снизить риск развития врожденных пороков сердца.

- Рекомендуем ознакомиться со следующей статьей "Клиника врожденного порока сердца"
Оглавление темы "Патогенез болезней сердца":- Строение сердца и его физиология
- Возрастные изменения сердца
- Общие механизмы развития болезней сердца
- Механизмы развития (патофизиология) сердечной недостаточности
- Механизмы развития (патофизиология) гипертрофии сердца
- Механизмы развития (патофизиология) левожелудочковой сердечной недостаточности
- Механизмы развития (патофизиология) правожелудочковой сердечной недостаточности
- Механизмы развития (патофизиология) врожденных пороков сердца
- Клиника врожденного порока сердца
- Механизмы развития (патофизиология) дефекта межпредсердной перегородки (ДМПП)

