Иммунодепрессия при опухолях. Торможение иммунитета опухолями
Иммунодепрессия может предшествовать развитию опухоли и усугубляться под действием растущей опухоли [Pontieri G. М. et al., 1988]. Имеются наблюдения развития злокачественных опухолей у больных с иммуносупрессивными состояниями — с ВИЧ-инфекцией, лекарственными, химическими и врожденными иммунодефицитами. Так, около 5% больных врожденными иммуноде-фицитами заболевают раком [Cotran R. S. et al., 1989]. У больных иммунодефицитами чаще развиваются лимфомы, рак кожи и губы.
Однако и сама опухоль может вызвать состояние иммунодепрессии, поскольку известно, что клетки многих опухолей способны выделять простагландины и лейкотриены, вызывающие развитие функционального дефицита иммунной системы [Pontieri G. М. et al., 1989]. Опухолевые клетки не только сами способны синтезировать метаболиты арахидоновой кислоты, но и потенцируют синтез этих веществ клетками иммунной системы — макрофагами, В- и Т-лимфоцитами. Под действием лейкотриенов и простагландинов, выделяемых мигрирующими макрофагами, нарушается дифференцировка тимоцитов (в основном в Т-супрессоры). Вилочковая железа подвергается инволюции, тимоциты мигрируют в другие органы и мозговое вещество.
Подавляется иммунный ответ не только на опухолевые антигены, но и на другие антигены, например на эритроциты овцы. Совершенно ясно, что опухолевый рост сопровождается прогрессирующим, генерализованным антигеннеспецифическим иммунодефицитом.
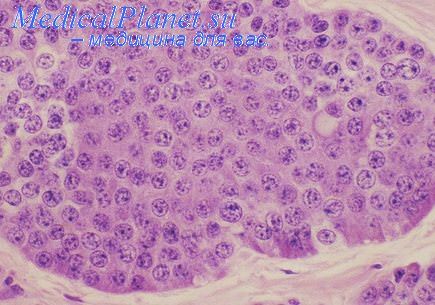
Аллогенное торможение проявляется в виде гибели клеток одного вида под действием клеток другого вида. На опухолевые клетки этот феномен не распространяется. Эти клетки, находящиеся в окружении нормальных клеток, продолжают расти. Предполагают, что отсутствие аллогенного торможения, так же как и контактного, связано с редукцией в опухолевых клетках щелевидных межклеточных контактов.
Это непонятным образом связано с активацией опухолевого промотора транскрипции ТРА, а также с уменьшением количества лектинов на поверхности опухолевых клеток [Weinberg R. А., 1989]. Аллогенное торможение в опухолевых клетках может также нивелироваться мощными митогенетическими сигналами, исходящими от онкобелков и факторов роста.
Кейлонное ингибирование в нормальных тканях осуществляется за счет продукции кейлонов дифференцированными клетками, обладающими тканевой специфичностью. В настоящее время известно более 10 типов кейлонов (эпидермальный, печеночный, гранулоцитарный, эритроцитарный и др.)- В трансформированных клетках нарушен синтез кейлонов, что может быть одной из причин изменения их дифференцировки [Walter J. В., Israel S., 1987].
Влияние гормонов на опухоль многообразно, зависит от дозы гормона и вида опухоли. Стрессорные гормоны — адреналин, кортизон — блокируют деление опухолевых клеток; адреналин, кроме того, сенсибилизирует трансформированные клетки к антимитотическому действию кейлона Сг. Удаление яичников и гипофиза препятствует развитию рака молочной железы у экспериментальных животных. Эстрогены оказывают противоопухолевое действие при раке предстательной железы, андрогены — при раке молочной железы.
- Читать далее "Влияние опухоли на организм. Системное воздействие опухоли"
Оглавление темы "Склероз и онкология":1. Пневмосклероз как причина рака легкого. Туберкулез как причина рака легкого
2. Рак в очагах пневмосклероза. Рак в рубце
3. Нефросклероз и рак почек. Сморщивание почки как причина рака
4. Морфология нефросклероза. Иммуногистохимия рака почек
5. Микроаденомы почек. Типы клеток опухолей почек
6. Взаимодействие опухоли и организма. Влияние организма на опухоль
7. Иммунный ответ на опухоль. Реакция клеток иммунитета на опухоль
8. Цитокины противоопухолевого иммунитета. ФНО, ИФН при опухолях
9. Иммунодепрессия при опухолях. Торможение иммунитета опухолями
10. Влияние опухоли на организм. Системное воздействие опухоли

