УЗИ в хирургии узлового зоба, рака щитовидной железы и заболеваний околощитовидных желез
В последние десятилетия оперативные вмешательства на ЩЖ и ОЩЖ становятся все менее инвазивными и более прецизионными. С этой целью на дооперационном этапе используют визуализирующие методы высокого разрешения, которые позволяют четко локализовать опухолевый узел и его топографоанатомические соотношения с окружающими тканями. В этой главе будут обсуждены преимущества и недостатки методов визуализации ЩЖ и ОЩЖ в контексте доброкачественных и злокачественных новообразований этих органов. Также речь пойдет о выборе оптимального объема операции на ЩЖ (гемитиреоидэктомия или тиреоидэктомия), ОЩЖ (минимально инвазивная паратиреоидэктомия или двусторонняя ревизия шеи) и показаниях к лимфодиссекции.
Хирургия играет ключевую роль в лечении заболеваний ЩЖ и ОЩЖ. ЩЖ — «glandulae laryngis» — была впервые описана Андреасом Везалием (1514-1564) в 1543 г„ а Юлиус Кессериус (1545-1616) первым изобразил ее в виде типичной подковообразной структуры. С тех пор усилия множества хирургов были направлены на разработку оптимальной оперативной техники резекции ЩЖ для снижения специфических осложнений и смертности.
Известный хирург Теодор Кохер (1841-1917) разработал методику удаления ЩЖ из стандартного шейного доступа и был награжден Нобелевской премией в области физиологии и медицины 1909 г..
а) Хирургические вмешательства на щитовидной и околощитовидных железах. Ниже перечислены хирургические вмешательства на ЩЖ и ОЩЖ.
1. Субтотальная резекция ЩЖ: удаление основной части ЩЖ с двух сторон с сохранением небольших участков. В современной эндокринной хирургии эта операция выполняется крайне редко.
2. Гемитиреоидэктомия: полное удаление одной доли ЩЖ с перешейком.
3. Предельно-субтотальная резекция ЩЖ: полное экстрафасциальное удаление одной доли с перешейком и резекция другой доли с сохранением <5% тиреоидной ткани. Эта операция, по сути, является тотальной тиреоидэктомией, при которой по усмотрению хирурга сохраняют участок паренхимы ЩЖ рядом со связкой Берри или верхним полюсом, что позволяет сохранить кровоснабжение верхней ОЩЖ и менее травматично выделить ВГН.
4. Тиреоидэктомия: полное удаление обеих долей ЩЖ с сохранением жизнеспособных ОЩЖ.
5. Центральная лимфаденэктомия: двустороннее удаление клетчатки и ЛУ центрального отдела шеи (уровень VI). Границы резекции: верхняя — подъязычная кость, нижняя — яремная вырезка, латеральные — ОСА.
6. Боковая модифицированная лимфаденэктомия: футлярнофасциальное иссечение клетчатки с ЛУ уровней IIa-Vb на шее. Границы резекции: верхняя — двубрюшная мышца, нижняя — ключица, латеральная — добавочный нерв, медиальная — ОСА.
7. Минимально инвазивная паратиреоидэктомия: удаление одной ОЩЖ без ревизии зон типичного расположения других ОЩЖ. Локализацию пораженной ОЩЖ устанавливают при помощи топических методов диагностики до операции, а финальный объем операции — при помощи интраоперационного мониторинга уровня ПТГ.
Стандартная ревизия шеи: двусторонняя ревизия шеи. Применительно к хирургическим вмешательствам на ОЩЖ данный подход используется для поиска и удаления всех увеличенных и гиперфункционирующих ОЩЖ.
Субтотальная паратиреоидэктомия: удаление трех ОЩЖ и большей части четвертой ОЩЖ при мультифокальном первичном поражении или вторичном гиперпаратиреозе.
Ниже указан список операционных осложнений.
Осложнения операций на щитовидной и околощитовидных железах:
1. Общие осложнения:
- Раневая инфекция
- Ларинготрахеальный отек
- Кровотечение
2. Специфические осложнения:
- Повреждение возвратного гортанного нерва
- Повреждение верхнего гортанного нерва
- Повреждение лимфатических протоков - Гипопаратиреоз
- Тиреотоксический криз
б) Планирование хирургического вмешательства:
1. Стандартные методы визуализации. Перед выполнением хирургического вмешательства необходима исчерпывающая визуализация всей ЩЖ, а также центральных и боковых зон шеи при помощи методов лучевой диагностики. При обследовании по поводу доброкачественных заболеваний методы лучевой диагностики позволяют выявить тиреоидит, реактивные изменения ЛУ, увеличение ОЩЖ, а также аномалии правой подключичной артерии и сопутствующие злокачественные новообразования.
Рак ЩЖ характеризуется высокой частотой метастазирования в регионарные ЛУ, однако физикальное обследование недостаточно чувствительно для выявления пораженных ЛУ, поэтому в этом случае также необходимо обследование при помощи методов лучевой диагностики.
Для первичного исследования ЩЖ методом выбора является УЗИ. Несмотря на зависимость от квалификации врача, выполняющего это исследование, оно неинвазивное и недорогое. УЗИ позволяет не только исследовать характеристики изучаемого узла, но и выявлять новообразования в контрлатеральной доле, определять их размер и локализацию, а также выявлять наличие инвазии опухоли в капсулу ЩЖ и прорастание за ее пределы. Общая точность УЗИ составляет 67% и 71,3% в отношении стадирования рака ЩЖ по параметрам Т (размер и инвазивность первичной опухоли) и N (статус регионарных ЛУ) соответственно.
При этом УЗИ-ТАБ лимфатических узлов, подозрительных на наличие метастазов по результатам УЗИ, следует проводить только в том случае, если результат может изменить тактику лечения. При подозрении на прорастание опухоли за пределы капсулы ЩЖ либо местнораспространенный рак необходимо провести КТ для исследования областей, плохо визуализирующихся при УЗИ (к примеру, клетчатка и ЛУ VII уровня шеи), а также для выявления прорастания опухоли в прилежащие анатомические структуры, в том числе пищевод и трахею.
2. Тонкоигольная аспирационная биопсия узлов щитовидной железы под контролем ультразвукового исследования. В общей популяции узлы ЩЖ встречаются достаточно часто (от 30 до 60% аутопсийного материала). Для того чтобы избежать неоправданных хирургических вмешательств, необходимо дооперационное обследование для выявления узлов, действительно требующих оперативного лечения.
УЗИ-ТАБ — превосходный метод определения, является ли узел злокачественным.
АТА рекомендует выполнять ТАБ узлов ЩЖ преимущественно солидной природы, локализованных по задней поверхности ЩЖ, а также узлов, ультразвуковые характеристики которых подозрительны в отношении злокачественного поражения (гипоэхогенность, наличие микрокальцинатов, повышенная васкуляризация узла, инфильтрирующие края или преобладание переднезаднего размера над шириной в поперечной проекции). При наличии более двух узлов в первую очередь следует выполнить ТАБ наиболее подозрительного узла.
При высоком риске злокачественного поражения ЩЖ (в анамнезе облучение головы и шеи в детском или подростковом возрасте, рак ЩЖ у одного или более родственников первой степени родства, случайная находка при ФДГ-позитронно-эмиссионной томографии (ПЭТ), множественная эндокринная неоплазия 2-го типа или семейная форма медуллярного рака ЩЖ с мутацией RET-онкогена) ТАБ рекомендована независимо от размеров узла.
Повторная ТАБ, предпочтительно под контролем УЗИ, рекомендована при увеличении узла (пальпаторно или по данным УЗИ) в динамическом наблюдении более чем на 50% в объеме, либо более чем на 20% по меньшей мере в двух линейных размерах; минимальное клинически значимое увеличение солидного узла или солидной части смешанного солиднокистозного узла составляет 2 мм. При верифицированном раке ЩЖ по данным ТАБ показана тиреоидэктомия.
3. Интраоперационное ультразвуковое исследование. С помощью интраоперационного УЗИ можно выявлять локальные анатомические особенности и планировать объем оперативного вмешательства. Особенно это актуально при повторных хирургических операциях. УЗИ может быть проведено непосредственно в операционной до начала хирургического вмешательства. При помощи интраоперационного УЗИ можно оценивать распространенность метастатического поражения непальпируемых ЛУ II и Vb уровней шеи. Также под контролем УЗИ можно ввести краситель или локализовать патологический очаг проволочной петлей.
в) Заболевания щитовидной железы:
1. Показания к тиреоидэктомии при доброкачественных заболеваниях щитовидной железы. В связи с высокой частотой осложнений до конца XIX в. тиреоидэктомию выполняли крайне редко. К началу XX в. модификация стратегии хирургических вмешательств на ЩЖ позволила предотвращать развитие послеоперационного гипопаратиреоза и гипокальциемических судорог, что, вместе со значительным улучшением технологий обезболивания, положило начало широкому использованию тиреоидэктомии для лечения доброкачественных заболеваний ЩЖ.
В настоящее время показания к тиреоидэктомии включают не только рак ЩЖ, но и диффузный (БГ) и многоузловой токсический зоб, а также нетоксический зоб при симптомах компрессии прилегающих анатомических структур (рис. 1). В контексте лечения доброкачественной патологии ЩЖ тиреоидэктомия позволяет немедленно и полностью устранить заболевание и избежать повторных хирургических вмешательств. В частности тиреотоксикоз при диффузном токсическом зобе склонен к рецидивированию после консервативного лечения тиреостатиками и радиойодтерапии; в связи с этим тиреоидэктомия как эффективный способ немедленного и полного эли минирования заболевания может рассматриваться в качестве метода выбора при лечении некоторых случаев диффузного токсического зоба.
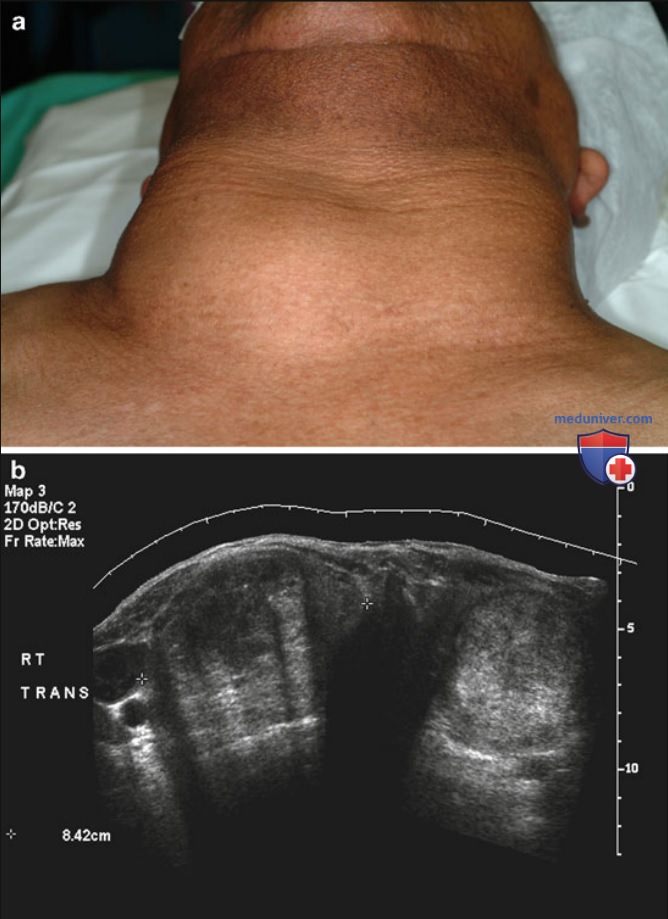
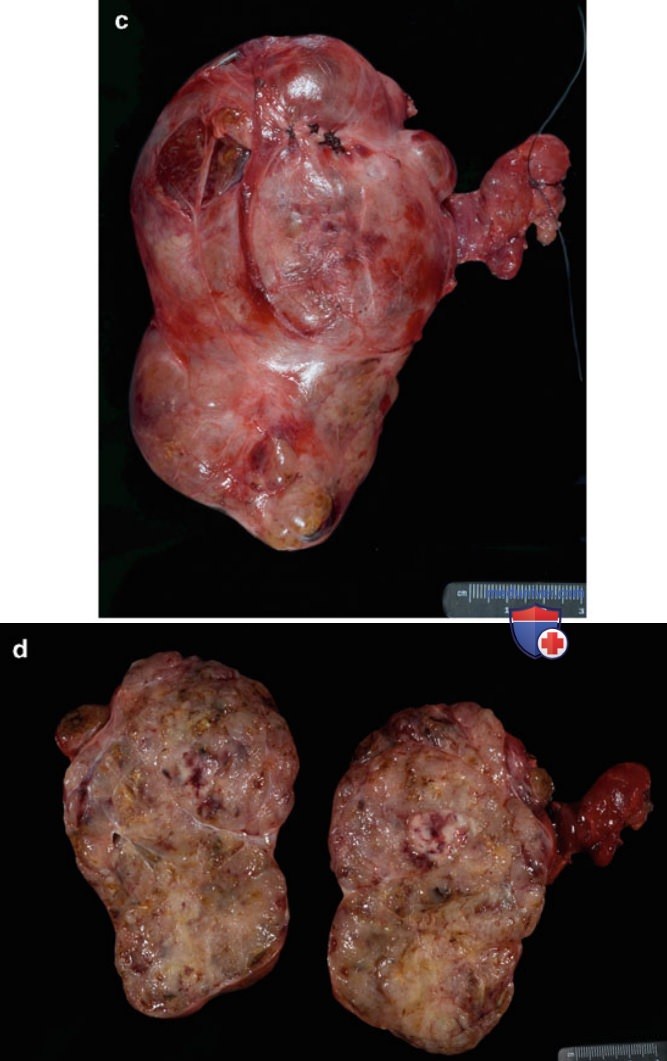
2. Показания к тиреоидэктомии и гемитиреоидэктомии при раке щитовидной железы. Главным преимуществом гемитиреоидэктомии перед тиреоидэктомией является то, что оставшейся доли ЩЖ достаточно для выработки нормального уровня гормонов ЩЖ, что, в свою очередь, позволяет избежать пожизненной заместительной терапии препаратами гормонов ЩЖ. В то же время этот подход неизбежно ассоциирован с риском повторного хирургического вмешательства, если при плановом гистологическом исследовании будет обнаружен рак. В этом случае выполненная в два этапа тиреоидэктомия удваивает риск (остающийся тем не менее достаточно низким) развития гипопаратиреоза и повреждения ВГН по сравнению со стандартной тиреоидэктомией.
Тиреоидэктомия показана пациентам с крупными (>4 см в наибольшем измерении) узлами, демонстрирующими по данным ТАБ выраженную клеточную атипию, цитологическую картину, подозрительную в отношении ПРЩЖ, а также пациентам с отягощенной в отношении рака ЩЖ наследственностью либо с воздействием ионизирующего излучения в анамнезе. Методом выбора в хирургическом лечении верифицированного рака ЩЖ при размере узла >1 см в наибольшем измерении является тиреоидэктомия либо предельно-субтотальная резекция ЩЖ; исключением являются ситуации, когда у пациента имеется повреждение ВГН с контрлатеральной стороны, либо при наличии противопоказаний к общему обезболиванию или антикоагулянтной терапии.
Гемитиреоидэктомия может быть выполнена при солитарных папиллярных микрокарциномах (<1 см в наибольшем измерении) низкого риска в отсутствие клинических и радиологических признаков экстратиреоидного распространения, метастатического поражения шейных ЛУ и при отсутствии в анамнезе облучения головы и шеи.
ТАБ часто используют для определения, является ли подозрительный узел злокачественным (см. выше). Тем не менее около 11% цитологических заключений являются неопределенными. Поскольку частота злокачественных поражений в солитарных узлах с неопределенным результатом биопсии (фолликулярная опухоль или опухоль из клеток Гюртле) может достигать 20%, в этих случаях показана гемитиреоидили тиреоидэктомия.
3. Показания к иссечению лимфатического узла центральной зоны шеи при раке щитовидной железы. Пальпаторное либо сонографическое выявление метастатического поражения ЛУ центральной зоны шеи (уровень VI) является показанием к центральной лимфаденэктомии при тиреоидэктомии. Даже при отсутствии клинических данных за метастатическое поражение ЛУ центральной зоны, при гистологическом исследовании микрометастазы в этих ЛУ обнаруживаются с частотой 30-60%. В связи с этим некоторые хирурги считают, что целесообразно профилактическое иссечение ЛУ центральной зоны.
Подобная тактика является спорной, так как иссечение ЛУ при тиреоидэктомии повышает риск послеоперационного гипопаратиреоза и повреждения ВГН. Эти осложнения могут значительно ухудшить качество жизни пациента, поэтому данное вмешательство рекомендовано только в тех случаях, когда потенциальные преимущества превышают риски. Таким образом, профилактическое иссечение ЛУ центральной зоны не рекомендовано в качестве рутинной процедуры при дифференцированном раке ЩЖ, однако может быть выполнено при уверенности хирурга в безопасном выполнении данного вмешательства у конкретного пациента.
Данная процедура рекомендована для пациентов с верифицированным в процессе дооперацинного обследования медуллярным раком ЩЖ, а также может рассматриваться в отношении пациентов с местнораспространенными (Т3 и Т4) формами ПРЩЖ. Для неинвазивных высокодифференцированных карцином малых размеров (Т1 и Т2), в том числе фолликулярных карцином, без клинических данных за метастатическое поражение ЛУ, методом выбора является операция в объеме предельно-субтотальной резекции ЩЖ либо тиреоидэктомии без центральной лимфодиссекции.
Футлярно-фасциальное иссечение клетчатки с ЛУ бокового треугольника шеи показано при верифицированном биопсией их метастатическом поражении. Профилактическое иссечение ЛУ этой группы ни при каком заболевании ЩЖ не показано.
4. Традиционная открытая тиреоидэктомия. Поскольку профессионализм в хирургии является ключевым фактором, определяющим исход операций на ЩЖ, для снижения риска осложнений ее должен выполнять хирург, имеющий значительный опыт в хирургии ЩЖ. После премедикации и проведения общего обезболивания пациент находится в положении лежа на спине с несколько запрокинутой головой, руки фиксируют вдоль туловища (рис. 2). Проводят поперечный разрез длиной 4-5 см на 2 пальца выше яремной вырезки.
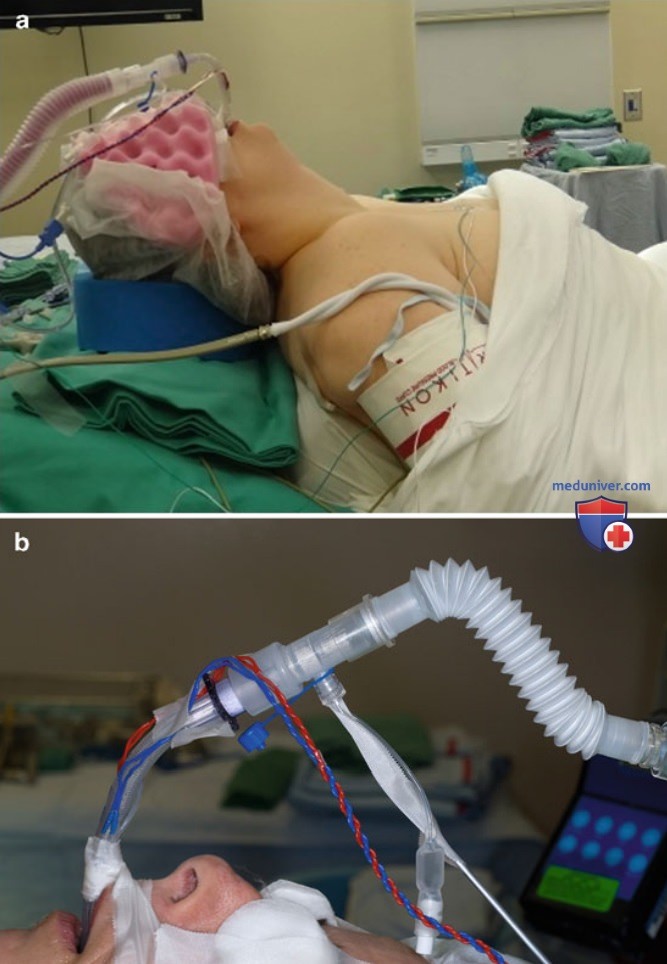
Кожные лоскуты после пересечения платизмы отсепаровывают сверху до нижней границы щитовидного хряща, снизу до яремной вырезки, латерально до медиального края грудино-ключично-сосцевидной мышцы. Претиреоидные мышцы разводят но срединной линии и ревизуют ЩЖ. Выделяют и сохраняют верхние и нижние ОЩЖ вместе с собственными сосудистыми ножками. В трахеопищеводной борозде визуализируют ВГН, его ход аккуратно прослеживают вплоть до вхождения в перстнещитовидную мышцу. Выделяют и отдельно перевязывают нижнюю щитовидную артерию, а также нижнюю и среднюю щитовидные вены. ЩЖ аккуратно отсепаровывают от хрящей трахеи, обращая особое внимание на ВГН.
Верхнюю щитовидную артерию и верхнюю щитовидную вены по отдельности выделяют и перевязывают на входе в паренхиму ЩЖ. ЩЖ мобилизуют медиально от передней поверхности трахеи. При необходимости выполнения тотальной тиреоидэктомии аналогично удаляют контрлатеральную долю. После извлечения удаленной ЩЖ или ее доли операционную рану послойно ушивают рассасывающимся шовным материалом.
5. Роботизированная хирургия щитовидной железы с использованием трансаксиллярного доступа. Роботизированная хирургия ЩЖ с использованием трансаксиллярного доступа — малоинвазивная методика хирургического вмешательства, набирающая популярность в Южной Корее в связи с желанием пациентов избежать видимого шрама на шее. Данный метод является разумной альтернативой для пациентов с подходящими телосложением и размерами ЩЖ, желающих избежать шрама на шее. В настоящее время авторы проводят данное вмешательство только при доброкачественной патологии ЩЖ. Хирургический доступ осуществляется через 5-сантиметровый разрез в подмышечной ямке со стороны удаляемой доли ЩЖ.
После разреза формируют подкожный туннель от латерального края большой грудной мышцы до головок грудино-ключично-сосцевидной мышцы. После отведения подподъязычных мышц обнажают боковую поверхность ЩЖ. После этого применяется робот Да Винчи. Гемитиреоидэктомию проводят в условиях 3D-визуализации и увеличения изображения иссекаемых тканей. Инсуффляцию газом не применяют. Данный метод может использоваться при низкой вероятности злокачественного поражения ЩЖ, размере удаляемой доли <6 см, индексе массы тела <36 и отсутствии в анамнезе хирургических вмешательств на шее.
Общее время роботизированной операции с использованием трансаксиллярного доступа больше, нежели при открытой тиреоидэктомии. Кроме того, разгибание и вынужденное положение руки на стороне операции несет в себе дополнительный риск апраксии. Также подобный подход ассоциирован с повышенным риском развития нарушений кожной чувствительности.
г) Заболевания околощитовидных желез. ПГПТ — распространенная эндокринная патология, диагностируемая в общей популяции с частотой 1-4 случая на 1 тыс. человек. Заболеваемость увеличивается с возрастом. Распространенные проявления ПГПТ — остеопороз, почечнокаменная болезнь, быстрая утомляемость, бессонница, нарушения концентрации внимания и памяти. Наиболее частой причиной ПГПТ является аденома ОЩЖ. Хирургическое удаление аденомы — единственный радикальный метод лечения.
При достаточном опыте хирурга в оперативных вмешательствах на ОЩЖ частота полного излечения превышает 95%. Начиная с первой паратиреоидэктомии, проведенной в США в 1926 г. и вплоть до середины 1990-х гг., методом выбора при лечении опухолей ОЩЖ была стандартная операционная двусторонняя ревизия шеи. Данный метод позволял хирургу осмотреть все 4 ОЩЖ и иссечь ту, которая вызывает наибольшие подозрения в отношении опухолевого поражения. В настоящее время методом выбора является минимально инвазивная паратиреоидэктомия. Широкое распространение малоинвазивных технологий хирургии ОЩЖ стало возможно благодаря трем факторам.
Во-первых, разработка интраоперационных экспресс-методов биохимического анализа крови позволила в режиме реального времени получать информацию о полноте удаления гиперфункционирующей ткани ОЩЖ по быстрому, значительному снижению уровня ПТГ в периферической крови. Во-вторых, общая современная тенденция развития технологий хирургического лечения диктует максимально возможное снижение объема хирургического вмешательства, размера послеоперационного шрама, длительности операции, выраженности послеоперационного болевого синдрома и длительности госпитализации.
Наконец, развитие технологий лучевой диагностики в настоящее время позволяет с высокой точностью определять локализацию аденомы ОЩЖ, что позволяет повысить прецизионность ее удаления и снизить объем операции с тем же функциональным результатом.
1. Определение локализации аденомы околощитовидных желез. Точное определение локализации аденомы ОЩЖ в процессе дооперационного обследования является залогом успешности минимально инвазивной паратиреоидэктомии. Традиционными методами визуализации опухолей ОЩЖ являются УЗИ и сцинтиграфия с технецием (99Тс) сестамиби (Технетрилом). Данный радиофармпрепарат накапливается митохондриями клеток гиперфункционирующей ткани ОЩЖ, позволяя визуализировать аденому ОЩЖ. При благоприятном анатомическом расположении аденома ОЩЖ может быть визуализирована при помощи УЗИ. Дооперационная визуализация позволяет выбрать оптимальный хирургический доступ, а интраоперационный мониторинг уровня ПТГ — зафиксировать момент удаления всей гиперфункционирующей ткани, указывающий на адекватность выполненной операции.
Таким образом, цель операции — безопасное удаление аденомы ОЩЖ с минимизацией объема операции и уменьшением послеоперационного рубца.
Резекция солитарной аденомы ОЩЖ при надлежащей квалификации оперирующего хирурга приводит к полному излечению от ПГПТ в 95% случаев. В то же время этот показатель снижается до 70% при повторной резекции по поводу персистенции гиперпаратиреоза; у 30% повторно оперированных пациентов ремиссии гиперпаратиреоза не наступает, либо заболевание рецидивирует повторно. В связи с этим точная локализация пораженной ОЩЖ до операции является ключевым фактором, определяющим успех хирургического лечения как первичного, так и рецидивирующего заболевания.
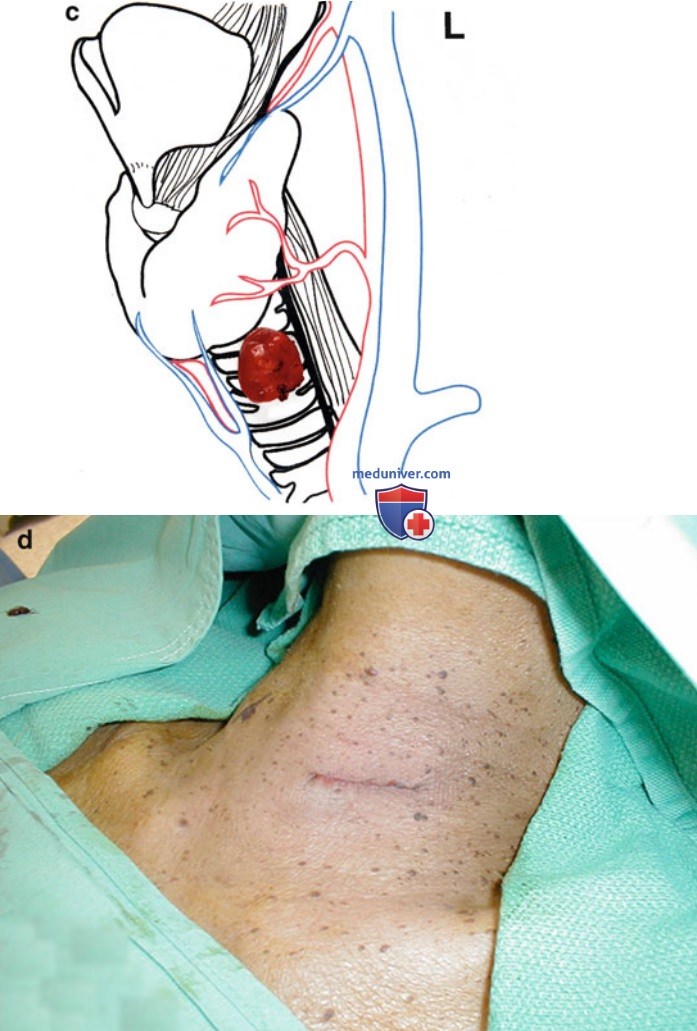
Для улучшения взаимопонимания специалистов различных профилей, участвующих в лечении пациентов с ПГПТ (эндокринологи, радиологи, хирурги и патоморфологи), и исключения неоднозначной трактовки результатов исследований была разработана единая стандартизированная система краткого описания семи типов анатомического положения ОЩЖ (рис. 3).
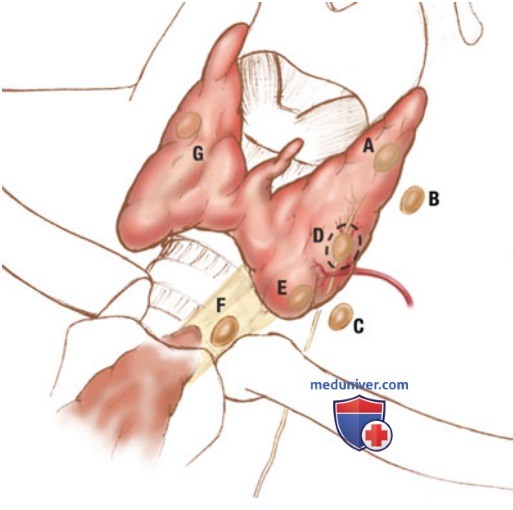
2. Роль тонкоигольной аспирационной биопсии при заболеваниях околощитовидных желез. ТАБ редко является методом выбора для верификации опухолевого поражения ОЩЖ. Обычно отличить ОЩЖ от узла ЩЖ или ЛУ позволяют такие УЗ-характеристики, как размер, особенности локализации и кровотока, наличие сосудистой ножки. Кроме того, топографо-анатомические особенности расположения ОЩЖ могут быть уточнены при помощи сцинтиграфии с технецием (99Тс) сестамиби (Технетрилом) или КТ с контрастированием. ТАБ может осложниться кровоизлиянием или воспалительными изменениями в аденоме, что может затруднить проведение хирургической операции.
В связи с этим авторы не рекомендуют проводить ТАБ в качестве рутинного диагностического метода при заболеваниях ОЩЖ; в отдельных случаях ТАБ может быть выполнена после обсуждения с лечащим врачом-хирургом. При дооперационном обследовании в контексте повторного хирургического вмешательства на ОЩЖ биопсия может быть показана при прогрессировании гиперпаратиреоза, если опухоль ОЩЖ не удается четко визуализировать либо при выявлении методами лучевой диагностики более одного подозрительного образования.
Иммуноцитохимическое исследование биоптатов, полученных в ходе УЗИ-ТАБ, — один из способов верификации тканевой принадлежности узлового поражения ОЩЖ. В то же время в контексте повторных хирургических вмешательств при наличии большого количества рубцовой ткани иммуноцитохимическое исследование менее информативно, поскольку аспират может содержать большое количество клеток фолликулярного эпителия ЩЖ, что может привести к диагностическим и лечебным ошибкам. В таких случаях показано исследование аспирата на ПТГ. Выполнение данного анализа требует предварительного планирования и подготовки. Аспират разводят в 1 мл изотонического раствора хлорида натрия и направляют на исследование. Чувствительность и специфичность данного метода составляют 91% и 95% соответственно.
Высокий уровень ПТГ указывает на паратиреоидный гистогенез аспирированной ткани, низкий — на ткань ЩЖ или ЛУ. Следует отметить, что данное исследование позволяет лишь выявить тканевую принадлежность образования и не способно дифференцировать нормальную, гиперпластическую и опухолевую ткани ОЩЖ.
При дооперационном обследовании по поводу патологии ОЩЖ часто выявляют узловые поражения ЩЖ, подозрительные в отношении злокачественного роста. Поэтому, хотя УЗИ-ТАБ не рекомендована для диагностики заболеваний ОЩЖ, в данном контексте она является ценным дополнительным методом диагностики коморбидной патологии ЩЖ.
3. Минимально инвазивная паратиреоидэктомия. Дооперационная локализация аденомы в определенном квадранте позволяет хирургу тщательно спланировать хирургический доступ и минимизировать объем и длительность операции. Верхние ОЩЖ удаляются боковым доступом, нижние — передним. При боковом доступе выполняют разрез длиной 2 см по медиальному краю грудино-ключично-сосцевидной мышцы (рис. 4). Латеральные края подподъязычных мышц продольно отсепаровывают от грудино-ключично-сосцевидной мышцы. В операционной ране локализуют латеральный край доли ЩЖ, последнюю отводят медиально. На этом этапе аденома ОЩЖ может быть выявлена пальпаторно. При необходимости капсулу ЩЖ аккуратно надсекают. ОЩЖ извлекают после кругового надреза и пересечения сосудистой ножки. На этом этапе требуется особая аккуратность во избежание повреждения ВГН.
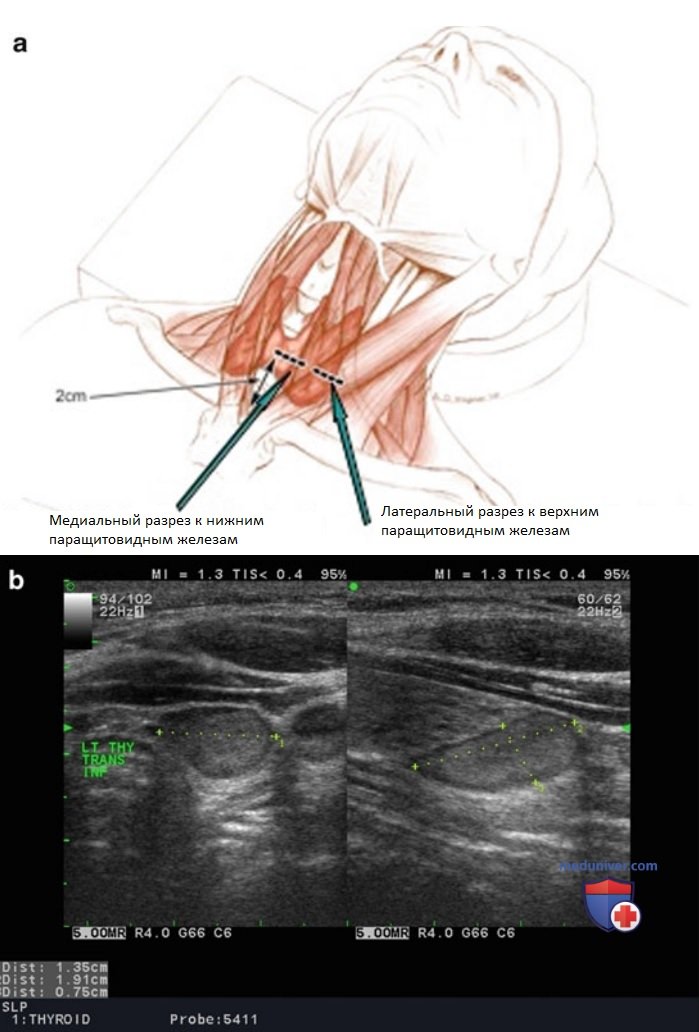
Доступ к нижним ОЩЖ осуществляется через 2-сантиметровый разрез, проведенный от средней линии шеи латерально на стороне пораженной ОЩЖ. Подподъязычные мышцы продольно сепарируют и отводят латерально. Нижний полюс ЩЖ отводят медиально. Аккуратно мобилизуют нижний полюс доли ЩЖ и верхнюю часть щитовидно-тимусной связки. При необходимости рассекают капсулу ЩЖ, аденому ОЩЖ выявляют и иссекают аналогично вышеописанной технике удаления верхних ОЩЖ. Интраоперационное снижение уровня ПТГ в сыворотке более чем на 50% через 5-10 мин после удаления аденомы ОЩЖ указывает на то, что вся гиперфункционирующая ткань ОЩЖ удалена. Следует четко понимать, что основная цель данного анализа — зафиксировать момент удаления всей гиперфункционирующей ткани, указывающий на то, что оперативное вмешательство может быть закончено.
4. Стандартная ревизия шеи. Стандартная ревизия шеи показана пациентам с наследственным, предположительно мультифокальным или вторичным поражением ОЩЖ. Производят разрез длиной 2-3 см кау-дальнее перстневидного хряща. Первые этапы операции аналогичны тиреоидэктомии. После продольного сепарирования подподъязычных мышц проводится рассечение тканей на стороне операции. ЩЖ смещают медиально, осматривают трахеопищеводную борозду. С целью сохранения выявляют ВГН и нормальные ОЩЖ. Нормальные ОЩЖ весят около 30 мг и имеют размер 3x1 мм. ОЩЖ — мягкоэластичной консистенции, цвета арахисового масла.
На данном этапе особое внимание следует уделить сосудистой ножке неизмененной ОЩЖ, чтобы не нарушить ее кровоснабжение. Биопсию неизмененных ОЩЖ не проводят. Аналогичную процедуру проводят с противоположной стороны. В большинстве случаев подобных вмешательств удается обнаружить асимметрично увеличенную ОЩЖ. Для того чтобы отличить измененную ОЩЖ от нормальной, оценивают цвет, контуры, форму, консистенцию и размеры.
Если аденому ОЩЖ не удается найти в типичных расположениях, следует мобилизовать и провести ревизию щитовидно-тимусной связки и верхнего рога тимуса. Если у пациента диагностирован наследственный синдром, проявляющийся гиперплазией и опухолевой трансформацией всех ОЩЖ, удаляют три ОЩЖ с резекцией четвертой. Обязательный этап такой операции — верификация жизнеспособности выбранной для сохранения остаточной ткани ОЩЖ перед иссечением трех остальных ОЩЖ.
д) Резюме. Современная хирургия ЩЖ и ОЩЖ эффективна и безопасна. Залог успеха хирургического вмешательства кроется в мультидисциплинарном подходе и тщательном планировании операции, в котором участвуют радиологи, эндокринологи и патоморфологи. Постановка точного дооперационного диагноза критична для снижения риска послеоперационных осложнений и повторных хирургических вмешательств, а хирург-эндокринолог должен досконально понимать патогенез заболеваний, входящих в круг его профессиональной компетенции.
- Вернуться в оглавление раздела "Ультразвуковое исследование (УЗИ)"
Редактор: Искандер Милевски. Дата публикации: 12.6.2023

