УЗИ лимфатических узлов шеи и их картирование
За последнее десятилетие роль УЗИ в лечении и наблюдении за пациентами с раком ЩЖ значительно повысилась. Метод включен в Рекомендации по ведению пациентов с узловыми образованиями и раком ЩЖ (АТА). УЗИ шеи стало основным исследованием при планировании объема хирургического вмешательства и послеоперационном наблюдении пациентов с раком ЩЖ.
Ключом к определению соответствующего объема хирургического вмешательства и своевременной диагностике рецидива является способность УЗИ выявлять на ранней стадии метастазы в шейные ЛУ.
В этой статье на сайте описаны хирургические уровни и отделы шеи. Очень важно, чтобы эндокринолог, проводящий УЗИ, понимал это деление шеи на анатомические пространства, для того чтобы точно донести УЗ-находки до оперирующего хирурга. Сначала приведены УЗ-характеристики для дифференциальной диагностики доброкачественных и злокачественных изменений ЛУ и как это может подтверждаться с помощью УЗИ-ТАБ. Затем обсуждается метод предоперационной оценки с помощью УЗИ и его возможности для оптимизации операции.
В заключение внимание сосредоточено на том, как УЗИ вместе с определением уровня ТГ эффективно и экономически обоснованно используется для долговременного наблюдения за пациентами, ранней диагностики остаточного и рецидивного рака ЩЖ, а также его метастазов.
а) Хирургические уровни и отделы шеи. Шея является крупной 3D-анатомической структурой. Лимфогенное метастазирование рака ЩЖ имеет тенденцию к распространению в определенные отделы шеи. Из-за этой особенности рака ЩЖ и для облегчения обмена информацией между врачами было введено деление шеи на анатомические уровни, значительно облегчающее предоперационную оценку пациентов с поражением ЛУ Всегда следует помнить о важности точной передачи информации между лечащими врачами, касающейся пространственного расположения патологического ЛУ, для более эффективного проведения операции.
Шея разделена на 7 областей или уровней (рис. 1).
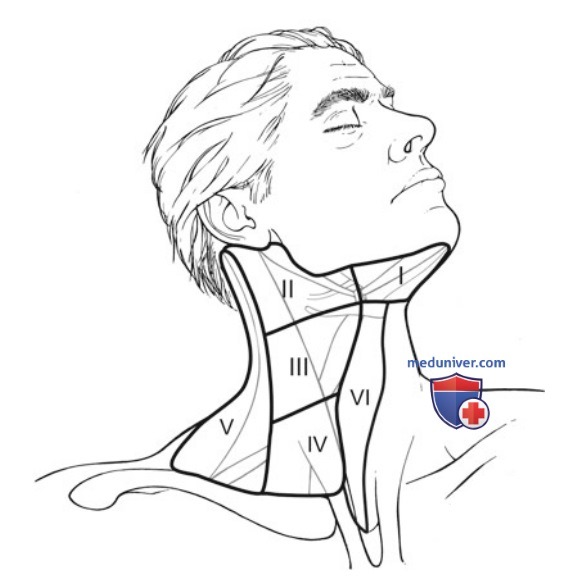
I уровень охватывает ЛУ, расположенные выше переднего и заднего брюшек двубрюшной мышцы, краниально от подъязычной кости и книзу от нижнего края нижней челюсти, и подбородочную группу ЛУ.
II уровень, также известный как верхний яремный, распространяется от основания черепа и добавочного нерва книзу до подъязычной кости. II уровень разделяется на IIА (ниже спинального добавочного нерва) и IIВ (выше спинального добавочного нерва) подуровни.
Средняя яремная группа — это III уровень, распространяется латеральнее сонной артерии, книзу от подъязычной кости до перстневидного хряща.
Уровень IV, или нижняя яремная группа, включает ЛУ по ходу сонной артерии и распространяется от перстневидного хряща книзу до ключицы.
Уровень V имеет треугольную форму, он ограничен задним краем грудинно-ключично-сосцевидной мышцы и передним краем трапециевидной мышцы, подразделяется на подуровни VA выше уровня перстневидного хряща и VB, или надключичную область, ниже уровня перстневидного хряща.
Уровень VI является центральным отделом шеи и разделяется на 4 подгруппы:
- предгортанные ЛУ (группа Дельфиана);
- претрахеальные ЛУ;
- левые паратрахеальные ЛУ;
- правые паратрахеальные ЛУ.
Уровень VII, или верхняя медиастинальная группа, также был описан, но по классификации АТА он включен в нижнюю подгруппу центральных ЛУ шеи для диссекции.
Стандартный протокол лимфодиссекции при ПРЩЖ не включает уровни I, IIВ и V из-за низкой частоты метастазов в них. Исключением из этого правила является выраженная лимфоаденопатия данных уровней, требующая диссекции.
Эти подгруппы ЛУ латеральной и центральной областей шеи дополнительно подразделяются на хирургические шейные блоки для диссекции. В настоящее время в хирургическом лечении поражений ЛУ преобладает отдел-ориентированная диссекция. В результате этого деления на отделы и хирургические подгруппы, как правило, при ПРЩЖ латеральная диссекция ограничивается уровнями II, III и IV, а центральная включает предгортанные, претрахеальные и по крайней мере одну паратрахеальную области (рис. 2).
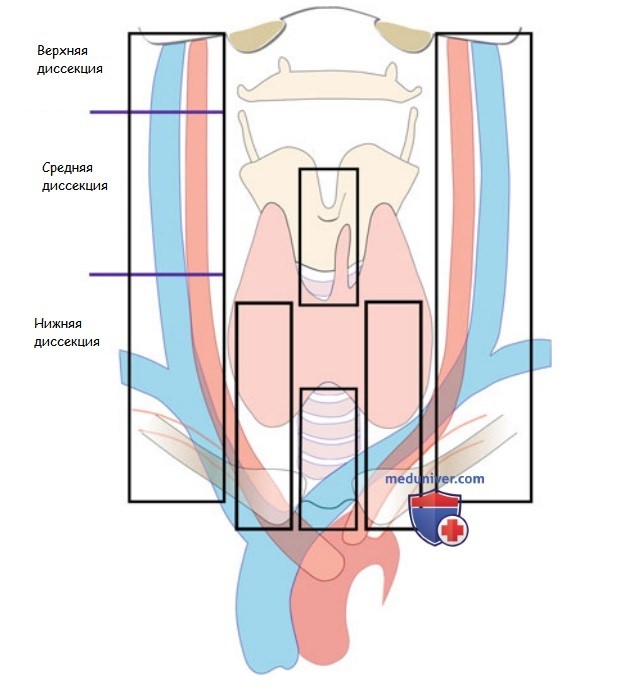
Обратите внимание, в некоторых случаях, особенно у пациентов с агрессивными подтипами рака ЩЖ, может определяться поражение ЛУ вне этих известных уровней шеи. Однако для подавляющего большинства пациентов с метастазами высокодифференцированного рака ЩЖ характерно поражение именно описанных выше уровней.
б) Ультразвуковые признаки доброкачественного и злокачественного поражений лимфатических узлов. В норме на шее находится приблизительно 300 ЛУ. Неизмененные ЛУ обычно имеют уплощенную овальную форму, в большинстве случаев их размер по короткой оси не превышает 0,5 см. Однако они часто увеличиваются при воспалительных процессах. Особенно это касается ЛУ фарингеальной области, где часто видны увеличенные до 0,8 см ЛУ Таким образом, общий размер ЛУ играет малую роль при определении злокачественного или доброкачественного поражения.
Поскольку на начальных стадиях злокачественного поражения ЛУ могут сохранять нормальные размеры или быть увеличены без метастазов, мы должны использовать иные УЗ-критерии для определения характера поражения.
При визуализации ЛУ датчик устанавливают в поперечном положении, измерение проводят по короткой оси (переднезадний размер) и длинной оси (поперечный размер). В норме ЛУ уплощены и имеют соотношение короткая/длинная ось <0,5. При воспалении и гиперплазии они увеличиваются, но обычно сохраняют свою уплощенную форму (соотношение короткая/длинная ось <0,5). При злокачественном поражении ЛУ, как правило, становятся округлыми на поперечных срезах с соотношением короткая/длинная ось >0,5.
Определение размеров на продольных срезах имеет ограниченную практическую ценность, так как в этой проекции доброкачественные ЛУ могут быть вытянуты на несколько сантиметров. Поскольку гиперплазия шейных ЛУ встречается очень часто, вопрос о проведении биопсии следует решать только при размере по короткой оси >0,5 см (0,8 см для I и II уровней) и соотношении короткая/длинная ось >0,5. В остальных случаях показано динамическое наблюдение с интервалом в 6 мес.
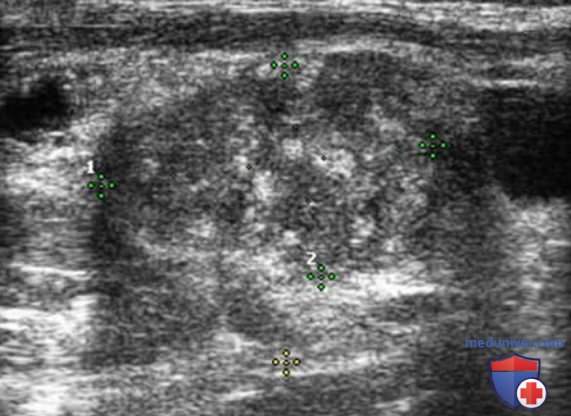
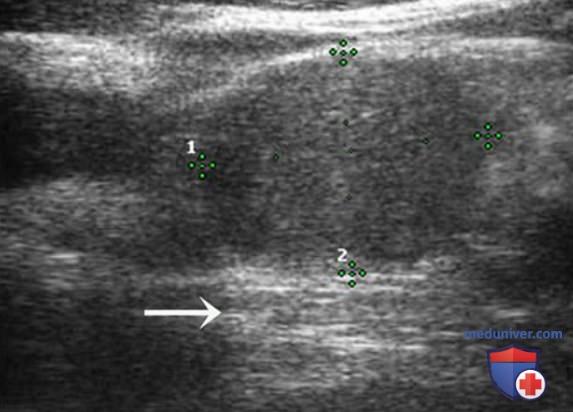
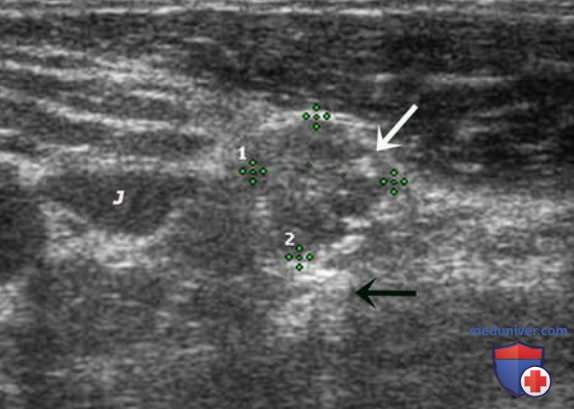
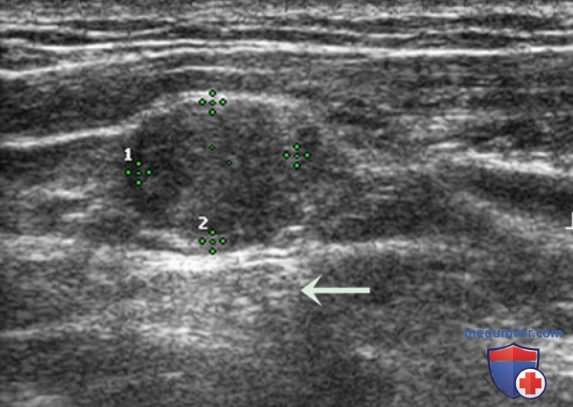
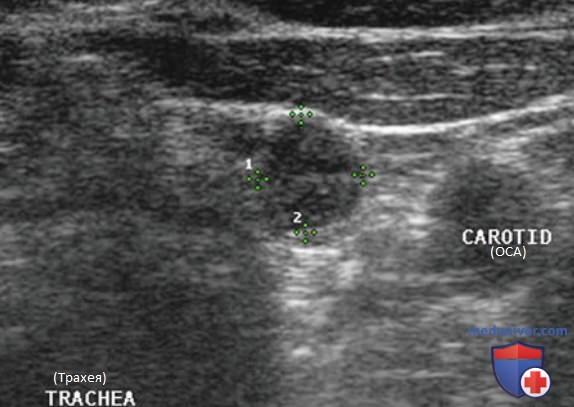
Нормальный ЛУ имеет гипоэхогенный корковый слой, часто видны гиперэхогенные ворота, содержащие жировую ткань и сосуды, создающие линию ворот, которая определяется в большинстве доброкачественных ЛУ с короткой осью >0,5 см и более выражена у пожилых пациентов. При метастазах в ЛУ шеи из ЩЖ или другого происхождения, например, при плоскоклеточном раке или лимфоме, ворота ЛУ определяются редко. Когда УЗИ выполняют пациенту с узловым зобом или раком ЩЖ в анамнезе и повышенным уровнем ТГ, обнаружение ЛУ с размером короткой оси >0,5 см, округлой формы (короткая/длинная ось >0,5) и отсутствием ворот является показанием к ТАБ ЛУ (рис. 3-7).
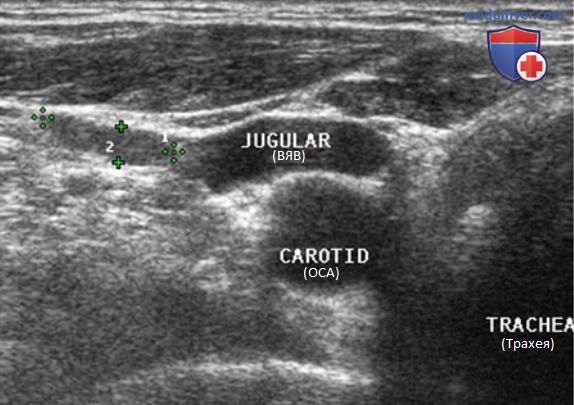
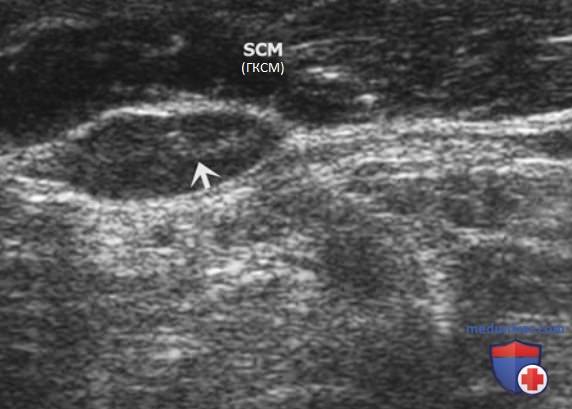
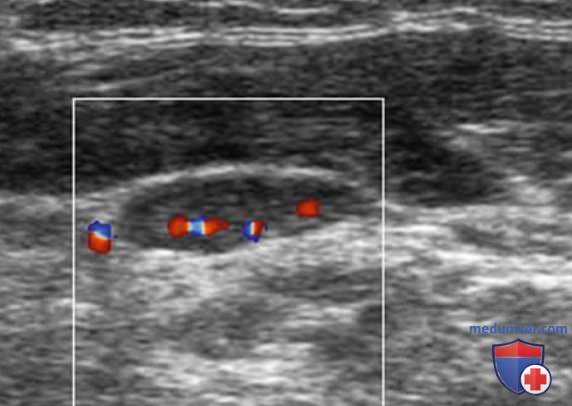
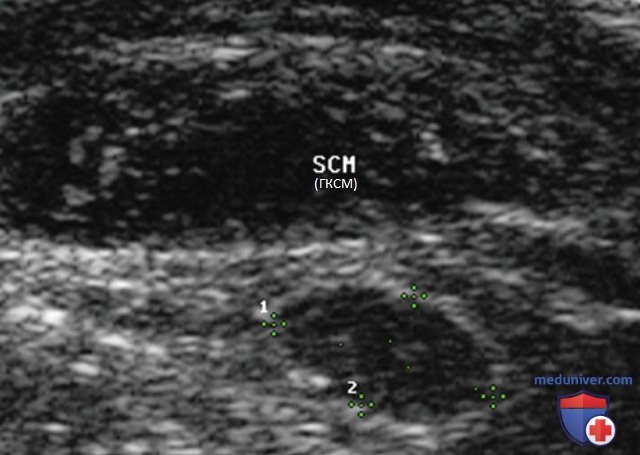
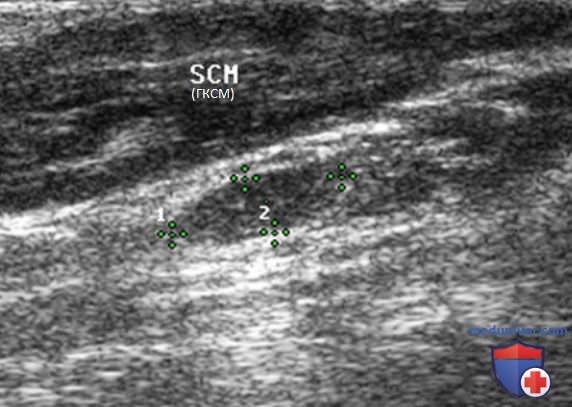
При выявлении других УЗ-признаков (табл. 1) вероятность злокачественного поражения ЛУ повышается. Любая кальцификация, микрокальцификация либо аморфная кальцификация с акустической тенью, является признаком злокачественного поражения. Другим признаком является кистозный некроз ЛУ с задним акустическим усилением. Несмотря на то что кистозный некроз может развиваться и при туберкулезе ЛУ, на Западе он, как правило, наблюдается в ЛУ при метастазах (рис. 8-20).
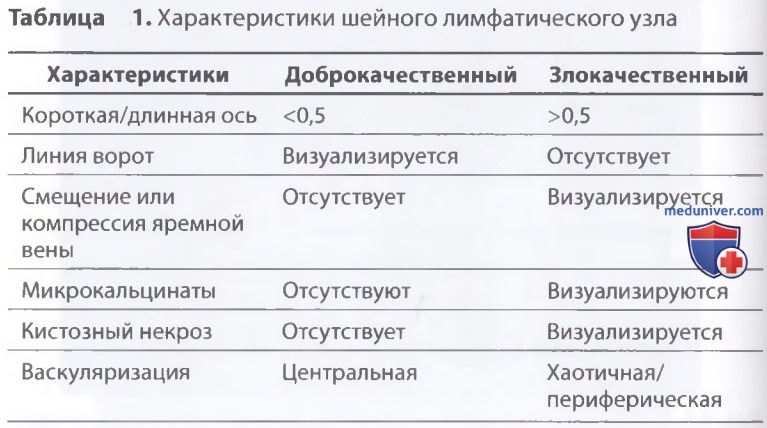
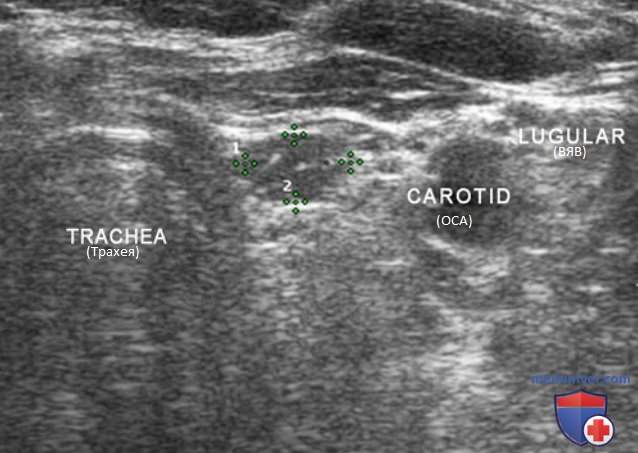
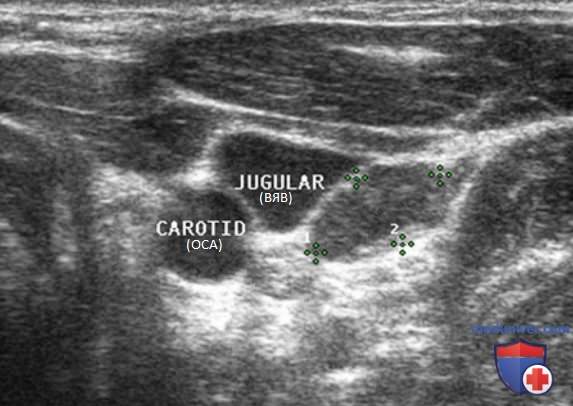
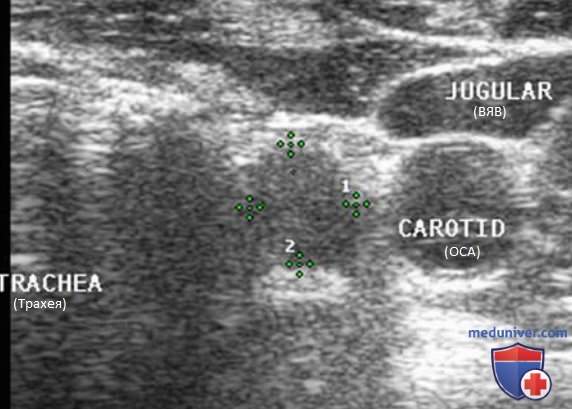
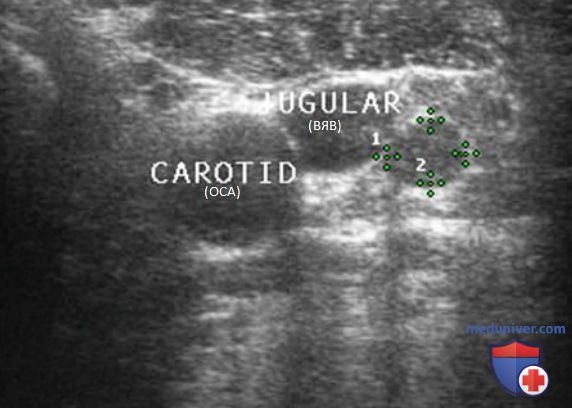
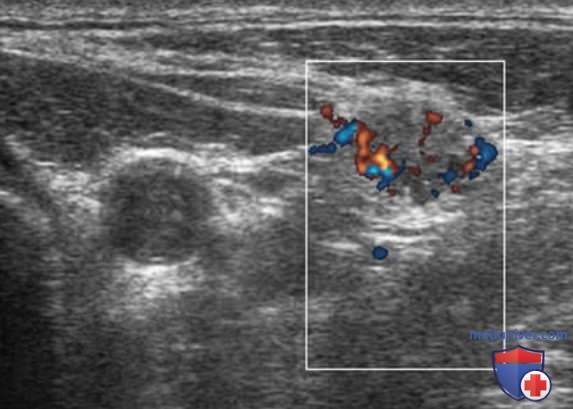
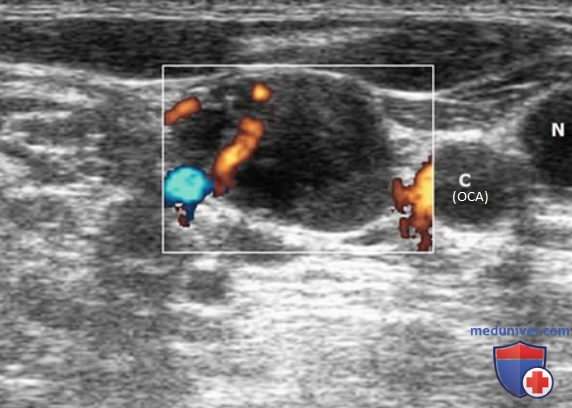
Энергетический допплер предпочтительнее ЦЦК кровотока в исследовании ЛУ, так как этот метод особенно чувствителен к кровотоку в артериолах. В нормальном ЛУ обычно отмечается васкуляризация в области ворот, а метастатически измененные ЛУ часто имеют хаотичную васкуляризацию по всей коре, обусловленную новообразованием сосудов на периферии (рис. 21-25).
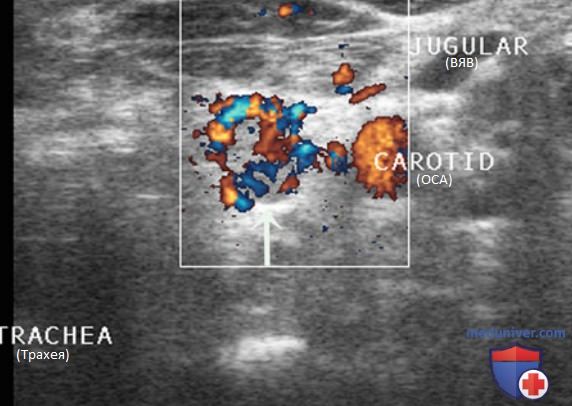
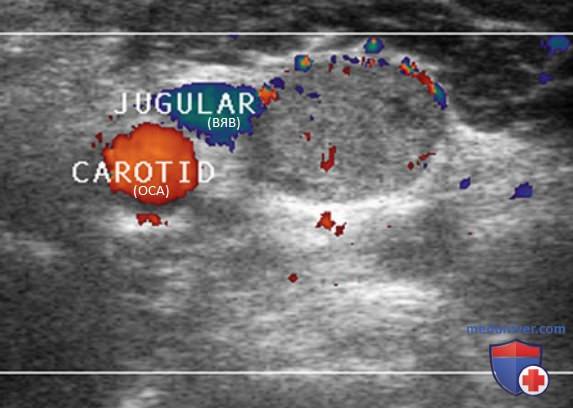
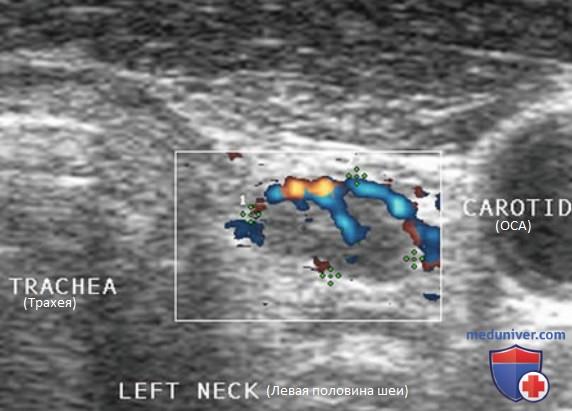
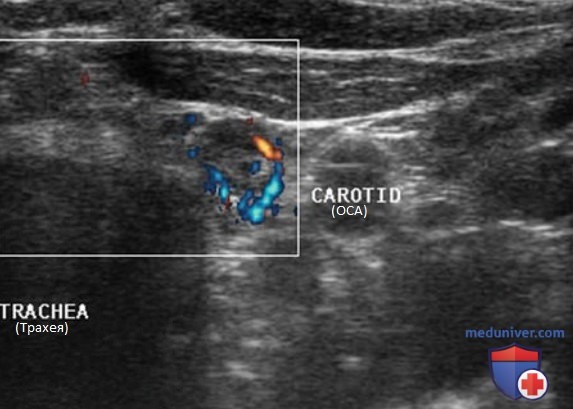
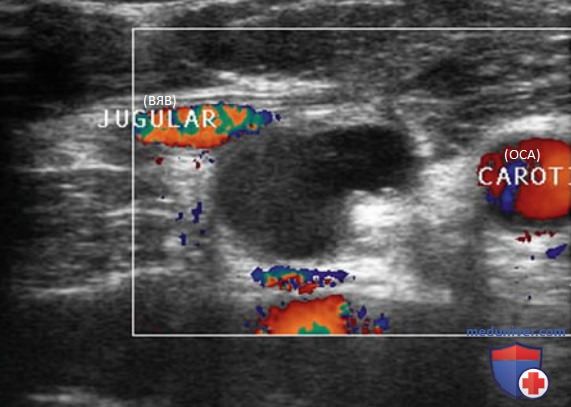
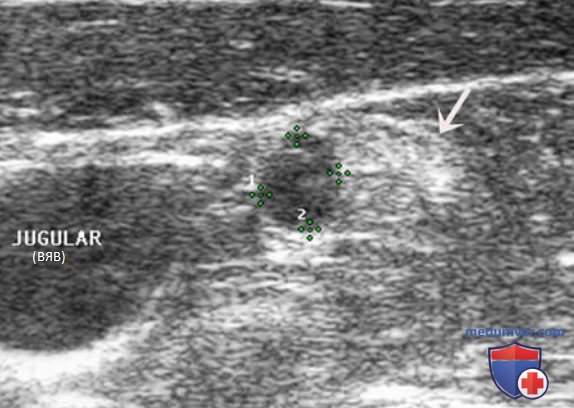
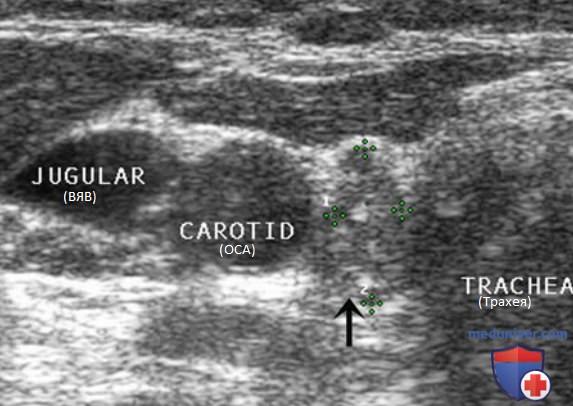
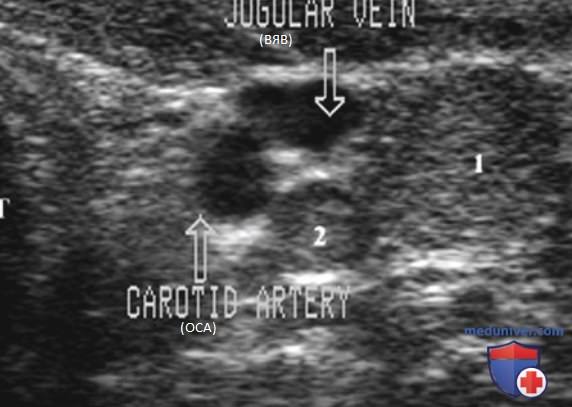
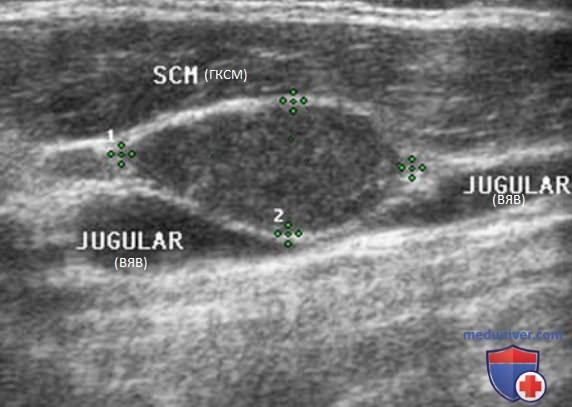
Внутренняя яремная вена (ВЯВ) прилежит к сонной артерии и сопровождает ее. Так как метастатические узлы обычно встречаются в непосредственной близости от яремной вены или сонной артерии, любое отклонение яремной вены от сонной артерии убедительно свидетельствует о наличии ЛУ с метастазом. Иногда необходимо переместить датчик в нескольких направлениях, чтобы выявить подозрительный узел. Следует тщательно осматривать пространство по всей длине сосудов, уделяя особое внимание каждой зоне, где артерия и вена расходятся.
В дополнение к отклонению ВЯВ метастатические ЛУ могут сдавливать вену и приводить к нарушению кровотока. ЦДК кровотока лучше отображает затрудненный кровоток в яремной вене. ЛУ с доброкачественными изменениями редко приводят к отклонению или сдавливанию яремной вены, кроме тех случаев, когда они увеличиваются до очень больших размеров (рис. 26-32).
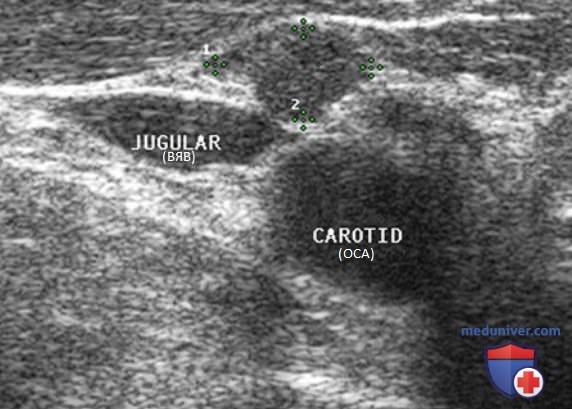
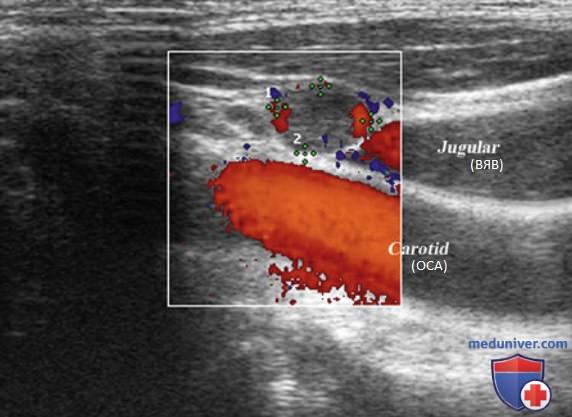
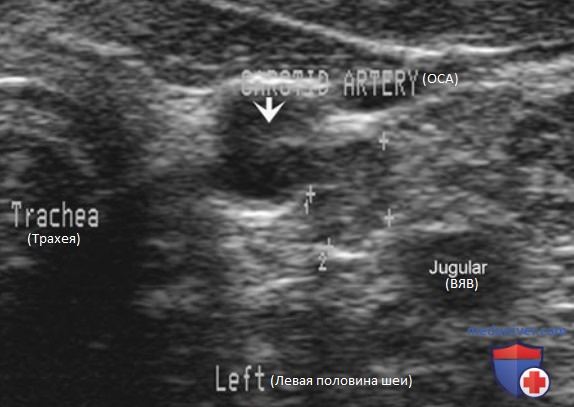
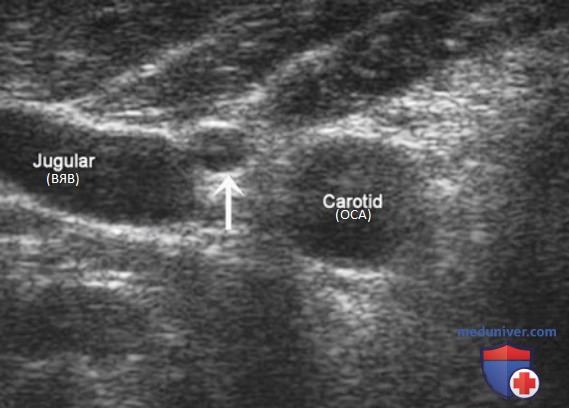
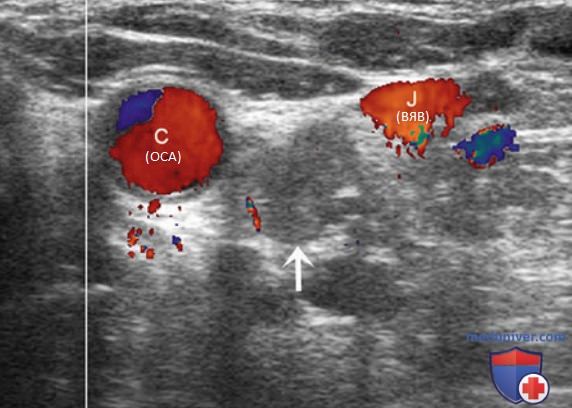
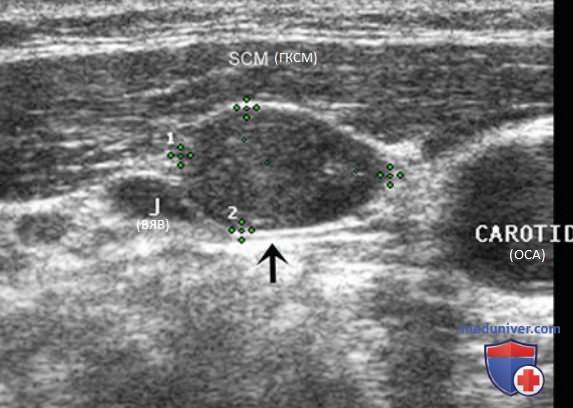
Важно помнить, что УЗ-характеристики, которые помогают при дифференциации доброкачественных и злокачественных образований ЩЖ, могут не подходить для оценки ЛУ. Например, при метастатическом поражении ЛУ могут иметь четкие края вплоть до достижения довольно больших размеров. Хотя злокачественные образования ЩЖ практически никогда не бывают гиперэхогенными, и нормальные, и метастатические ЛУ обычно гипоэхогенные по сравнению с ЩЖ, однако ЛУ с метастазами могут иметь разную эхогенность. Например, иногда ранние метастазы ПРЩЖ бывают плотными и могут быть гиперэхогенными. По достижении ими размера 1 см и развитии кистозного некроза они становятся гипоэхогенными.
В связи с этим эхогенность нельзя использовать в качестве определяющего критерия при решении вопроса о метастазах в ЛУ. При метастатическом поражении ЛУ может становиться матовым, однако это тоже не является достоверным признаком, так как выявляется и при воспалительных процессах или после облучения.
в) Тонкоигольная аспирационная биопсия лимфатических узлов под контролем ультразвукового исследования. Так как УЗИ-признаки метастазов в ЛУ выявляются не всегда, а УЗИ-признаки доброкачественных и злокачественных поражений ЛУ перекрещиваются, перед проведением оперативного вмешательства часто требуется выполнить УЗИ-ТАБ подозрительных ЛУ для постановки окончательного диагноза.
УЗИ-ТАБ ЛУ проводится так же, как и ТАБ узла ЩЖ: с приготовлением мазков из аспирата и их отправкой для цитологического исследования. Цитология ЛУ иногда с трудом поддается интерпретации. Однако метастазы дифференцированного рака ЩЖ содержат ТГ, который можно измерить и использовать как тканевой маркер. После нанесения аспирата на предметное стекло биопсийную иглу промывают 1 мл изотонического раствора хлорида натрия, а смыв направляют на исследование на ТГ. Также на исследование посылают контрольный изотонический раствор хлорида натрия.
Вещество в игле разводится примерно в 100-1000 раз, поэтому ТГ более 10 в смыве с иглы считается положительным анализом на злокачественное образование. Так как внутриклеточный ТГ не подвергается действию циркулирующих в крови анти-ТГ-антител, положительный анализ на анти-ТГ-антитела в сыворотке не влияет на обнаружение ТГ в ЛУ. И положительный результат цитологического исследования, и ТГ в смыве с иглы подтверждают злокачественное поражение ЛУ. Используя и тот и другой методы, Ли (Lee) и соавт. заявили о 100-процентной чувствительности и специфичности обнаружения метастатического рака ЩЖ. В исследованиях было выявлено, что анализ смыва с иглы более информативен, чем цитологическое исследование, при определении злокачественного поражения.
Возможно, это обусловлено малым количеством клеточного материала в ЛУ с кистозным некрозом (см. рис. 9). При подозрении на медуллярный рак ЩЖ в качестве тканевого маркера можно использовать кальцитонин.
г) Предоперационное ультразвуковое исследование и хирургическое лечение. Папиллярный рак ЩЖ — заболевание, для которого характерно метастазирование в ЛУ. Клинически выявляемые узлы подразделяются на выявленные при физикальном обследовании перед операцией, при предоперационной лучевой диагностике или во время операции, их обнаруживают у 35% пациентов с ПРЩЖ. Однако очень маленькие, микроскопические, ЛУ могут определяться у 80% пациентов с ПРЩЖ. Основное прогностическое значение метастазов в ЛУ у пациентов с ПРЩЖ заключается в риске рецидивирования, а не в прогнозировании выживания. У пациентов с ЛУ малого размера частота рецидивирования после прохождения лечения варьирует от 2 до 6%, независимо от иссечения ЛУ или проведения терапии радиоактивным йодом.
Такие микроскопические поражения узлов не имеют большого клинического значения.
В то же время шейные ЛУ, обнаруженные на предоперационном УЗИ (например, клинически явные, макроскопически измененные ЛУ), предполагают более высокий риск рецидивов (>20%), даже при иссечении узлов и/или абляции радиоактивным йодом, чем при клинической стадии N0 или патологоанатомически подтвержденной стадии N1a. Хирургическое лечение ЛУ должно быть ориентировано на выявление и лечение больших, клинически явных, макроскопически измененных ЛУ. В соответствии с рекомендациями по лечению, разработанными АТА, всем пациентам перед операцией по поводу рака ЩЖ следует проводить УЗИ. Учитывая накопленные данные, всем пациентам с ПРЩЖ должно быть проведено картирование ЛУ методами лучевой диагностики для выявления и определения метастатического поражения ЛУ перед операцией (рис. 33, 34).
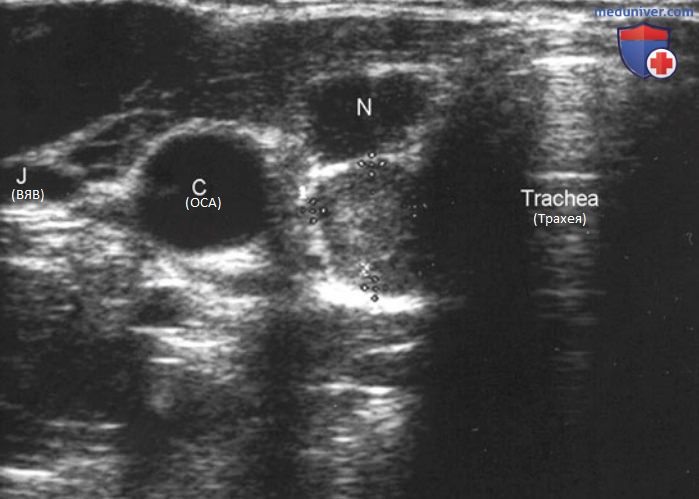
д) Центральная область шеи. Данные о значимости проведения УЗИ центрального отдела шеи перед оперативным вмешательством менее убедительны. Это может быть связано с тем, что в настоящее время большинство хирургов-эндокринологов при тиреоидэктомии чаще всего иссекают ЛУ центральной зоны шеи. Предоперационное УЗИ центрального пространства шеи намного менее чувствительно, чем исследование латеральных отделов, так как даже макроскопически измененные ЛУ могут быть скрыты за ЩЖ. Предоперационная ТАБ ЛУ центрального отдела шеи связана с риском искажения результатов, если игла случайно пройдет через ЩЖ, что приведет к ложноположительным результатам цитологического анализа и/или смыва на ТГ.
По-прежнему рекомендуется проводить УЗИ ЛУ как центрального отдела, так рецидив по данным хотя бы одного исследования. Результаты радиоизотопного сканирования (WBC) оказались положительными у 23 (45%) пациентов, анализ на стимулированный ТГ — у 34 (67%) пациентов, а УЗИ в сочетании с ТАБ — у 48 (94%) пациентов. В связи с тем, что в большинстве случаев рак ЩЖ первоначально метастазирует в ЛУ шеи, очень редко рак распространяется в другие области без вовлечения шейных ЛУ. На основании этих данных считается, что УЗИ шеи — это самый чувствительный из доступных тестов для обнаружения рецидива на ранних стадиях заболевания, даже до повышения уровня ТГ в сыворотке.
Обнаружение и исследование ЛУ следует проводить с помощью УЗИ высокого разрешения, используя датчик с частотой 10-15 МГц и энергетический допплер, позволяющий оценить васкуляризацию. При проведении УЗИ шеи у пациента, перенесшего тиреоидэктомию, можно увидеть, что сонная артерия и яремная вена смещены медиально, ближе к трахее. Если врач не знаком с УЗ-картиной шеи после операции, ему следует начать с исследования пациентов, перенесших тиреоид- или гемитиреоидэктомию по поводу доброкачественного заболевания. Это позволит привыкнуть к измененной анатомии шеи после операции и не беспокоиться о поиске рецидива рака.
После тиреоидэктомии ложе железы заполняется различным количеством гиперэхогенной соединительной ткани, которая при УЗИ выглядит белой (плотной). Это помогает лучше определить рецидив рака или метастатический ЛУ, которые выглядят темными (гипоэхогенными). Описанные выше критерии используются для определения необходимости проведения УЗИ-ТАБ как для цитологического анализа, так и для исследования смыва с иглы на ТГ.
Решение о выполнении диссекции ЛУ после тиреоидэктомии должно быть мультидисциплинарным, обсуждаться эндокринологом и хирургом и, что важно, с участием пациента. Риски, связанные с хирургической ревизией, весьма существенны и включают (но не ограничиваются) одно- или двустороннее повреждение возвратного гортанного нерва (ВГН) с паралитической дисфонией, дисфагией и возможным развитием дыхательных нарушений, а также постоянной формы гипопаратиреоза. Значительный опыт лечения рака ЩЖ и ревизий на шее является важным условием для достижения успешных исходов.
Рецидив рака ЩЖ в центральном отделе шеи может демонстрировать инвазивный рост и прогрессивно ухудшающееся клиническое течение. Однако чаще всего хирургические ревизии ЛУ нацелены не на улучшение выживаемости, а на улучшение лабораторного показателя ТГ. Мы должны быть осторожны, помня о цене, которую может заплатить пациент за это лабораторное улучшение. У операции должны быть четко определенные цели. Рондеу (Rondeau) в недавно проведенном исследовании показал, что рецидив рака в мелких узлах центрального отдела шеи может быть стабильным в условиях подавления тиреотропного гормона даже без проведения любой другой терапии.
В нескольких недавних исследованиях было отмечено, что ТГ может не определяться у 40% пациентов при ревизии ЛУ по поводу ПРЩЖ.
Учитывая изменение анатомии шеи и потребность в точном определении положения ЛУ во время хирургической ревизии, мы исследовали эффективность КТ как дополнение к УЗИ в предоперационной оценке пациентов с рецидивирующим метастатическим поражением и нашли, что комбинация этих методов выявляет макроскопически измененные ЛУ у 27% пациентов, которым была проведена ревизия ЛУ.
Видео УЗИ анатомия шеи
- Рекомендуем ознакомиться далее "УЗИ паращитовидных желез в норме и при патологии"
Редактор: Искандер Милевски. Дата публикации: 12.6.2023

