Хроническая гранулематозная болезнь: причины, клиника, диагностика, лечение
Хроническая гранулематозная болезнь - краткий обзор:
- Группа заболеваний, при которых дефектные промежуточные продукты активного кислорода нарушают внутриклеточное уничтожение микроорганизмов.
- Х-сцепленная или аутосомно-рецессивная форма наследования.
- Мутации в генах, которые кодируют компоненты системы никотинамид-аденин-динуклеотид-фосфат-оксидазы.
- Пневмонии, лимфаденопатия, гепатоспленомегалия и кожные инфекции.
- Гранулемы, чаще всего легких и печени.
а) Эпидемиология. Хроническая гранулематозная болезнь (ХГБ) представляет собой группу Х-сцепленных и аутосомно-рецессивных нарушений. 90% больных являются мужчинами, общая частота распространения составляет один случай на 200000-250000 человек. Х-сцепленная форма наблюдается у 70% больных, симптомы появляются на первом году жизни. Клиническая картина у пациентов с аутосомно-рецессивной формой (30%) развивается в более позднем возрасте и с более легкими проявлениями; у 56% пациентов отмечается недостаточность p47phox остальные случаи представлены дефицитом p22phox и p67phox.
б) Патогенез. Хроническая гранулематозная болезнь (ХГБ) вызывается нарушениями истощенной никотинамид-аденин-динуклеотид-фосфат (НАДФН)-оксидазы — ферментного комплекса, который отвечает за генерацию супероксида. Для нормальной бактерицидной активности после фагоцитоза требуется система НАДФР-оксидазы, которая состоит из НАДФН, нетипичного фагоцита цитохрома b (b558) и цитозольных белков. У пациентов с ХГБ эта мембрано-ассоциированная система НАДФН-оксидазы не может продуцировать супероксид и другие токсические метаболиты кислорода.
До недавнего времени считалось, что лишь оксидативные метаболиты отвечают за уничтожение внутриклеточных организмов. Новая парадигма, открытая для НАДФ-Н запущенного уничтожения микробов предполагает, что оксидативные молекулы выполняют роль внутриклеточных сигнальных молекул, активируя высвобождение первично гранулированных нейтрофильных белков-эластазы и катепсина G- внутри фагоцитированной вакуоли, что, как оказалось, играет важную роль в уничтожении микробов. Данная концепция поддерживает двойную роль НАДФ-Н оксидазы, учитывая и бактерицидный эффект оксидативных метаболитов, и ее способность запускать другие бактерицидные процессы. При Х-сцепленном наследовании мутация находится в CYBB гене, кодирующем gp91phox (оксидазу фагоцита) субъединицу цитохрома b558.
Пациенты с аутосомно-рецессивной хронической гранулематозной болезнью (ХГБ) демонстрируют недостаточность цитозольного фактора НАДФ-Н оксидазы (р47phox или р67phox), и иногда недостаточность р22phox (у-субъединица цитохрома b558), содержащей участок соединения с p47phox. Считается, что цитохром b558 является местом мембранного прикрепления для цитозольных факторов, перемещающихся из цитозоли в плазму мембраны, собирая оксидазные компоненты для активации НАДФ-Н оксидазы.
Необходимо внутриклеточное уничтожение микроорганизмов, вызывающих инфекции у пациентов с ХГБ и обычно являющихся каталазопозитивными. За подавляющее большинство инфекций при ХГБ в Северной Америке и Европе отвечают пять организмов: (1) Staphylococcus aureus, (2) Serratia marcescens, (3) Burkholderia cepacia, (4) Nocardia sp. и (5) Aspergillus sp. Интенсивные гуморальный и гранулематозный ответы при хронической гранулематозной болезни, как полагают, являются компенсаторной сильной, но неэффективной реакцией иммунной системы.
в) Клиника и симптомы. Пиодермии с сочетанной региональной лимфаденопатией и дерматитом, в особенности вокруг ноздрей и ушей, обычно возникают у грудных и иногда у больных неонатального возраста. Стафилококковые абсцессы выявляются у 40% пациентов, в частности в перианальной области. На участках дренирования лимфоузлов или минимальной кожной травмы могут развиваться гнойные воспалительные реакции, они медленно заживают с образованием рубцов. У пациентов с ХГД нередко развиваются хронические воспалительные гранулемы, чаще всего — в легких и печени. Кожные гранулемы являются узловыми и часто носят некротический характер. Гранулемы могут перекрывать жизненно важные структуры, особенно ЖКТ и мочеполового тракта.
У многих пациентов были описаны изъязвления в полости рта, напоминающие афтозный стоматит, хронический гингивит, периоральные язвы, фолликулиты волосистой части кожи головы и себоррейный дерматит. Женщины носители Х-сцепленной ХГД не имеют повышенного риска развития инфекций, но могут иметь кожные элементы, характерные для дискоидной или системной красной волчанки, лимфоцитарной инфильтрации кожи Йесснера, а также афтозный стоматит, гнарулематозный хейлит, фоточувствительность и/или феномен Рейно.
Наиболее частыми экстрадермальными проявлениями являются поражения лимфатических узлов, легких, печени, селезенки и ЖКТ. Гнойный лимфаденит с абсцессом и образованием фистулы обычно поражает шейные лимфоузлы. Пневмония встречается почти у всех больных детей и может вести к формированию абсцессов, кавитации и эмпиемы. Гепатоспленомегалия была зарегистрирована у 80-90% пациентов; более чем у 30% пациентов развиваются абсцессы печени, при этом стафилококковые абсцессы печени являются патогномоничным симптомом ХГБ.
У пациентов с бактериальными инфекциями, а также инфекциями Nocardia sp. заболевание, как правило, протекает с выраженными симптомами, часто отмечаются лейкоцитоз, анемия и повышение скорости оседания эритроцитов (СОЭ). Напротив, отсутствие лихорадки, нормальная СОЭ и незначительные клинические проявления более типичны для инфекций Aspergillus sp. Таким образом, нормальные результаты лабораторных исследований не исключают наличие инфекции у пациента с хронической гранулематозной болезнью. У пациентов нередко выявляются повышение СОЭ, гипергаммаглобулинемия, лейкоцитоз и легкая анемия; иммунные функции обычно не нарушены.
Диагноз хронической гранулематозной болезни основан на результатах исследований продукции супероксида. В настоящее время отдается предпочтение анализу различий Х-сцепленной и аутосомно-рецессивной форм; еще одним количественным методом измерения окислительного всплеска является анализ восстановления феррицитохрома С. Скрининг-тест на ХГБ представляет собой анализ восстановления нитросинего тетразолина (НСТ), при котором желтый НСТ переходит в растворимую окисленную форму (синий формазан) при преципитации с нормальным окислительным метаболизмом. Также могут проводиться количественные НСТ-тесты и хемилюминесцентные исследования. Иммуноблоттинг подтверждает отсутствие компонента гликопротеина 91phox (gp91phox); так как дефицит одного компонента цитохрома b558 ведет к отсутствию другого, при выявлении по данным иммуноблоттинга данного компонента необходимо секвенирование гена gp91phox или p22phox.
Диагностически значимым тестом может считаться иммуноблоттинг, при котором выявлено отсутствие p47phox или p67phox.
В биоптате кожных гранулем выявляются гистиоцитарные инфильтраты, ассоциированные с инородными телами гигантские клетки и накопление нейтрофилов с некрозом. Хотя гистологические признаки волчаночно-подобных кожных поражений у пациентов с ХГБ и носителей могут напоминать таковые у пациентов с волчанкой, иммунофлуоресцентное исследование патологических элементов кожи обычно является негативным.
в) Прогноз, течение и лечение. Пациенты с Х-сцепленной ХГБ, р22phox ХГБ и p67phox ХГБ имеют тенденцию к более тяжелому клиническому течению по сравнению с пациентами с p47phox ХГБ. Средний возраст установления диагноза Х-сцепленной ХГБ составляет 3 года, аутосомно-рецессивной формы — 8 лет. Более чем у 90% пациентов с не-р47phox ХГБ отмечались неопределяемые уровни продукции супероксида. У некоторых пациентов тяжелые инфекции разовьются в грудном возрасте, в то время как у других внезапная тяжелая инфекция, типичная для ХГБ, разовьется в более позднем детском возрасте.
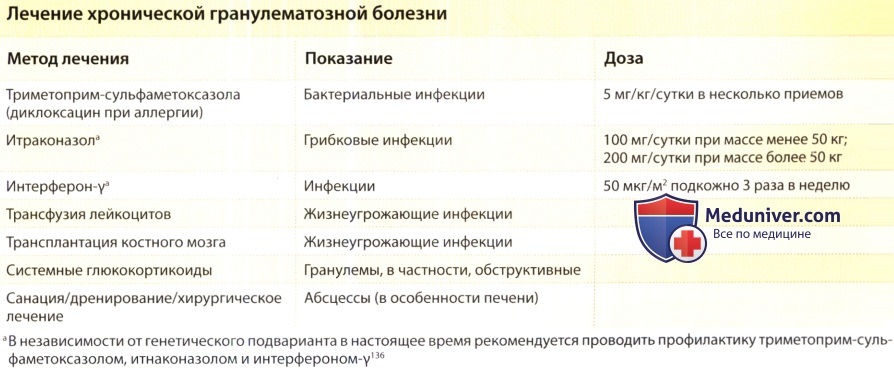
Небольшие очаги локализованного воспаления могут не сопровождаться лихорадкой, и иногда трудны для выявления без тщательного обследования легких, печени и костей при помощи рентгенологических методов, сканирования или ультразвукового исследования. Для выявления возбудителя инфекции должны предоставляться образцы культур, с целью получения адекватных образцов ткани могут потребоваться инвазивные процедуры. Пациенты с признаками инфекции должны получать эмпирическую терапию парентеральными антибиотиками широкого спектра, действующими на S. aureus и грамотрицательные организмы. Внутривенные введения должны продолжаться по меньшей мере 10-14 дней, с последующим курсом пероральной антибиотикотерапии в течение нескольких недель. При более глубоких инфекционных процессах могут потребоваться хирургические вмешательства (дренирование, санация).
Терапия триметоприм-сульфаметоксазолом снижает частоту бактериальных инфекций без повышения частоты грибкового поражения. Для профилактики грибковых инфекций эффективным препаратом является итраконазол. Было показано, что профилактическое назначение ИФН- γ снижает частоту и тяжесть инфекций без повышения частоты хронических воспалительных осложнений как при Х-сцепленной, так и при аутосомно-рецессивной ХГБ. Применение ИФН- γ не сопровождается какими-либо значительными изменениями в активности Н АДФН-оксидазы; его клиническая эффективность связана с повышением функций фагоцитов и уничтожения клеток при помощи неокислительных механизмов.
При быстро прогрессирующих жизнеугрожающих инфекциях применялись трансфузии лейкоцитов. Недавнее исследование показало уровень выживаемости 90% после трансплантации стволовых клеток и, в связи с этим, данная процедура должна проводиться пациентам с подобранными донорами (родственники или нет), а также тем, у кого наблюдаются тяжелые, жизнеугрожающие инфекционные процессы, не отвечающие на другие виды грамотного лечения. При обструктивных гранулемах внутренних органов были эффективны системные глюкокортикоиды. Пренатальная диагностика проводилась при помощи NBT-слайд-теста и в настоящее время также может основываться на молекулярном анализе.
Профилактическое назначение антибактериальных препаратов и ИФН-у снизило смертность от ХГБ примерно до 2% на пациенто-год при аутосомной ХГБ и 5% для Х-сцепленной ХГБ. Наиболее частыми причинами летальности являются пневмония и/или сепсис, вызванный Aspergillus или В. cepacia.
- Рекомендуем далее ознакомиться со статьей "Синдром гипериммуноглобулинемии Е (СГИЕ): причины, клиника, диагностика, лечение"
Редактор: Искандер Милевски. Дата публикации: 26.12.2018

