Механизм развития плоскоклеточного рака кожи (патогенез плоскоклеточной карциномы)
Как мыши, так и крысы чувствительны к индукции плоскоклеточного рака кожи (ПРК) различными химическими и физическими экзогенными факторами, а индукция плококлеточного рака кожи (ПРК) у мышей посредством УФО имитирует патогенез плоскоклеточного рака кожи (ПРК) в коже человека. Многоэтапный химический канцерогенез в коже мышей стал мощным инструментом для описания многих фундаментальных концепций, лежащих в основе эпителиального канцерогенеза в других органах.
Инбредные линии мышей отличаются по чувствительности к индукции опухоли посредством химических канцерогенов и опухолевых промоутеров, а обширный генетический анализ привел к идентификации локусов, от которых зависит чувствительность или резистентность к индукции доброкачественных и злокачественных опухолей. Интересно отметить, что доброкачественные опухоли, которые развиваются у инбредной линии мышей FVB/n, имеют более высокую частоту конверсии в плоскоклеточный рак кожи (ПРК) вследствие полиморфизма в аллели FVB/n Ptch, что усиливает Ras-индуцированное развитие плоскоклеточного рака кожи (ПРК).
Мышиные модели, построенные на основании нарушенной при раке у человека регулировки EG-FR-сигнализации, показывают, что нерегулируемая активация EGFR является важным компонентом формирования кожной опухоли. Выбор в качестве трансгенной эпидермальной мишени TGF-α, который активирует TGFR, может привести к образованию фенотипа доброкачественной опухоли в отсутствие активирующих RAS-мутаций. Однако активация EGFR только путем гиперэкспрессии лиганда—недостаточно активный стимул для автономного формирования опухоли, поскольку многие такие опухоли регрессировали.
Исследования утраты функций также указывают на важную роль EGFR в генезисе плоскоклеточной опухоли кожи. Трансформация Egfr-нулевых кератиноцитов с онкогенными ras при их пересадке иммунодефицитным мышам приводит к формированию доброкачественных опухолей меньшего размера по сравнению с опухолями, развивающимися из контрольных ras-экспрессирующих кератиноцитов. Эти данные предполагают важную роль EGFR-сигнализации в плоскоклеточных опухолях, но указывают на существование альтернативного, ras-индуцированного механизма опухолевого роста в ранних, предзлокачественных опухолях.
Дополнительные данные об усиленном пути сигнализации при плоскоклеточном раке кожи (ПРК) получены в трансгенных исследованиях с применением доминантной SOS, адаптерной молекулы, участвующей в передаче стимулирующих рост сигналов от рецепторных тирозинкиназ типа EGFR, что приводило к спонтанному развитию папиллом в коже мышей. Гиперэкспрессия ErbВ2, рецепторной тирозинкиназы, родственной EGFR и способной с ним взаимодействовать, приводит к спонтанному развитию опухоли кожи у трансгенных мышей.
Инсулиноподобный фактор роста 1 (Igf1) в случае гиперэкспрессии в коже мышей также провоцирует развитие плоскоклеточных папиллом, при этом некоторые из них прогрессируют в карциномы. В то время как в большинстве из этих исследований активируется аутокринный механизм стимуляции роста опухолевых клеток, факторы, генерируемые клетками в опухолевой строме, могут посылать митогенные, а также ангиогенные сигналы кератиноцитам. Дополнительные исследования на мышах предполагают, что специфические компоненты в механизме клеточного цикла, в том числе E2F1, циклин D1, и Cdk4, могут способствовать развитию и/или прогрессии плоскоклеточного рака кожи (ПРК).
Сигнальный путь TGFβ — еще один дополнительный механизм фактора роста, который способствует развитию ПКР, но в отличие от EGFR он функционирует как негативный регулятор эпидермальной пролиферации, поддерживающий гомеостаз эпидермиса. Пониженные уровни межклеточных медиаторов TGFβ-сигнализации, Smad2 и Smad4, наблюдаются при ПКР у человека, следовательно, утрата или разрыв в этом механизме контроля роста играют важную роль для развития опухоли. Интересно отметить, что в случаях плоскоклеточного рака кожи (ПРК) у реципиентов трансплантированных органов, получающих препараты, препятствующие отторжению, отмечается значительная активизация механизма TGFβ.

Следовательно, в этом контексте сигнальный путь TGFβ может повышать восприимчивость к развитию опухоли.
Помимо нарушения регуляции контроля роста при прогрессии плоскоклеточного рака кожи (ПРК) отмечается прогрессивная потеря способности к терминальной дифференциации, что в итоге приводит к образованию опухоли с клетками веретеновидной формы, неотличимыми от злокачественных опухолей, образовавшихся из мезенхимальных тканей. Хотя механизмы, ответственные за нарушение дифференциации на разных стадиях рака кожи человека неизвестны, имеются доказательства того, что нарушение регуляции в семействе ферментов протеинкиназы С (ПКС, РКС) играет роль в нарушении дифференциации кератиноцитов кожи мышей, экспрессирующих онкоген Ras.
РКСδ участвующий в терминальной дифференциации нормальных кератиноцитов эпидермиса, инактивируется в результате фосфорилирования тирозина в ras-трансформированных кератиноцитах. Восстановление РКСδ до его первоначальной формы без фосфорилирования тирозина снимало блокирование терминальной дифференциации в ras-трансформированных кератиноцитах. Кроме того, повышенная экспрессия РКСδ в коже трансгенных мышей подавляет развитие плоскоклеточных папиллом и карцином. Напротив, направленное усиление экспрессии РКСε в коже приводило к формированию менее дифференцированных плоскоклеточных карцином, которые быстро метастазировали в региональные лимфатические узлы.
Необходима дополнительная работа для улучшения понимания механизма, по которому опухолевые клетки при ПРК избегают сигналов, запускающих дифференциацию в нормальные кератиноциты.
Метаболизм простагландина активируется УФО и конституционально индуцируется в плоскоклеточный рак кожи (ПРК) человека, возможно, в результате повышения экспрессии фермента циклооксигеназы-2 (СОХ-2, ЦОГ-2). Хотя механизм влияния изменения обмена простагландинов на рак кожи пока неясен, по-видимому, они вовлечены в промоции опухоли. Активность теломеразы выявляется в значительной части случаев рака кожи у человека, что указывает на то, что эти опухолевые клетки могут избегать старения, а мыши с дефицитом теломеразы резистентны к химическому канцерогенезу.
Дополнительными способствующими канцерогенезу факторами, которые, похоже, участвуют в канцерогенезе, являются медиаторы ангиогенеза, ММП и интегрины, а также другие молекулы, участвующие в адгезии и миграции клеток.
Спонтанное или вызванное канцерогеном образование опухоли у генетически модифицированных мышей позволило выявить гены и пути, которые, по-видимому, играют важную роль в индукции рака кожи, но не были выявлены при изучении наследственных синдромов с развитием рака кожи или при анализе случаев рака кожи человека. Направленное воздействие С-myc на супрабазальный слой у трансгенных мышей позволяет супрабазальным клеткам проходить стадии клеточного цикла и приводит к формированию новообразования с фенотипом папилломы/актинического кератоза, тогда как направленное действие С-myc на базальные клетки не является онкогенным.
Делеция циклин/CDK ингибитора p21, нисходящего эффектора р53, увеличивает число доброкачественных опухолей, но не частоту предраковой прогрессии. Инактивация TGFβ-сигнализации усиливает предзлокачественную прогрессию, в то время как гиперэкспрессия блокирует развитие папилломы и способствует инвазии и метастазам сформировавшихся опухолей и прогрессии плоскоклеточного рака кожи (ПКР) в фенотип веретеноклеточной опухоли. Удивительно, что уменьшение кожного TGFβ1 также подавляет образование папилломы, что указывает на решающую роль физиологических уровней этого фактора роста в поддержке опухолевого роста.
Два фактора транскрипции АР-1 влияют на определенные стадии развития опухоли, на которых для развития папилломы необходим c-Jun, a c-Fos необходим для развития плоскоклеточного рака кожи (ПКР). Подавление активности АР-1 в доброкачественных папилломах предотвращает прогрессию в карциному, и вместо этого превращает эти очаги поражения в доброкачественную аденому сальных желез, что поддерживает концепцию о происхождении плоскоклеточных опухолей из прогениторных клеток с мультилинейным потенциалом. К дополнительным молекулам, которые связывают с развитием ПРК, относятся орнитин декарбоксилаза, p16lnk4a, p15lnk4b, Е-кадгерин, STAT3,C -myc, Notch, α-катенин, ядерный фактор каппа В и Smad3.
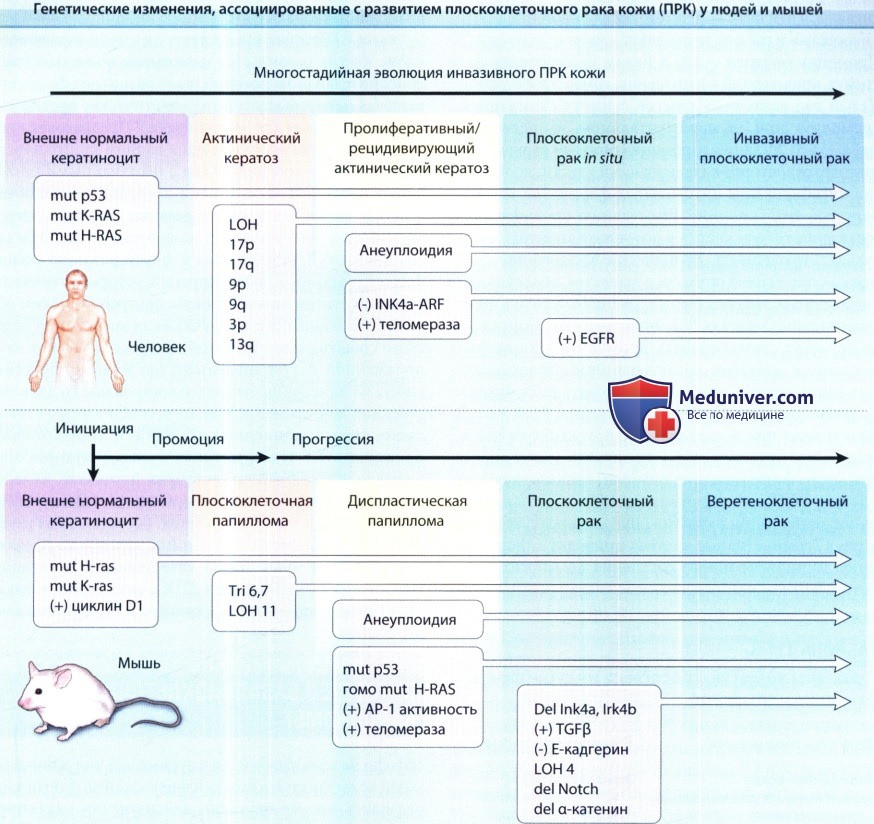
многостадийная эволюция инвазивного ПРК кожи у человека с часто ассоциированными генетическими изменениями.
Мутации одного основания в очагах поражения на ранних стадиях часто характерны для УФ-индуцированного повреждения, тогда как позднее развивающиеся изменения ассоциированы с геномной нестабильностью.
В результате эпигенетических изменений также может развиваться увеличение активности теломеразы (делеция ингибитора) или тирозинкиназы рецептора эпидермального фактора роста (EGFR) (амплификация гена).
При химически индуцированном ПРК кожи многостадийная эволюция в веретеноклеточную опухоль в этой модели является высокоупорядоченным процессом как с временной, так и с генетической точки зрения.
Операционально определенные стадии включают инициацию, промоцию и прогрессию.
Мутация Ras характерна для химических мутагенов, используемых для инициации образования опухоли.
Раннее повышение активности циклина-D1 и позднее повышение активности трансформирующего фактора роста- β1 (TGF- β1), по-видимому, являются важными компонентами канцерогенеза.
Следует отметить, что хотя повреждение р53 выявляется на ранних стадиях развития ПРК человека и при развития УФ-индуцированного ПРК у мышей (не показано), в процессе химического канцерогенеза у мышей мутации р53 возникают на более поздних стадиях.
АР-1 — активирующий белок 1; LOH — потеря гетерозиготности; mut — мутант.
- Рекомендуем далее ознакомиться со статьей "Врожденные и внешние факторы влияющие на прогноз рака кожи (модификаторы канцерогенеза)"
Оглавление темы "Патогенез рака кожи.":- Общие принципы развития рака кожи (патогенез)
- Механизм развития базальноклеточного рака кожи (патогенез базальноклеточной карциномы)
- Механизм развития плоскоклеточного рака кожи (патогенез плоскоклеточной карциномы)
- Врожденные и внешние факторы влияющие на прогноз рака кожи (модификаторы канцерогенеза)
- Новые молекулярные мишени рака кожи используемые для их лечения
- Ультрафиолетовое облучение солнца и солярия как причина рака кожи
- Повреждение ДНК и мутации под действием ультрафиолета как причина рака кожи
- Этапы развития рака кожи вызванного ультрафиолетовым облучением
- Наследственные факторы риска рака кожи от ультрафиолета
- Меры профилактики рака кожи от ультрафиолета (солнца, солярия)

