Схема каскада коагуляции
Каскад коагуляции — третье звено процесса гемостаза. Сигнальные пути схематично представлены на рисунке ниже. В данном разделе обсуждены только основные принципы.
Каскад коагуляции — это существенно усиливающаяся серия ферментных превращений, на каждом этапе которой происходит протеолитическое расщепление неактивного профермента в активный фермент, заканчивающееся образованием тромбина. Тромбин — самый важный фактор коагуляции, участвующий в разных стадиях каскада коагуляции.
В завершение протеолитического каскада тромбин превращает растворимый белок плазмы крови фибриноген в мономеры фибрина, которые полимеризуются в нерастворимый фибриновый гель. Этот гель упаковывает тромбоциты и другие циркулирующие клетки во вторичную гемостатическую пробку, а полимеры фибрина ковалентно связываются и стабилизуются фактором ХШа (который активируется тромбином).
Каждая реакция пути — результат сборки комплекса из фермента (активированного коагуляционного фактора), субстрата (профермента коагуляционного фактора) и кофактора (усилителя реакции). Эти компоненты обычно собираются на фосфорилированной поверхности и удерживаются вместе ионами кальция (с другой стороны, коагуляция предотвращается присутствием хилатов кальция). Непременное условие процесса коагуляции — расположение факторов коагуляции в непосредственной близости друг от друга — с большой долей вероятности указывает на то, что в норме свертывание происходит на поверхности активированных тромбоцитов или эндотелиоцитов.
Каскад коагуляции условно можно назвать «танцами комплексов», в которых факторы коагуляции успешно переходят от одного «партнера» к другому. Связывание факторов коагуляции II, XII, IX и X с кальцием зависит от добавления у-карбоксильной группы к соответствующим остаткам глутаминовой кислоты на этих белках. В этой реакции как кофактор используется витамин К, и она может быть заблокирована такими препаратами, как кумадин, который широко применяют в качестве антикоагулянта.
Каскад коагуляции традиционно делят на внешний и внутренний пути, которые сходятся в точке активации фактора X. Для внешнего пути необходимо участие дополнительного внешнего триггера (первоначально обеспечиваемого тканевыми экстрактами). Для внутреннего пути нужен только фактор XII (фактор Хагемана) на тромбогенных поверхностях. К такому разделению путей пришли в результате проведения тестов in vitro. Фактически существует несколько точек соприкосновения этих двух путей.
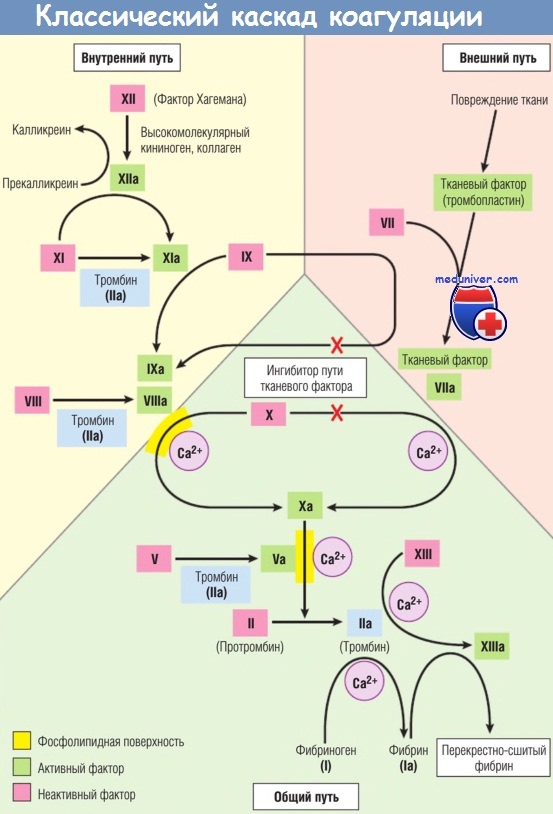
Активация фактора IX возможна как за счет фактора XIа, так и за счет фактора VIIa.
В лабораторных условиях активация фактора IX происходит преимущественно за счет внутреннего пути свертывания, т.е. фактора XIа.
Обратите также внимание на многочисленные реакции, посредством которых тромбин усиливает коагуляцию по механизму положительной обратной связи.
Красными крестами обозначены места активации ингибитора пути тканевого фактора, подавляющего активацию факторов X и IX за счет фактора VIIa.
Более того, внешний путь каскада коагуляции — наиболее физиологически значимый при повреждении сосуда. Этот путь активируется тканевым фактором (также известным как тканевый тромбопластин или фактор III), мембраносвязанным липопротеином, экспрессируемым в местах повреждения.
Состояние двух путей каскада коагуляции оценивают по двум стандартным показателям: протромбиновому времени и частичному тромбопластиновому времени. По протромбиновому времени оценивают функцию белков внешнего пути (факторов VII, X, II, V и фибриногена). Это достигается добавлением тканевого фактора и фосфолипидов к цитратной плазме (цитрат натрия хилирует кальций и предотвращает спонтанную коагуляцию).
Коагуляцию инициируют добавлением экзогенного кальция и фиксируют время, за которое формируется фибриновый сгусток. Частичное тромбопластиновое время отражает функцию белков внутреннего пути (факторов XII, XI, IX, VIII, X, V, II и фибриногена). Коагуляцию инициируют добавлением отрицательно заряженных частиц (например, используя матовое стекло), которые активируют фактор XII (фактор Хагемана), фосфолипиды и кальций и фиксируют время формирования фибринового сгустка.
В добавление к каталитическому действию на последнем этапе каскада коагуляции тромбин оказывает широкий спектр провоспалительных эффектов. Большинство этих эффектов тромбина проявляются после активации им рецепторов, активируемых протеазами, принадлежащих к семейству 7-трансмембранных G-белок-связанных рецепторов. Рецепторы, активируемые протеазами, экспрессируются на эндотелии, моноцитах, дендритных клетках, Т-лимфоцитах и других типах клеток. Активация инициируется расщеплением внеклеточного конца рецептора, активируемого протеазами. В результате образуется привязанный пептид, который связывается с clipped-рецепторами и вызывает конформационное изменение, генерирующее сигнал.
После активации каскад коагуляции должен быть локализован в месте сосудистого повреждения для предотвращения цепной реакции коагуляции по всему сосудистому дереву. Кроме фактора, ограничивающего активацию каскада коагуляции, на фосфолипидной поверхности есть еще три эндогенных антикоагулянта:
(1) антитромбины (например, антитромбин III), которые ингибируют активность тромбина и других сериновых протеаз, включая факторы IXa, Ха, ХIа и ХIIа. Антитромбин III активируется связыванием с гепариноподобными молекулами на эндотелиальных клетках, что обусловливает клиническую значимость применения гепарина для минимизации риска тромбоза;
(2) С- и S-белки, которые являются витамин К-зависимыми белками и работают в комплексе, инактивируя путем протеолиза факторы Va и VIIIa. Активация С-белка тромбомодулином была описана ранее;
(3) ингибитор пути тканевого фактора — белок, продуцируемый эндотелиальными и другими клетками, который инактивирует комплексы тканевого фактора с фактором VIIa.
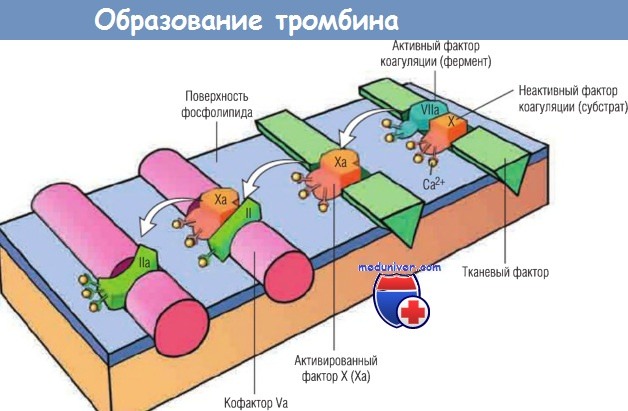
Начальный комплекс реакции состоит из фермента (фактора VIIa), субстрата (фактора X) и кофактора (тканевого фактора), собранных на поверхности фосфолипида тромбоцита.
Для реакции необходимы ионы кальция, которые удерживают собранные компоненты вместе.
Активированный фактор X (Ха) становится частью фермента второго смежного комплекса в каскаде коагуляции,
преобразовывая субстрат протромбина в фактор IIа и используя кофактор Va как усилитель реакции.
Активация каскада коагуляции также запускает каскад фибринолиза, который модерирует размер окончательного сгустка. Фибринолиз обусловливает ферментная активность плазмина, который расщепляет фибрин и запускает его полимеризацию. Образующиеся продукты распада фибрина тоже могут выступить в качестве слабых антикоагулянтов. Повышенные уровни продуктов распада фибрина (в большей степени D-димеры) могут быть использованы при диагностике некоторых состояний: диссеминированного внутрисосудистого свертывания (ДВС), тромбоза глубоких вен нижних конечностей или легочной эмболии.
Плазмин образуется при ферментном катаболизме циркулирующего в крови неактивного предшественника — плазминогена либо по фактор XII-зависимому пути, либо при действии активаторов плазминогена. Наиболее важный среди последних — тканевый активатор плазминогена. Он синтезируется в основном эндотелием и является наиболее активным в присутствии фибрина. Сродство с фибрином делает тканевый активатор плазминогена важным терапевтическим агентом, т.к. он способен в большей степени ограничить фибринолитическую активность в очагах недавнего тромбоза.
Другим активатором плазминогена является урокиназоподобный активатор плазминогена, присутствующий в плазме и других тканях. Он может активировать плазмин в жидкости.
В конечном счете плазминоген может быть расщеплен до плазмина бактериальным ферментом стрептокиназой, которая имеет клиническое значение при определенных бактериальных инфекциях. Активность плазмина, как и других регуляторов, строго контролируется. Для предотвращения бесконтрольного выхода избытка плазмина из растворяемых тромбов свободный плазмин быстро инактивируется ингибитором а2-антиплазмином.
Эндотелиальные клетки так же точно регулируют баланс коагуляции/антикоагуляции путем высвобождения ингибитора активатора плазминогена. Он блокирует фибринолиз, ингибируя связывание тканевого активатора плазминогена с фибрином, и оказывает другие прокоагулянтные эффекты. Образование ингибитора активатора плазминогена повышают тромбин и цитокины, что, возможно, играет определенную роль в тромбозе сосудов при тяжелом воспалении.
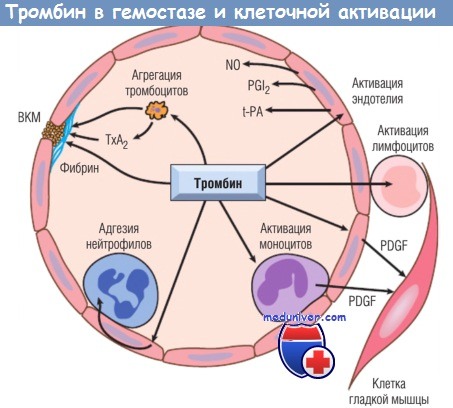
Тромбин играет важную роль в образовании перекрестно-связанного фибрина (путем превращения фибриногена в фибрин и активации фактора XIII).
Посредством рецепторов, активируемых протеазами, тромбин также регулирует несколько клеточных реакций.
Он непосредственно индуцирует агрегацию тромбоцитов и секрецию ТхА2 и может активировать эндотелий для синтеза молекул адгезии лейкоцитов и ряда фибринолитических (t-PA),
вазоактивных (NO, PGI2) и цитокиновых (PDGF) медиаторов. Тромбин также непосредственно активирует лейкоциты.
NO — оксид азота; PDGF — тромбоцитарный фактор роста; PGI2 — простагландин I2;
t-PA — тканевый активатор плазминогена; ТхА2 — тромбоксан А2; ВКМ — внеклеточный матрикс.
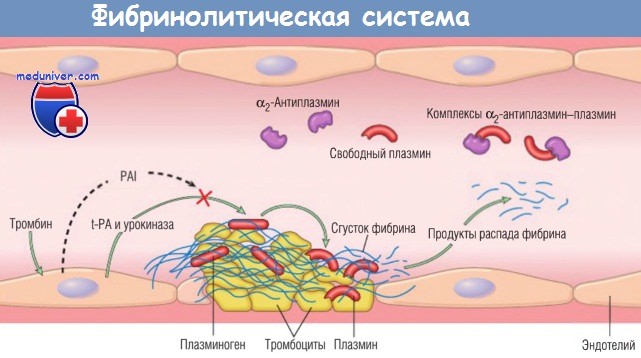
PAI — ингибитор активатора плазминогена; t-PA — тканевый активатор плазминогена.
Видео схема гемостаза - механизмы внешнего и внутреннего пути
- Рекомендуем ознакомиться со следующей статьей "Причины тромбоза и гиперкоагуляции. Триада Вирхова"
Оглавление темы "Патофизиология":- Механизмы фиброза при заживлении раны и ее причины
- Причины и механизмы развития отеков
- Механизмы гиперемии и застоя
- Виды кровотечения и их причины
- Схема гемостаза в норме. Как останавливается кровотечение?
- Участие эндотелия сосудов в гемостазе
- Участие тромбоцитов в гемостазе и их функции
- Схема каскада коагуляции
- Причины тромбоза и гиперкоагуляции. Триада Вирхова
- Синдром гепарин-индуцированной тромбоцитопении как причина тромбоза

