Механизмы развития (патогенез) астмы
Астма — это хроническое воспалительное заболевание дыхательных путей, характеризующееся повторяющимися эпизодами хрипов, одышки, тяжести в груди и кашля, особенно по ночам и/или ранним утром. Симптомы, как правило, обусловлены распространенным, но выраженным в разной степени бронхоспазмом и ограничением воздушного потока. Симптомы частично обратимы (спонтанно или после лечения).
Отличительными признаками этого заболевания являются повышенная чувствительность дыхательных путей к различным стимулам, приводящим к эпизодически повторяющемуся бронхоспазму, воспаление стенок бронхов, увеличение секреции слизи. Некоторые стимулы, вызывающие у больных астмой приступы, оказывают незначительное воздействие или вообще не влияют на пациентов без патологии дыхательных путей. В воспалительном ответе принимает участие множество клеток, в частности лимфоциты, эозинофилы, тучные клетки, макрофаги, нейтрофилы, эпителиальные клетки.
У лиц, длительно страдающих астмой, приступы одышки, кашля и свистящего дыхания, вызванные внезапным бронхоспазмом, могут иметь различную степень выраженности. Редко развивается состояние непрекращающегося бронхоспазма, называемое астматическим статусом, которое может стать фатальным. Между приступами симптомов может практически не быть. В течение последних 40 лет в западных странах зарегистрирован значительный рост заболеваемости астмой.
Астма может быть атопической (при наличии у пациентов повышенной чувствительности к аллергенам, часто с аллергическим ринитом, экземой) и неатопической (без доказанной повышенной чувствительности к аллергенам). При любом типе астмы эпизоды бронхоспазма могут быть вызваны различными триггерами, например респираторной инфекцией (особенно вирусной), раздражающими агентами окружающей среды (например, дымом, специфическими запахами), холодным воздухом, стрессом и физическими нагрузками.
Исследования последних лет показали важность понимания различных вариантов воспаления дыхательных путей — эозинофильного, нейтрофилъного и смешанного. Определяемые в соответствии с этими вариантами типы астмы могут отличаться этиологией, иммунопатологией и ответом на терапию. Астму также классифицируют в соответствии с агентами или событиями, которые вызывают бронхоспазм. Так, выделяют сезонную астму, лекарственную астму, профессиональную астму и астматический бронхит курильщика.
а) Атопическая астма. Этот наиболее распространенный тип астмы является классическим примером IgE-опосредованной аллергической реакции. Заболевание обычно манифестирует в детстве после воздействия экзогенного аллергена, например домашней пыли, пыльцы растений, продуктов жизнедеятельности насекомых, перхоти животных или пищевых продуктов. Типично наличие астмы в семейном анамнезе и положительного кожного теста на раздражающий антиген (реакции гиперчувствительности немедленного типа) с покраснением кожи и образованием волдыря.
Атопическую астму также диагностируют по наличию сенсибилизации к аллергену, установленной с помощью сывороточного радиоаллергосорбентного теста, которым идентифицируют присутствие в организме человека специфических IgE.
б) Неатопическая астма. У больных неатопической астмой нет повышенной чувствительности к аллергенам, и результаты кожных тестов, как правило, отрицательные. В семейном анамнезе астма присутствует редко. Как правило, триггерами неатопической астмы являются респираторные инфекции, вызванные вирусами (например, риновирусом, вирусом парагриппа). У этих пациентов в основе заболевания лежит повышенная реактивность бронхиального дерева. Считается, что вирус-индуцированное воспаление слизистой оболочки дыхательных путей снижает порог чувствительности субэпителиальных вагусных рецепторов на раздражители.
Вдыхаемые с воздухом поллютанты, например диоксид серы, озон и диоксид азота, в некоторых случаях могут внести свой вклад в хроническое воспаление дыхательных путей и повышение реактивности бронхов.
в) Лекарственная астма. Такую астму провоцируют некоторые фармакологические агенты. Аспирин-чувствительная астма — редкий тип, развивающийся у некоторых пациентов с рецидивирующим ринитом и назальными полипами. Эти индивиды чрезвычайно чувствительны к малым дозам ацетилсалициловой кислоты, а также другим нестероидным противовоспалительным средствам. У этих пациентов наблюдаются не только астматические приступы, но и крапивница. Вероятно, у этих пациентов ацетилсалициловая кислота вызывает астму путем ингибирования циклооксигеназного пути метаболизма арахидоновой кислоты, не влияя на липоксигеназный путь, сдвигая реакцию в сторону усиления синтеза лейкотриенов, стимулирующих бронхоконстрикцию.
г) Профессиональная астма. Эту астму вызывают испарения (эпоксидные смолы, пластмассы), органическая и химическая пыль (дерево, хлопок, платина), газы (толуол) и другие химические вещества (формальдегид, производные пенициллина). Приступ астмы способно вызвать незначительное количество химического вещества, но, как правило, после многократного его воздействия. Основные механизмы вариабельны, зависят от агента и включают реакцию гиперчувствительности I типа с выбросом агентов, вызывающих бронхоспазм, и реакцию гиперчувствительности неизвестного происхождения.
д) Патогенез. Основным этиологическим фактором атопической астмы является генетическая предрасположенность к развитию реакции гиперчувствительности I типа (атопической реакции) на воздействие факторов окружающей среды, которые, как правило, остаются неидентифицированными. Установлено, что генетическая предрасположенность к атопической астме проявляется активной реакцией Тн2-клеток на антигены окружающей среды (аллергены), на которые организм большинства людей реагирует слабо или не реагирует совсем. В дыхательных путях развивается сенсибилизация к вдыхаемым аллергенам, стимулирующим индукцию Тн2-клеток.
Тн2-клетки секретируют цитокины, инициирующие воспаление, и стимулируют секрецию IgE и других антител В-клетками. Такими цитокинами являются:
(1) IL-4, стимулирующий продукцию IgE;
(2) IL-5, активирующий местные эозинофилы;
(3) IL-13, усиливающий секрецию слизи бронхиальными железами, а также способствующий выработке IgE В-клетками.
Как и при других аллергических реакциях, IgE фиксируются на поверхности тучных клеток, находящихся в подслизистом слое, и при повторном воздействии аллергена вызывают дегрануляцию тучных клеток с высвобождением содержимого их гранул и секрецию цитокинов и других медиаторов.
Все эти агенты участвуют в развитии ранней фазы аллергической реакции (реакции гиперчувствительности немедленного типа) и поздней фазы аллергической реакции.
Ранняя фаза аллергической реакции характеризуется бронхоспазмом, повышенной продукцией слизи, расширением сосудов и повышением их проницаемости. Бронхоспазм инициируется прямой стимуляцией субэпителиальных рецепторов блуждающего нерва (парасимпатической стимуляцией) посредством механизма центральных и местных нейронных рефлексов (в т.ч. при посредничестве немиелинизированных чувствительных С-волокон).
Поздняя фаза аллергической реакции характеризуется воспалением с лейкоцитарной инфильтрацией, состоящей из эозинофилов, нейтрофилов и большого количества Т-клеток. Накопление лейкоцитов в тканях стимулируется некоторыми цитокинами и хемокинами, выделяемыми тучными и эпителиальными клетками, а также Т-клетками. Эпителиальные клетки, как известно, продуцируют большое количество цитокинов в ответ на инфекционные агенты, лекарственные препараты и газы, а также медиаторы воспаления. Эта вторая волна медиаторов также стимулирует позднюю фазу аллергической реакции. Например, эотаксин, вырабатываемый эпителиальными клетками дыхательных путей, является мощным хемоаттрактантом и активатором эозинофилов.
В свою очередь, главный основной белок эозинофилов повреждает эпителий и вызывает еще большую констрикцию бронхов. В астматический ответ вовлечено множество медиаторов, важность каждого из них оценить сложно.
Медиаторы, предположительно участвующие в патогенезе острого приступа астмы, можно разделить на три группы в соответствии с клиническим эффектом при воздействии ингибиторами или антагонистами медиаторов:
- медиаторы, роль которых в бронхоспазме доказана эффективностью лекарственной терапии:
(1) лейкотриены С4, D4 и Е4 (чрезвычайно мощные медиаторы, вызывающие длительный спазм бронхов, повышающие проницаемость сосудов и увеличивающие секрецию слизи);
(2) ацетилхолин (секретируется внутрилегочными двигательными нервами, которые, непосредственно стимулируя мускариновые рецепторы, могут вызвать спазм гладких мышц дыхательных путей);
- медиаторы, присутствующие в легочной ткани и обладающие выраженными астмоподобными эффектами:
(1) гистамина (мощного бронхоконстриктора);
(2) простагландина D2 (вызывает дилатацию сосудов и бронхов);
(3) фактора активации тромбоцитов (вызывает агрегацию тромбоцитов и высвобождение из их гранул гистамина и серотонина).
Роль этих медиаторов в патогенезе острой аллергической астмы кажется относительно незначительной из-за отсутствия эффекта их потенциальных антагонистов или ингибиторов синтеза. Эти медиаторы могут участвовать в патогенезе хронической неаллергической астмы;
- медиаторы, для которых конкретные антагонисты или ингибиторы не найдены или еще не изучены: многочисленные цитокины, такие как IL-1, TNF и IL-6 (некоторые из этих цитокинов содержатся в гранулах тучных клеток), хемокины (например, эотаксин), нейропептиды, оксид азота, брадикинин и эндотелины.
Таким образом, развитию острой астматической реакции способствует большое количество медиаторов (разных у различных индивидов или при разных типах астмы). Понимание роли клеток и медиаторов воспаления в патогенезе астмы привело к использованию при ее лечении противовоспалительных препаратов, таких как кортикостероиды.
Со временем повторные контакты с аллергеном и иммунные реакции приводят к структурным изменениям в бронхиальной стенке — происходит ремоделирование дыхательных путей. Эти изменения (более подробно см. далее) включают гипертрофию и гиперплазию бронхиальных гладкомышечных клеток, повреждение эпителия, усиление васкуляризации дыхательных путей, гипертрофию/гиперплазию бронхиальных слизистых желез и субэпителиальное отложение коллагена.
Сложные взаимодействия между иммунной системой, эпителием дыхательных путей и мезенхимальными тканями дыхательных путей еще недостаточно изучены. Инфекции дыхательных путей, вызванные такими типичными патогенами, как респираторный синцитиальный вирус и вирус гриппа, могут усугубить изменения и серьезно ухудшить течение заболевания.
Инфекции часто являются причиной астмы, однако некоторые из них, как это ни парадоксально, дают защитный эффект. Эпидемиологические исследования впервые выявили, что заболеваемость астмой была выше в популяциях, не подвергавшихся значительному воздействию микроорганизмов, чем в тех, которые находятся в среде с обильным микробным окружением. Именно этим и объясняется все возрастающая частота аллергических реакций, в т.ч. астмы, в индустриально развитых странах. Так появилась гигиеническая гипотеза, согласно которой устранение инфекции может способствовать аллергическим и другим иммунопатологическим реакциям организма человека, однако объяснить такую связь между инфекцией и астмой пока не смогли.
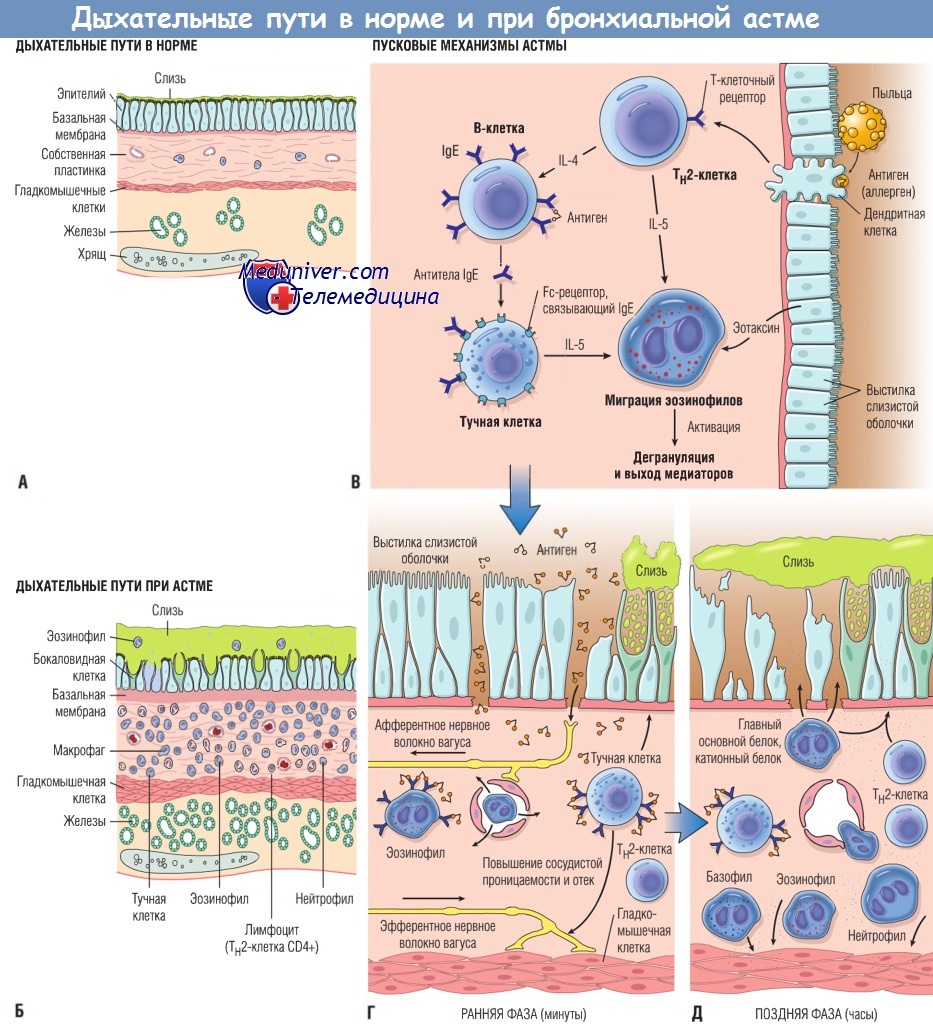
Обратите внимание на скопление слизи в просвете бронха в результате увеличения ее секреции бокаловидными клетками слизистой оболочки
и гипертрофированными подслизистыми железами и выраженное хроническое воспаление с инфильтрацией эозинофилами, макрофагами и другими клетками.
Эпителиальная базальная мембрана утолщена, гладкомышечные клетки гипертрофированы и гиперплазированы.
(В) Ингаляционные аллергены (антиген) вызывают реакцию Тн2-клеток, способствуя продукции иммуноглобулина Е (IgE),
миграции эозинофилов в очаг воспаления и их сенсибилизации.
(Г) При повторном воздействии антигена реакция гиперчувствительности немедленного типа вызвана IgE,
связанными с IgE-рецепторами на тучных клетках. Эти клетки выделяют находящиеся в них медиаторы,
которые, действуя напрямую либо с помощью нейронных рефлексов, индуцируют бронхоспазм, повышение сосудистой проницаемости, выработку слизи и экстравазацию других клеток.
(Д) Миграция в очаг воспаления лейкоцитов (нейтрофилов, эозинофилов, базофилов, лимфоцитов и моноцитов) свидетельствует о начале поздней фазы и выбросе новых медиаторов из лейкоцитов, эндотелиальных и эпителиальных клеток.
Выброс факторов, особенно из эозинофилов (например, главного основного белка, катионного белка), также приводит к повреждению эпителия.
IL — интерлейкин.
е) Генетика. Астма характеризуется сложными генетическими особенностями, которые касаются множества генов, обусловливающих предрасположенность к астме и отвечающих за взаимодействие с факторами окружающей среды, в результате которого развивается патологическая реакция. Как и при других сложных процессах, у каждого индивида существует значительная вариабельность экспрессии этих генов, комбинаций полиморфизмов и их значимости. Среди более 100 генов, взаимосвязь которых с астмой была установлена, лишь некоторые из них широко представлены в популяции. Многие гены влияют на иммунный ответ или ремоделирование ткани, некоторые — на развитие астмы, а другие — на тяжесть течения астмы или реакцию организма пациента на лечение:
- один из наиболее воспроизводимых локусов, связанных с восприимчивостью к астме, расположен на хромосоме 5q вблизи кластера генов, кодирующих цитокины IL-3, IL-4, IL-5, IL-9 и IL-13, а также рецепторы IL-4. В этом месте также располагаются ген рецептора LPS (CD14) и ген, кодирующий b2-адренергические рецепторы. Этот регион представляет большой интерес, поскольку в нем расположены гены, влияющие на механизм регулирования IgE, а также рост и дифференцировку тучных клеток и эозинофилов. Полиморфизм гена IL13 имеет самую сильную и последовательную связь с астмой и другими аллергическими заболеваниями.
Связь атопических реакций с полиморфизмом гена CD14, кодирующего рецептор эндотоксина моноцитов, нуждается в дополнительных комментариях, поскольку раскрывает суть взаимосвязи генотипа с факторами окружающей среды. В некоторых исследованиях генотип ТТ CD 14 ассоциировался со сниженным уровнем IgE и уменьшением риска астмы и других атопических реакций, но другие исследования показали повышенный риск этих реакций. Дальнейший анализ продемонстрировал, что генотип ТТ защищает от астмы или аллергической сенсибилизации при воздействии небольшого количества эндотоксина, но ассоциируется с повышенным риском развития астмы или аллергической сенсибилизации при воздействии большого количества эндотоксина.
Такой эффект может быть обусловлен различным воздействием разных уровней эндотоксина на Тн1-и Тн2-клетки. У лиц с генотипом ТТ и высоким уровнем эндотоксина Тн2-клетки продуцируют большое количество IgE, соответственно предрасположенность к аллергической реакции у таких индивидов выше. Исследования показали, что связь между генотипом и фенотипом является контекстно зависимой, и помогли объяснить некоторые противоречивые результаты, полученные при изучении различных популяций;
- предрасположенность к синтезу антител IgE к некоторым антигенам, например пыльце амброзии, может быть непосредственно связана с HLA класса II;
- ADAM-33 относится к подсемейству металлопротеиназ, связанных с ММР, например с коллагеназами. Точная функция остается неясной, однако известно, что ADAM-33 экспрессируются легочными фибробластами и бронхиальными гладкомышечными клетками. Вероятно, полиморфизм ADAM-33 усиливает пролиферацию гладкомышечных клеток и фибробластов бронхиальной стенки, способствуя повышенной реактивности бронхов и субэпителиальному фиброзу. ADAM-33 также принимает участие в угнетении легочных функций; - ген b2-адренергических рецепторов располагается на хромосоме 5q. Полиморфизм этого гена в условиях in vivo связан с различными реакциями гиперчувствительности в дыхательных путях, а в условиях in vitro — с различными ответами на стимуляцию b-агонистами. Таким образом, знание генотипа позволяет спрогнозировать ответ организма больного на терапию;
- множество вариантов полиморфизма гена рецептора IL-4, кодирующего a-цепь рецептора IL-4, связаны с атопией, повышенным уровнем общего IgE в сыворотке и астмой; - у человека в состав семейства хитиназ млекопитающих (хитиназа относится к ферментам, расщепляющим хитин — полисахарид, содержащийся во многих паразитах человека и клеточной стенке грибов) входят представители с ферментативной активностью и без таковой. У кислой хитиназы млекопитающих описано повышение активности при воспалительном ответе Тн2-клеток. Другой член семейства — YKL-40 — не обладает ферментативной активностью и связан с развитием астмы. Уровень YKL-40 в сыворотке коррелирует с тяжестью астмы.
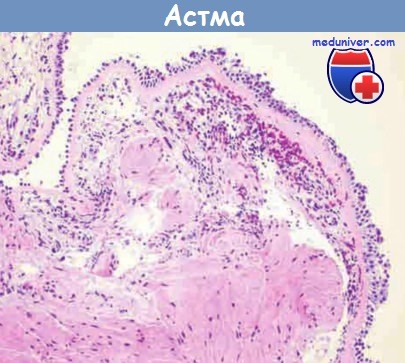
и гиперплазия гладкомышечных клеток при астме (бронхобиопсия).
ж) Морфология. У больных, умерших в состоянии астматического статуса, обнаруживают расширенные в результате гиперинфляции легкие с небольшими участками ателектазов. Наиболее ярким макроскопическим признаком приступа астмы является окклюзия бронхов и бронхиол крупными, вязкими слизистыми пробками. Гистологически пробки представляют собой слепки спущенного эпителия мелких бронхов и имеют спиралевидную форму (спирали Куршмана). Эти пробки также могут формироваться из слизи в протоках бронхиальных желез, а затем перемещаться в бронхиолы. В бронхиальном содержимом присутствуют многочисленные эозинофилы и кристаллы Шарко-Лейдена. Последние представляют собой кристаллы вытянутой формы из белка, связывающего липофосфолипазу эозинофилов, называемого галектином-10. Другие характерные гистологические изменения при астме, обозначаемые термином «ремоделирование дыхательных путей»:
• утолщение стенок бронхов;
• фиброз базальной мембраны под бронхиальным эпителием за счет отложения коллагена типов I и III под базальной мембраной, которая в норме состоит из коллагена типа IV и ламинина;
• усиление васкуляризации;
• увеличение размера бронхиальных подслизистых желез;
• слизистая метаплазия эпителия дыхательных путей;
• гипертрофия и/или гиперплазия гладких мышц бронхиальной стенки.
Это привело к разработке нового метода терапии — бронхиальной термопластики, при которой на стенки центральных дыхательных путей воздействуют радиоволнами через зонд, размещенный в бронхоскопе, что уменьшает гиперчувствительность дыхательных путей по крайней мере на 1 год.
Препятствие прохождению воздуха при астме связано прежде всего с бронхоспазмом, отеком слизистой оболочки и обтурацией слизью, однако и ремоделирование дыхательных путей может вносить свой вклад в обструкцию. Ремоделирование дыхательных путей, как полагают, способствует необратимой хронической обструкции дыхательных путей.
з) Клинические признаки. Классический острый приступ астмы длится несколько часов. У некоторых пациентов такие симптомы, как чувство стеснения в груди, одышка, свистящее дыхание и кашель с мокротой или без нее, присутствуют постоянно. При наиболее тяжелой форме проявления астмы — астматическом статусе — острый приступ длится несколько дней и даже недель. В этих условиях обструкция может быть столь выражена, что способна вызвать тяжелые застойные явления и даже смерть.
Клинический диагноз ставят на основании прогрессирования обструкции (от исходного уровня), затрудненности выдоха (удлинение времени выдоха, хрипы), эозинофилии, а также появления в мокроте эозинофилов, спиралей Куршмана и кристаллов Шарко-Лейдена (особенно у пациентов с атопической астмой).
Обычно астма протекает с приступами и ремиссиями, т.е. временными промежутками без респираторных симптомов, и больше изматывает больного, чем несет опасность летального исхода. При терапии, уменьшающей количество и тяжесть приступов, большинство людей с астмой могут вести активную жизнь. До 50% приступов астмы у детей смягчаются в подростковом возрасте, но довольно часто возвращаются в зрелом возрасте. В отсутствие терапии происходит постепенное снижение функции легких.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) бронхоэктатической болезни"
Оглавление темы "Патогенез болезней легких":- Механизмы развития (патогенез) отека легких
- Механизмы развития (патогенез) острого повреждения легких и ОРДС
- Механизмы развития (патогенез) острой интерстициальной пневмонии
- Классификация хронических диффузных болезней легких
- Классификация обструктивных болезней легких
- Механизмы развития (патогенез) эмфиземы легких
- Механизмы развития (патогенез) хронического бронхита
- Механизмы развития (патогенез) астмы
- Механизмы развития (патогенез) бронхоэктатической болезни
- Классификация рестриктивных болезней легких

