Коллоидальное золото в иммуногистохимии опухоли. Биотин-авидиновая иммуногистохимия
Использование в качестве метки антител коллоидального золота и других частиц основано на стабильном и быстром связывании частиц коллоидального золота с протеинами (в том числе антителами), энзимами и лектинами без изменения их биологической активности. Механизм состоит в том, что „вторичное" антитело, меченное частицами коллоидального золота, связывается с немеченым „первичным" антителом, уже связанным с тканевым антигеном. Красящая реакция интенсифицируется преципитацией серебра на частицах коллоидального золота. Для реализации такого механизма не требуются ни специальные субстраты, ни дорогое оборудование (как в методиках с энзимами или иммунофлуоресценцией) [De Mey, 1993]. Кроме того, он может комбинироваться с энзимной цитохимией, с другими методиками.
Для выявления золотой метки, окрашивающейся в красный цвет при световой микроскопии, нужна довольно высокая концентрация реагента. Правда, чувствительность реакции заметно возрастает, если дополнительно применять преципитацию серебра, что, кстати, уменьшает расход золота. Металлическое золото ускоряет уменьшение ионов серебра до размеров ионов металлического серебра в присутствии редуцента (гидрокинона), что в итоге приводит к положению, когда частица золота тесно обволакивается гранулами серебра, увеличивающими общий объем конгломерата так, что его без труда видно в световом микроскопе (черное окрашивание). P. Fritz с соавторами [1986] предложили ряд модификаций этого метода. Преимущества: высокая чувствительность, отсутствие рассеивания продуктов реакции, слабое фоновое окрашивание, возможности комбинации с обычным гистологическим окрашиванием срезов [Denk, 1987].
Частицы, несущие специфическую антигенную структуру, случайно прикрепившуюся к их поверхности или входящую в ее состав, скажем, антигены групп крови в эритроцитах, могут использоваться в качестве проб при фиксации к идентичным антигенам в тканях посредством антител-мостиков. Примером является реакция специфической адгезии эритроцитов, служащая для выявления антигенов групп крови в тканях.
Нередко применяют также метку „первичного" антитела гаптеном, например, арсалиновой кислотой, динитрофенолом, р-аминобензоил-глицином, р-аминобензонилглютаминовой кислотой. Гаптены затем распознаются мечеными антителами. Поскольку довольно большое количество гаптенов может связываться с антителом, антигенность последнего для „вторичного" антитела возрастает, и чувствительность также увеличивается. В качестве модификации используют методику немеченого антигаптенового антитела, реагирующего с гаптенизированным „первичным" антителом. Иными словами, в этом случае антитело-мостик, находящееся в среднем слое, связывается своими короткими цепями посредством молекул гаптена с длинными цепями „первичного" антитела и антитела внешнего слоя, которое, в свою очередь, может нести пару молекул пероксидазы или ПАП-комплекс.
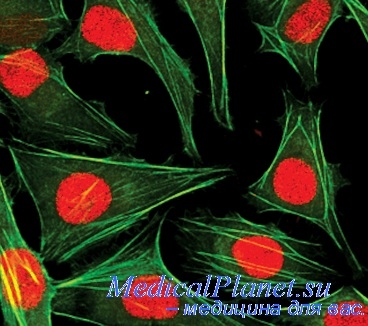
Нельзя не остановиться также на биотин-авидиновой методике. Авидин представляет собой белый яичный гликопротеин с молекулярным весом 68 тыс. дальтон и выраженной родственностью к биотину [Hsu, Raine, 1984]. В указанной методике антитела, меченные биотином, и авидин, меченный энзимом, применяются в определенной последовательности. В качестве маркерного энзима можно использовать в дополнение к пероксидазе хрена щелочную фосфатазу. С помощью „вторичных" антител, меченных биотином (трехступенчатая методика), требуется совсем немного биотинизированных антител для определения широкого ряда „первичных" антител. Однако „первичные" антитела, меченные биотином (двухступенчатая методика), способствуют выгодному слабому окрашиванию фона и устойчивому окрашиванию искомого субстрата. При прямой авидин-биотиновой мостовой методике авидин с помощью мостов связывается с „первичным" антителом, меченным биотином, и с энзимом (пероксидазой), меченным также биотином.
В случае применения непрямой методики „вторичное" антитело, меченное биотином, а также меченый энзим связываются посредством авидина. На различных ступенях реакции субстанции или применяются последовательно, или замещаются авидин-биотин-пероксидазным комплексом (ABC-реакция). Высокая чувствительность последней реакции объясняется следующими обстоятельствами: 1) Биотин связывается с антителом или энзимом (пероксидазой) посредством аминогрупп. Поскольку многочисленные половины молекул биотина могут быть введены в иммуноглобулин или пероксидазу, количество связующих сайтов для авидина возрастает. 2) Авидин имеет 4 активно связующих сайта для биотина. Не все эти сайты реагируют с биотином, связанным с антителом, но все они могут реагировать с молекулами биотина, связанными с пероксидазой. Это приводит к усилению красящей реакции, так как формируется большой комплекс, содержащий множество молекул пероксидазы. 3). Проникновение реагентов обеспечивается малым размером их молекул [Hsu, Raine, 1994]. По мере усугубления пенетрации антител Fab-фрагменты меченого биотина могут быть использованы и для световой, и для электронной микроскопии.
Конечно, качество реагентов ABC-реакции определяет ее чувствительность. Так, избыток свободных молекул авидина снижает чувствительность для молекул биотина, связанных с антителом. Если же имеется избыток биотин-пероксидазного комплекса, то биотин-связывающие сайты молекул авидина в этом комплексе могут насыщаться, и комплекс лишается этих сайтов, препятствующих его реакции с биотинизированным „вторичным" антителом. Неспецифическое связывание ABC-комплекса наблюдается при высоких концентрациях и может быть уменьшено за счет соответствующих разведений. Другие артефакты системы авидин-биотина могут быть следствием того, что авидин при нейтральном рН имеет сильный положительный заряд (изоэлектрическая точка около 10) и отсюда — неспецифическое прикрепление к отрицательно заряженным молекулам, включая нуклеиновые кислоты и фосфолипиды [Savage, 1996].
Авидин может быть заменен стрептавидином, который является белковым производным гриба Stretomyces avidini и имеет четыре высокоспецифичных связующих сайта для биотина. Он может быть конъюгирован с метками без утраты биотин-связывающих характеристик. Метки, используемые в системе стрептавидина, включают флуоресцеин, техасский красный, ферменты (пероксидазу, щелочную фосфатазу, бета-галактозидазу), коллоидальное золото. Неспецифического связывания стрептавидина с отрицательно заряженными молекулами и лектинами можно избежать благодаря отсутствию остатков карбогидратов и нахождению изоэлектрической точки около нейтрального рН. Усиление „сигнала" достигается включением биотина в множественные сайты „вторичного" антитела или при использовании стрептавидина, содержащего на каждую молекулу по несколько меченых молекул.
- Читать далее "Иммуногистохимия по методике меченого протеина А. Оценка кариотипа опухоли"
Оглавление темы "Иммуногистохимия опухоли":- Абберации хромосом опухолевых клеток. Модальное число
- Гистограммы распределения ДНК в опухоли. Анэуплоидные опухолевые клетки
- Перидиплоидные стволовые линии опухоли. Тест ядрышковых организаторов опухолевых клеток
- Онкофетальные антигены. Канцеро-эмбриональный антиген
- Альфа-фетопротеин (АФП). Иммуногистохимические маркеры дифференцировки опухоли
- Основные принципы иммуногистохимии. Иммунофлуоресцентная (или иммунолюминесцентная) микроскопия
- Пероксидазно-антипероксидазная (ПАП) методика. Реакции с гликозил-оксидазой при опухолях
- Хромоген для пероксидазных методик. Иммуногистохимия с щелочной фосфатазой
- Коллоидальное золото в иммуногистохимии опухоли. Биотин-авидиновая иммуногистохимия
- Иммуногистохимия по методике меченого протеина А. Оценка кариотипа опухоли

