Схема механизма развития гипоксии
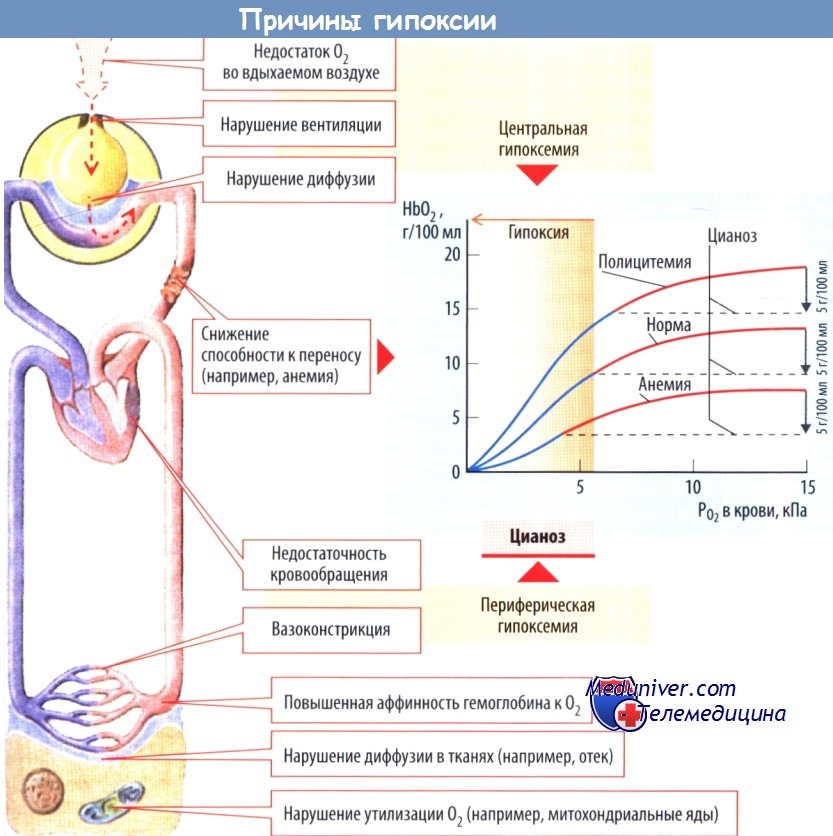
Гипоксия развивается при нарушении транспорта О2 из окружающего воздуха в ткани. Выделяют следующие причины гипоксии.
В результате гиповентиляции легких падает альвеолярная концентрация О2, уменьшая насыщение кислорода кровью. Однако значительное снижение поглощения О2 возникает только при выраженных нарушениях вентиляции.
Снижение диффузионной способности легких нарушает газовое равновесие между альвеолами и капиллярной кровью.
Уменьшение кислородной емкости крови отмечается при анемии либо неспособности гемоглобина связывать и высвобождать О2. Например, аффинность окиси углерода (СО) к гемоглобину превышает сродство кислорода в 200 раз. Соединение СО с одной из групп гема повышает сродство остальных трех, в результате пораженная молекула гемоглобина связывает меньше О2, значительно снижается и ее способность высвобождать ранее связанный кислород.
Повышенная аффинность к О2 в сочетании суменьше-нием высвобожденияО2 в ткани встречается при дефиците 2,3-бисфосфоглицерата и алкалозе.
Недостаточность кровообращения или местная ишемия вызывают нарушения сосудистого транспорта О2.
Нарушение диффузии в тканях возникает в случае увеличения расстояния между клеткой и ближайшим к ней капилляром, которое встречается при гипертрофии тканей без соответствующей пролиферации сосудов микроциркуляторного русла или отеке. Диффузионное расстояние увеличивается также при сокращении прекапиллярного сфинктера ближайшего капилляра. В этом случае О2 поступает через следующий ближайший сосуд.
Некоторые токсины, поступающие в дыхательную цепь, также могут нарушать утилизацию О2.
Наиболее значимое последствие всех вышеупомянутых причин — нарушение аэробного энергетического обмена клеток.
При гипоксии возрастающие потребности клетки в энергии могут быть частично удовлетворены АТФ, образующимся при распаде глюкозы до молочной кислоты. Однако в результате такой реакции высвобождается очень мало энергии (2 молекулы АТФ на 1 молекулу глюкозы в отличие от 32 молекул АТФ, образующихся при окислительном метаболизме), а диссоциация молочной кислоты приводит к развитию метаболического ацидоза. Недостаточное поступление энергии в клетку вначале вызывает обратимые нарушения ее функции, которые в конечном итоге сменяются необратимым повреждением.
Максимально допустимая продолжительность периода кислородного голодания, в течение которого изменения носят обратимый характер, зависит от типа клеток. Нейроны погибают приблизительно через 10 мин, клетки почек и печени — через несколько часов. Однако весь организм гибнет уже через 4 мин. Период обратимых изменений можно значительно увеличить путем снижения потребности клеток в О2 (например, при гипотермии).
Гиповентиляция, нарушение диффузии газов в легких и недостаточность кровообращения вызывают цианоз (синюшный цвет кожных покровов и слизистых оболочек) в том случае, если средняя концентрация восстановленного гемоглобина в капиллярной крови не превышает 0,7 ммоль/л (5 г/100 мл). При гиповентиляции и нарушении диффузии газов в легких артериальная кровь содержит недостаточное количество О2 (центральный цианоз).
Следует, однако, отметить, что цианоз не всегда является показателем дефицита О2. Если концентрация гемоглобина в крови возрастает, цианоз может сохраняться даже при отсутствии дефицита О2 (псевдоцианоз). И наоборот, низкое содержание гемоглобина (анемия) может сопровождаться недостатком О2, но концентрация восстановленного гемоглобина может не достигать уровня, необходимого для возникновения цианоза.
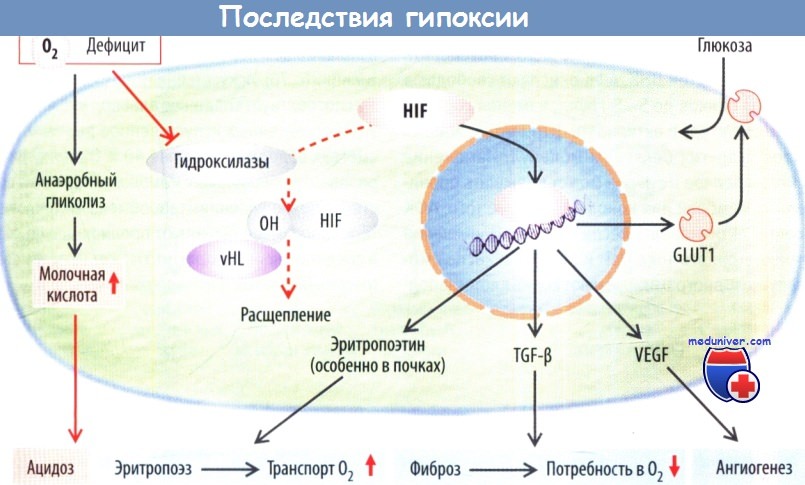
Недостаток кислорода вызывает увеличение количества чувствительных рецепторов HIF (фактор, индуцируемый гипоксией). Когда О2 поступает в достаточном количестве, происходит гидроксилирование этого фактора транскрипции HIF-пролил-4-гидроксилазой с последующим убиквитинированием — реакцией, опосредованной белком Гиппеля—Линдау (vHL) Убиквитинирование способствует протеасомному расщеплению HIF. При наличии О2 гидроксилазы активируются, в условиях гипоксии — инактивируются. Таким образом, при гипоксии HIF не расщепляется, проникает в ядро, связывается с ответственными за гипоксию элементами ДНК и вызывает экспрессию генов, отвечающих за выживание в условиях гипоксии.
К HIF-чувствительным генам относятся VEGF (эндотелиальный фактор роста сосудов), который стимулирует образование новых капилляров (ангиогенез), и TGF-b, стимулирующий образование матриксных белков (фиброз). Замещение клеток матриксными белками снижает потребность ткани в О2. Однако уменьшение количества клеток нарушает функцию органа (например, сократимость сердечной мышцы) Изменение экспрессии клеток при повторных коротких или продолжительных транзиторных периодах гипоксии повышает сопротивляемость тканей к гипоксии или ишемии (предварительная подготовка и гибернация). В почках HIF повышает выработку эритропоэтина, который является стимулятором образования новых эритроцитов и, соответственно, улучшает транспортную функцию крови.
- Рекомендуем ознакомиться со следующей статьей "Схема развития отравления кислородом (гипероксии, оксидативного стресса)"
Оглавление темы "Патофизиология в схемах":- Схема развития эмфиземы легких
- Схема развития отека легких
- Схема развития нарушения регуляции дыхания
- Схема развития острого респираторного дистресс синдрома (ОРДС)
- Схема механизма развития гипоксии
- Схема развития отравления кислородом (гипероксии, оксидативного стресса)
- Схема развития респираторного и метаболического алкалоза
- Схема развития респираторного и метаболического ацидоза
- Схема механизмов компенсации ацидоза и алкалоза
- Функции почек и виды их нарушений

