Принципы функционирования ионных каналов клетки - с точки зрения физиологии человека
Оглавление статьи:- Основные свойства ионных каналов
- Ионные токи, проходящие через каналы
- Резюме
- Список использованной литературы
Мальчик из племени куреши-бидари, обитающего на севере Пакистана, с 10 лет получил популярность, особенно в местных больницах, благодаря своим эксцентричным «уличным представлениям». Он наносил себе раны, втыкал в руки ножи, ходил по раскаленным углям и при этом не испытывал боли. Мальчик погиб незадолго до того, как ему исполнилось четырнадцать, спрыгнув с крыши дома во время одного из своих номеров.
Английские генетики и врачи заинтересовались этим случаем и позднее выявили еще шесть детей в возрасте от 6 до 14 лет, которые не проявляли никаких признаков наличия болевых ощущений, несмотря на многочисленные гематомы, плохо залеченные переломы, а также повреждения губ и языка. Осязание, проприоцепция и восприятие температуры были у них нормальными.
Современные генетические исследования (например, анализ сцепления между генными локусами) показали, что причиной полного отсутствия болевой чувствительности у этих детей были мутации гена SCN9A, который кодирует потенциалзависимые натриевые каналы типа NaV1.7 и экспрессируется прежде всего в спинальных нервах, проводящих болевые сигналы.
а) Основные свойства ионных каналов. Ионные каналы — интегральные мембранные белки, которые обеспечивают перемещение ионов через липидный бислой клеточной мембраны.
Многие физиологические процессы, такие как генерация возбуждения и его проведение в нервах, в сердце или скелетных мышцах, обусловлены электрическими процессами в клеточной мембране. Основу их составляют потоки малых неорганических ионов (Na+, K+, Ca2+ или Cl-) через ионные каналы — особый класс мембранных белков.
1. Структура клеточной мембраны. Клеточная мембрана состоит из двух химических компонентов — липидного бислоя и встроенных в него мембранных белков. Липидный бислой представляет собой практически идеальный электрический изолятор. В то время как липофильные неполярные вещества могут диффундировать через липидный бислой, для заряженных и полярных частиц он непроницаем.
Чтобы проникнуть из воды в липидный слой, заряженные частицы должны освободиться от своей гидратной оболочки. Для этого ионы нуждаются в большом количестве энергии, которым клетка не обладает (барьер Борна).
2. Концепция ионных каналов. Ионные каналы — интегральные мембранные белки, которые образуют в мембране заполненную водой диффузионную пору (рис. 1). Липофильные частицы канала контактируют с клеточной мембраной, а гидрофильные частицы соединяют внутриклеточное и внеклеточное пространство через пору.
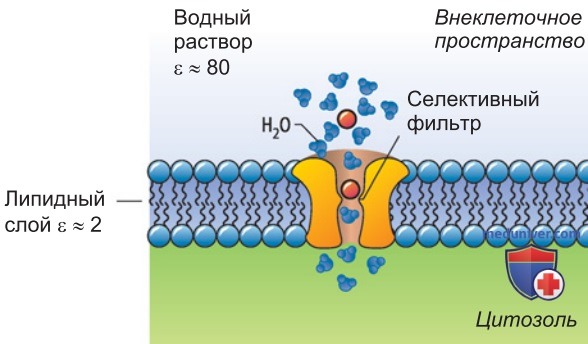
При транспорте иона от одной стороны мембраны к другой не требуются изменения конформации белка. Поэтому ионные каналы — это эффективные электрические проводники (скорость транспорта ~107-108 ионов/с). Они всегда присутствуют там, где возникают достаточно сильные электрические токи, например в возбудимых клетках, генерирующих разряды потенциалов действия.
3. Электрохимические потенциалы. Существует два вида движущей силы, способные перемещать ионы по трансмембранным каналам: градиент концентрации (химическая движущая сила) и разность потенциалов (электрическая движущая сила). В совокупности они составляют электрохимическую движущую силу.
Если концентрация иона в клетке равна c1, а вне клетки — с2, то возникает трансмембранный потенциал V; тогда разность электрохимической энергии рассчитывается по следующей формуле:
ΔE = RT ln c1/ c2 + zFV,
где R — универсальная газовая постоянная; Т — абсолютная температура; z — заряд или валентность иона; F — постоянная Фарадея; V — мембранный потенциал.
Другое уравнение, отражающее аналогичные закономерности, основано на определении равновесного потенциала для иона (Vrev), т. е. мембранного потенциала, при котором результирующий поток иона (нетто-поток) равен 0:
ΔE = zF(V - Vrev), при Vrev = RT/zF x lnc1/ c2
Пассивный транспорт осуществляется по электрохимическому градиенту. Перемещение против электрохимического градиента, например для создания градиента концентрации, невозможно обеспечить путем транспорта через ионный канал.
4. Селективность. Ионные каналы в той или иной мере избирательны по отношению к проникающим через них ионам. В принципе ионные каналы подразделяются на катионные и анионные. Многие катионные каналы избирательны для определенных ионов, названиями которых обозначены типы каналов. Натриевый канал пропускает только ионы натрия, калиевый канал — ионы калия.
5. Воротные механизмы ионных каналов. Пропускная способность ионных каналов зависит от специфических изменений их конформации. Канал может совершать переходы от закрытого состояния к открытому и наоборот. Такое устройство канала получило название воротного механизма (gating). Переключение воротного механизма канала (открытие или закрытие ворот) может происходить в ответ на различные внешние стимулы:
- изменения мембранного потенциала;
- изменения концентрации медиаторных веществ (иначе говоря трансмиттеров);
- механические воздействия (например, давление или растяжение);
- изменения температуры (тепло или холод).
Переключение воротного механизма сопровождается быстрым изменением электрического тока, проходящего через клеточную мембрану. Эта реакция составляет основу электрических сигналов, генерируемых клетками.
б) Ионные токи, проходящие через каналы. Среднее значение ионного тока, проходящего через канал, зависит от проницаемости канала и вероятности его открывания.
1. Ток ионов через канал. Средний ток ионов, проходящий за конкретное время через ионный канал, определяют два фактора.
- Амплитуда тока через индивидуальный канал, т. е. сила тока (рис. 2). Зависит от концентрации проникающих ионов по обе стороны мембраны и от заряда мембраны. При равновесном потенциале ток через индивидуальный канал равен нулю, поскольку электрический и химический градиенты уравнены.
- Вероятность открывания канала, т. е. продолжительность времени, в течение которого канал открыт для прохода ионов.
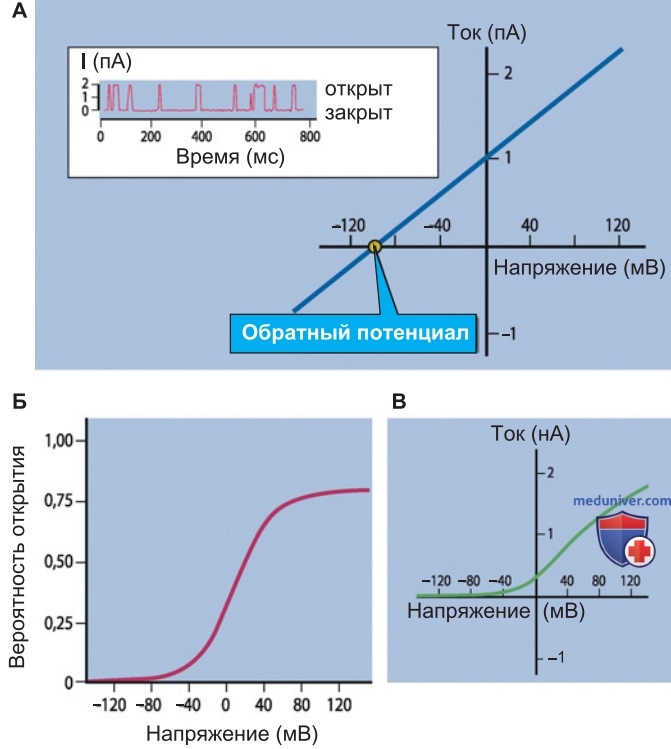
При значениях мембранного потенциала, более положительных, чем равновесный потенциал для иона, возникает выходящий результирующий нетто-ток катионов через катионные каналы и входящий нетто-ток анионов через анионные каналы. При отрицательном мембранном потенциале наблюдается противоположная ситуация. Чем значительнее движущая сила, т. е. разница между мембранным потенциалом и равновесным потенциалом, тем больше амплитуда ионного тока (рис. 2).
Исходя из соотношения между мембранным потенциалом и амплитудой тока индивидуального ионного канала можно на основе закона Ома (R = U/I) вычислить сопротивление или проводимость (g = 1/R) индивидуального канала. В зависимости от типа канала, концентрации ионов и температуры среды проводимость индивидуальных ионных каналов составляет от 1 до 100 пС (1 пС = 10-12 С), а сопротивление от 1 ТОм (1 ТОм = 1012 Ом) до 10 ГОм (1 ГОм = 109 Ом).
- Фиксация потенциала (voltage-clamp) и пэтч-кламп (patch-clamp) — локальная фиксация потенциала, или фиксация потенциала микроучастка мембраны. Токи ионных каналов регистрируются с помощью метода фиксации потенциала (рис. 3). Представлена исходная версия метода, разработанная в экспериментах на гигантском аксоне кальмара. Были использованы два электрода.
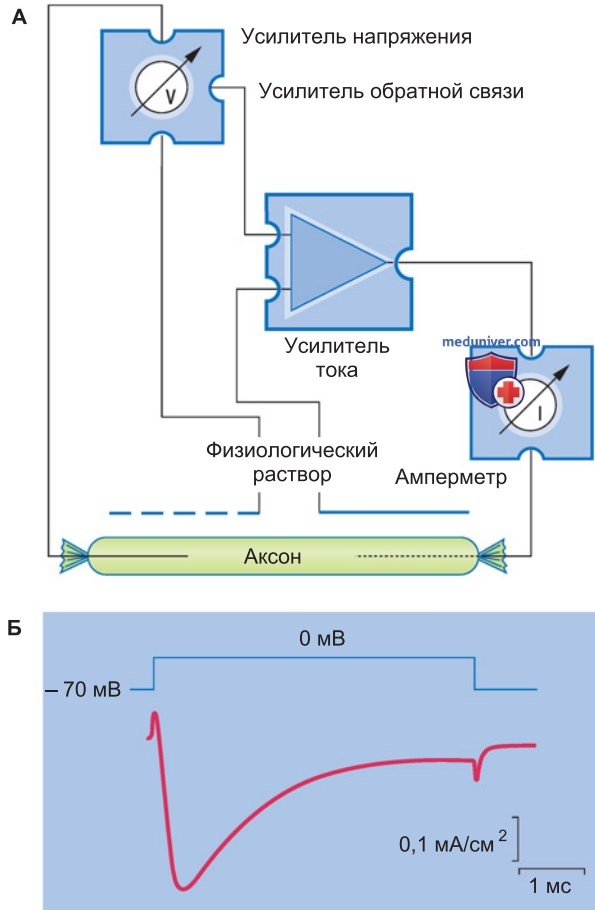
С помощью одного из них измеряют мембранный потенциал, сопоставляемый с заданным (фиксируемым) уровнем. Второй электрод служит для пропускания тока фиксации, который в случае отклонения мембранного потенциала удерживает его на заданном уровне. Пропускаемый ток является отражением ионного тока, проходящего через мембрану при заданном уровне потенциала (рис. 3). Чтобы выявить токи потенциалуправляемых натриевых каналов, нужно блокировать все иные компоненты регистрируемого суммарного тока.
При смещении мембранного потенциала от -70 до 0 мВ Na+-ток сначала равен нулю, затем быстро нарастает до максимума и снова возвращается к нулю. Причиной такой динамики Na+-тока является изменение числа открытых Na+-каналов с течением времени. При -70 мВ все Na+-каналы закрыты, при 0 мВ вероятность их открывания сначала повышается, затем в результате особого процесса (инактивации каналов) вновь падает до нуля (см. далее).
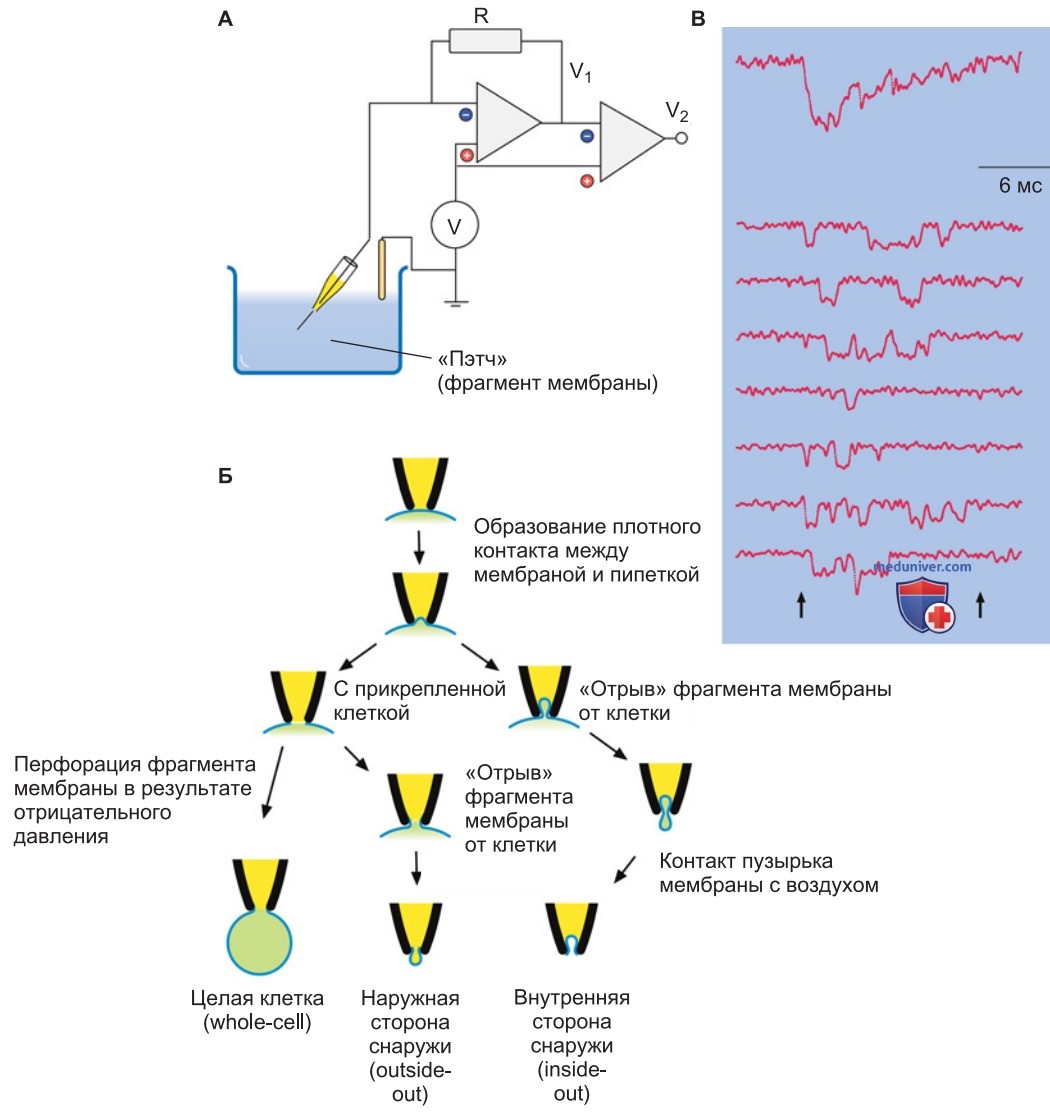
- Метод локальной фиксации потенциала позволяет регистрировать токи одиночных ионных каналов, причем в отличие от двухэлектродной методики в эксперименте используют только один электрод и соответствующую схему обратной связи (рис. 4). При этом вплотную к клеточной мембране подводят кончик стеклянной микропипетки, в который затем всасывают фрагмент мембраны (patch), обеспечивая электрически изолированный (высокоомный) контакт.
Если пипетку вместе с втянутым в ее кончик фрагментом мембраны резко оторвать от клетки, получится конфигурация inside-out-patch — «внутренняя сторона снаружи», когда с раствором в пипетке контактирует внешняя сторона мембраны; возможна также конфигурация outside-out-patch — «наружная сторона снаружи», когда с содержимым пипетки контактирует внутренняя сторона мембраны. Если во фрагменте мембраны находится только один функционирующий канал, то с помощью метода фиксации потенциала можно исследовать его свойства.
1. Структура ионных каналов. Ионные каналы — интегральные мембранные белки, которые образуют заполненную водой пору, обеспечивая проникновение ионов через липидный бислой мембраны. Движущей силой для диффузии ионов через пору является электрохимический градиент, который складывается из градиента концентрации (химическая движущая сила) и разности потенциалов (электрическая движущая сила).
2. Селективность ионных каналов. Ионные каналы проявляют более или менее выраженную селективность в отношении проходящих через них ионов. Существует две основные группы каналов: катионные (различаются в зависимости от природы пропускаемых ими катионов) и анионные. Функциональные характеристики каналообразующих белков (за исключением селективности) определяются особенностями работы их воротного механизма.
В результате конформационных изменений канал может переключаться между открытым и закрытым состояниями, причем в открытом состоянии пора канала проницаема для ионов.
Поток ионов через канал зависит от вероятности его открывания и амплитуды тока через него.
- Рекомендуем ознакомиться далее "Строение потенциалуправляемых катионных каналов клетки - с точки зрения физиологии человека"
Редактор: Искандер Милевски. Дата публикации: 10.9.2024

