Современное лечение меланомы
а) Лечение первичной меланомы:
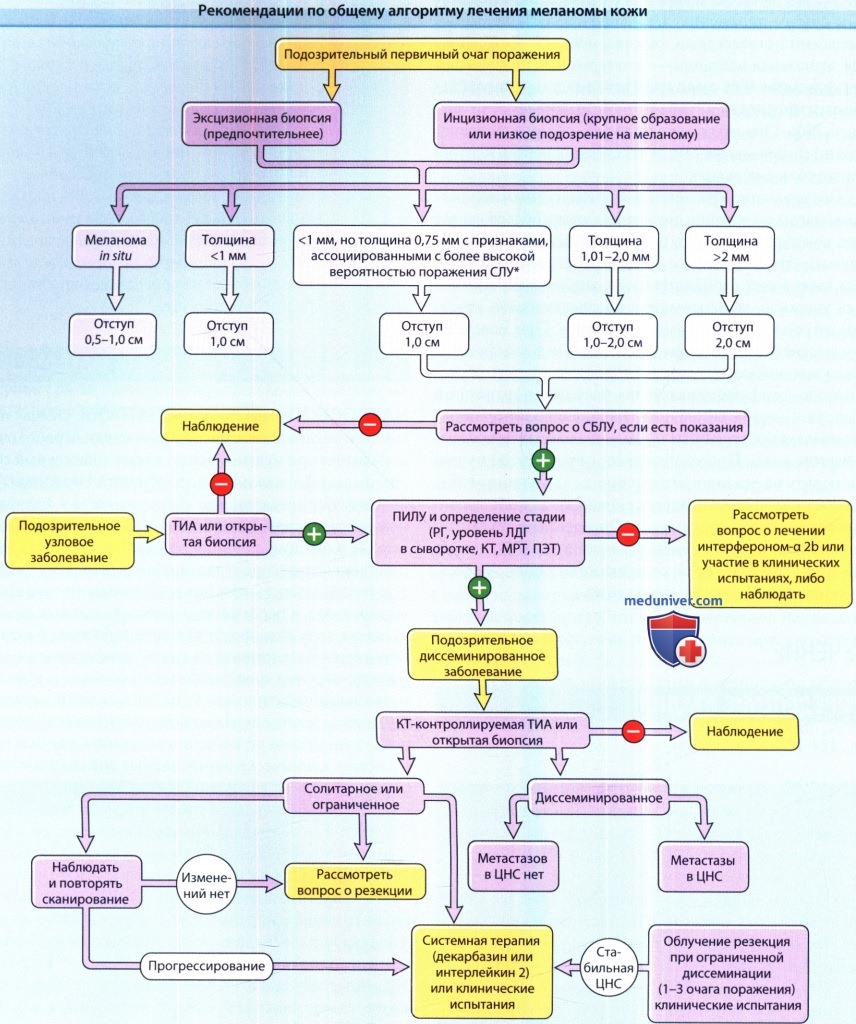
1. Хирургическое лечение меланомы. Общий алгоритм ведения пациентов с меланомой кожи от 2018 года представлен на рисунке ниже. Стандарт лечения первичной меланомы кожи — это широкое иссечение. Целью широкого местного иссечения является предотвращение рецидива путем радикальной резекции с гистологическим подтверждением отсутствия опухоли в краях раны.
Истинный местный рецидив, возникший в результате неадекватного иссечения, имеет большое клиническое значение в небольшом количестве случаев возможного предотвращения летального исхода. Рекомендованный в настоящее время отступ от края резидуального образования или рубца, оставшегося после биопсии меланомы in situ, не по типу злокачественного лентиго, составляет 0,5-1 см; в случае меланомы с толщиной по Бреслоу менее 1 мм отступ составляет 1 см; при меланоме толщиной 1-2 мм анатомически возможен отступ 1-2 см; при меланоме толщиной > 2 мм — отступ 2 см (с гистологическим подтверждением чистоты края раны во всех случаях). В ряде крупных рандомизированных контролируемых исследований не удалось доказать наличие различий по показателям выживаемости или частоте развития локальных рецидивов между узким (1-2 см) и широким (3-5 см) отступом.
В конечном счете каждого пациента нужно обследовать по индивидуальному плану с учетом актуальных хирургических рекомендаций, а также области поражения (т.е., локализации вблизи жизненно важных структур), возможности первичного заживления раны или необходимости использования кожного трансплантата, а также наличия или отсутствия негативных прогностических факторов, согласно результатам определения микростадии. Иссечение меланомы в особых локализациях, таких как пальцы, подошвы, уши, влагалище или анус, требует особого подхода с учетом не только хирургических, но и физиологических аспектов. Тем не менее в онкологии должен соблюдаться следующий основной принцип: в первую очередь удаление опухоли, и, что наиболее важно, реконструктивное вмешательство во вторую очередь. При хирургическом лечении подногтевой меланомы методом выбора остается частичная или полная ампутация пальца.
2. Злокачественное лентиго и лентиго-меланома. Гистологическое подтверждение чистоты краев раны особенно важно при злокачественном лентиго (ЗЛ) и лентиго-меланоме (ЛМ), подтипах меланомы, с хорошо известной склонностью к формированию по периферии субклинической части очага поражения. Риск наличия инвазивного десмопластического компонента при ЗЛ возрастает. Стандартные хирургические рекомендации соблюдения отступа 0,5 см при ЗЛ и 1 см при ЛМ с толщиной менее 1 мм часто недостаточны, и позволяют полностью удалить только 50% опухолей.
В одном исследовании было обнаружено, что отступ, необходимый для полного удаления злокачественной меланомы (ЗЛ) составляет 0,8 см, а для удаления 96% очагов злокачественной меланомы (ЗЛ) требуется отступ, равный 1,5 см. Средний отступ, необходимый для удаления лентиго-меланомы (ЛМ) составил 1,1 см, и 2,6 см для удаления 95% очагов ЛМ. Другие авторы сообщали, что при 97% меланом размером менее 1,5 см для полного удаления требовался отступ 11,5 см, тогда как при 95% меланом диаметром более 3 см для полного удаления требовался отступ 2,5 см. В другом исследовании у пациентов с меланомой ЗЛ/ЛМ периокулярной локализации резекция проводилась по краям без опухолевых клеток в среднем с отступом 1,3 см для ЛМ in situ и 1,6 см для инвазивной ЗЛ, при этом частота рецидивов составляла 2% за 8 лет.
Частота рецидивов после стандартного иссечения со стандартным изготовлением срезов по типу «буханки хлеба» при ЗЛ недопустимо высока и составляет до 20% и выше. Разработано несколько методов сочетания иссечения и гистологического исследования: стандартное иссечение со стандартным вертикальным изготовлением срезов (то есть по типу «буханки хлеба»); картированное поэтапное иссечение с вертикальными разрезами и узкими интервалами; микрографическая хирургия по Мосу с получением горизонтальных замороженных срезов с иммуногистохимическим окрашиванием или без него; микрографическая хирургия по Мосу с изготовлением перманентных горизонтальных срезов; картированные (то есть «медленная техника» по Мосу) поэтапные геометрические иссечения по периметру с вертикальными срезами образцов ткани по периферии (то есть «квадратная» техника).
Использование техники по Мосу предпочтительнее с точки зрения возможности максимально «экономного» иссечения тканей, но замороженные препараты срезов очень трудно точно интерпретировать, даже с использованием иммуногистохимического окрашивания. Хотя подход и обсуждается, до настоящего времени не представлено исследований, подтверждающих преимущество того или иного подхода и обладающих минимально приемлемым научно-методическим дизайном и анализом данных. «Золотым стандартом» гистологического исследования хирургических краев для изучения меланоцитарных образований считается использование перманентных срезов, фиксированных в формалине, которое в целом значительно эффективнее метода замороженных срезов. Даже при использовании «медленной техники» по Мосу перманентная обработка и интерпретация горизонтальных срезов проблематична для патогистологов, не знакомых с этой техникой.
Гистологическая оценка краев требует значительного опыта, так как существует целый спектр, варьирующий от фоновой доброкачественной гиперплазии переходных меланоцитов до среза зоны гиперплазии атипичных переходных меланоцитов. Одним из наиболее часто гипердиагностируемых пролифератов являются образования с активированными меланоцитами. Эти клетки очень часто присутствуют на коже с признаками фотоповреждения и характеризуются одинаковым строением с маленькими округлыми ядрами, окруженными бледной цитоплазмой, расположенными в центре «прозрачной зоны» гиперхромного ядра полулунной формы с минимальным количеством цитоплазмы вдоль зоны базальной мембраны. Этот тип изменений может быть обнаружен в большинстве дермальных невусов и ангиофибром на открытых участках кожи. Для всех техник, описанных выше и используемых в настоящее время, ключевое значение имеет опыт выполняющего их патологоанатома.
Изъязвление, экстенсивная вертикальная регрессия толщиной до 1 мм и больше, молодой возраст пациента, высокий митотический индекс (в особенности у молодых пациентов, положительный результат исследования глубоких краев раны, инвазия в кровеносные и лимфатические сосуды и IV уровень инвазии по Кларку).
ПИЛУ—полное иссечение лимфатических узлов; ЦНС—центральная нервная система; КТ—компьютерная томография; РГ—рентгенография органов грудной клетки;
ТИА—тонкоигольная аспирация; ЛДГ—уровень лактатдегидрогеназы в сыворотке крови; МРТ—магнитно-резонансная томография;
ПЭТ—позитронно-эмиссионная томография; БСЛУ—биопсия сторожевого лимфатического узла.
Знак «минус» указывает на отсутствие признаков заболевания, «плюс» означает наличие метастазов.
Пациента, которому планируется проведение биопсии сторожевого лимфатического узла, следует направить к хирургу, имеющему опыт в проведении данной процедуры, чтобы можно было всесторонне обсудить необходимость данной процедуры и возможные осложнения.
б) Лечение меланомы при региональных метастазах:
1. Поражение лимфатических узлов макрометастазами. Полное иссечение лимфатических узлов. В настоящее время стандартом лечения микроскопических и макроскопических метастазов меланомы в лимфатические узлы является полное иссечение лимфатических узлов (ПИЛУ) в области пораженного бассейна. Оставление пораженных лимфатических узлов является причиной смерти от меланомы и значительно снижает качество жизни. Современные рекомендации NCCN не регламентируют число лимфатических узлов, которое является достаточным для адекватного иссечения. Согласно этим рекомендациям, отчет об операции полной лимфодиссекции должен включать полноценное описание анатомических пределов удаления лимфоузлов. ПИЛУ для удаления регионарных метастазов меланомы сопровождается долгосрочной выживаемостью у значительной части пациентов.
2. Микрометастатическое поражение лимфатических узлов. Элективное иссечение лимфатических узлов (ЭИЛУ) — это удаление регионарных лимфатических узлов, дренирующих область, в которой расположен первичный очаг поражения при меланоме, в отсутствие пальпируемых лимфатических узлов или других клинических признаков метастазов. До появления биопсии СЛУ, ЭИЛУ назначалась при меланомах с высоким риском поражения регионарных лимфоузлов для своевременной и потенциально излечивающей эрадикации субклинических микрометастазов. Достоверного преимущества ЭИЛУ при меланоме не удалось доказать ни в одном из многочисленных проспективных рандомизированных контролируемых исследований. В этой связи на сегодняшний день ЭИЛУ не играет значимой роли в лечении меланомы, особенно в свете доступности и усовершенствования БСЛУ.
Как отмечалось ранее, БСЛУ представляет собой мощный инструмент для определения стадии болезни при поражении лимфатических узлов микрометастазами. БСЛУ в настоящее время с учетом имеющихся данных нельзя считать терапевтической процедурой, и в рандомизированном исследовании MSLT-I у пациентов, прошедших БСЛУ, выживаемость, связанная с наличием меланомы, не отличалась от таковой у пациентов, которым БСЛУ не выполнялась. Это неудивительно, поскольку исследование не обладает достаточной мощностью, чтобы дать ответ на этот вопрос, при том что приблизительно у 80% пациентов не выявляются метастазы в лимфоузлах. Вместе с тем в группе пациентов с метастазами меланомы в лимфатические узлы пятилетняя выживаемость была достоверно выше при положительных результатах биопсии сторожевого лимфатического узла с последующей немедленной лимфаденэктомией по сравнению с пациентами, у которых лимфаденэктомия проводилась после периода наблюдения в связи с клинически выраженным поражением лимфоузлов (72% и 52% соответственно).
Критики исследования справедливо указывают на тот факт, что по этому показателю рандомизации не проводилось, и эти данные нельзя назвать окончательными. Вместе с тем полученная информация указывает на потенциальные преимущества, что требует в дальнейшем проведения анализа более полноценных данных.
Среди пациентов с положительным результатом БСЛУ доля тех, у которых при полной лимфаденоэктомии выявляются метастазы в других лимфоузлах, составляет 15—20%. Соответственно при положительных результатах БСЛУ следует проводить полную лимфаденэктомию, что обеспечивает как терапевтический эффект, так и улучшение прогноза. Среди пациентов с меланомой, у которых выявляются метастазы в лимфатические узлы, поражение несторожевых лимфоузлов является значимым плохим прогностическим признаком. Кроме того, полученные отчеты говорят в пользу улучшенного контроля состояния региональных лимфоузлов, что позволяет уменьшить число осложнений. Пациенты, которым проводится полная лимфаденэктомия по поводу положительных результатов биопсии сторожевого лимфатического узла, отличаются значительно меньшим риском послеоперационных осложнений или лимфостаза по сравнению с пациентами, у которых такое вмешательство проводится в связи с клинически выраженным поражением.
В настоящее время проводится исследование MSLT-II, цель которого состоит в определении того, существует ли идентифицируемая субпопуляция пациентов, у которых были бы показаны благоприятные результаты без проведения полной лимфаденэктомии после положительного результата биопсии сторожевого лимфатического узла. Ввиду отсутствия новых данных пациенты с положительными результатами биопсии—по описанным выше причинам—должны пройти полную лимфаденэктомию или быть включенными в исследование MSLT-II.
3. Адъювантная терапия меланомы:
- Интерферон-а2b. Адъювантная терапия — это дополнительное лечение пациентов, которым проведена хирургическая резекция клинически определяемых очагов поражения, но у которых имеется высокий риск рецидива, например толщина меланомы > 4 мм в сочетании с изъязвлением или поражением лимфатических узлов. Высокие дозы интерферона-а2b (ИФН-а2b) являются единственным вариантом адъювантной терапии, утвержденным Управлением по контролю за продуктами и лекарствами США, которая достоверно улучшает безрецидивную выживаемость при IIB-III стадиях меланомы. Низкодозные режимы не показали преимущества. Схема лечения высокими дозами предусматривает применение 20 млн. единиц на квадратный метр поверхности тела в день, которые вводятся внутривенно пять дней в неделю в течение четырех недель (фаза индукции), после чего— 10 млн. единиц на квадратный метр поверхности тела в день подкожно три раза в неделю в течение 48 недель (поддерживающая фаза). Примечательно, что появление аутоантител или клинических проявлений аутоиммунных реакций (витилиго) в ходе лечения препаратами ИФН может ассоциироваться созначительным улучшением безрецидивной выживаемости и общей выживаемости пациентов с меланомой при проведении адъювантной терапии ИФН.
При проведении терапии высокими дозами ИФН наблюдается выраженный токсический эффект, который чаще всего проявляется в виде гриппоподобных симптомов практически у всех пациентов (то есть утомляемость, анорексия, снижение массы тела, миалгии, лихорадка, тошнота, головная боль). Другие побочные эффекты включают депрессию, гепатотоксичность (повышение уровня трансаминаз) и подавление образования клеток крови в красном костном мозге. Токсичность может потребовать коррекции дозы, и большинство из тех пациентов, которые переносят первые 3 месяца терапии,способны получить по меньшей мере 80% назначенной дозы и завершить весь курс лечения. Кроме того, улучшается качество жизни, и пациенты, по-видимому, предпочитают получать лечение ИФН вместо отсутствия терапии. Следует оценивать потенциальный положительный эффект и потенциальные риски развития интоксикации индивидуально у каждого пациента.
- Антимеланомная вакцина. Были проведены широкие исследования использования ряда аутологичных, аллогенных и пептидных вакцин для лечения меланомы, но, к сожалению, без существенных успехов, так как ни одна из вакцин в настоящее время не разрешена для использования в клинической практике. Вакцины являются привлекательным методом лечения, они обладают ясным механизмом действия, связываясь с антигенами, и характеризуются низкой токсичностью. При использовании этого метода пытаются стимулировать специфический иммунный ответ на действие ассоциированных с меланомой антигенов. Изучается несколько многообещающих подходов к разработке антимеланомной вакцины.
4. Сателлитные или транзиторные метастазы:
- Изолированная перфузия конечности. В целом при заболевании с регионарными, транзиторными или сателлитными метастазами должно быть по возможности выполнено иссечение с получением гистологически «чистых» краев раны. Однако если множественные очаги поражения делают хирургическое вмешательство нецелесообразным, можно рассмотреть вопрос об изолированной перфузии конечности (ИПК) при локоре-гиональной форме заболевания, ограниченной только конечностью. ИПК это форма регионарной химиотерапии, которая позволяет доставить более высокие дозы химиотерапевтического препарата, что сопровождается значительно менее выраженными симптомами интоксикации. Эта методика включает перфузию конечности цитотоксическими препаратами, обычно мелфаланом, в условиях гипертермии. ИПК с мелфаланом — эффективная форма регионарной терапии, которая в некоторых случаях сопровождается возникновением осложнений, и при которой частота достижения частичного или полного регионарного ответа может составлять до 80%. Преимущества обусловлены возможностями местно-регионарного контроля, а не улучшением общей выживаемости.
Процедура ИПК связана с серьезными местными осложнениями, которые включают значительно повреждение тканей и компартмент-синдром. Пожилой возраст и тяжелые сопутствующие заболевания в целом считаются противопоказаниями для проведения этой терапии. Изолированная инфузия конечности (ПИК) — это более новый, более простой и менее инвазивный метод. Первые исследования ПИК с мелфаланом и актиномицином L) продемонстрировали сравнимую эффективность с ИПК с мелфаланом. Вопрос о проведении ПИЛ можно рассматривать у пациентов, которым ИПК противопоказана.
в) Лечение меланомы при отдаленных или диссеминированных метастазах. При лечении меланомы IV стадии необходимо учитывать, что средняя выживаемость составляет 6-8 месяцев, и что нет системных методов лечения, которые в рандомизированных контролируемых исследованиях увеличивали бы выживаемость. Целью лечения должно быть увеличение продолжительности жизни и облегчение симптомов заболевания. Вариант наблюдения и консервативного лечения также обоснован, особенно при бессимптомном течении, пожилом возрасте пациента или наличии тяжелых сопутствующих заболеваний.
Может быть проведено хирургическое иссечение отдельных метастазов внутренних органов (т.е. метастазэктомия), стабильных в течение 3-6 месяцев до удаления, при этом в некоторых случаях отмечаются длительные ремиссии. Хирургическое иссечение кожи/подкожной жировой клетчатки или отдаленных лимфатических узлов может улучшить результаты местного лечения и уменьшить осложнения. Хирургическое лечение также может быть паллиативным, например, для устранения обструкции при метастазах в желудочно-кишечном тракте. Меланома не отличается высокой чувствительностью к лучевой терапии, однако этот вид лечения применяется, ему отдают предпочтение при метастазах в головной мозг с образованием более трех очагов, а также после стереотаксической радиохирургии или стандартного оперативного вмешательства по поводу очагового поражения. Паллиативное облучение может быть показано при компрессии спинного мозга и болезненных метастазах в костях.
г) Системная терапия меланомы:
1. Химиотерапия и иммунотерапия. Алкилирующий препарат декарбазин (DTIC) является единственным химиотерапевтическим средством, разрешенным Комиссией по контролю за лекарствами и питательными веществами для лечения метастатической меланомы. Частота улучшения варьирует от 10% до 20%, при этом средняя продолжительность улучшения составляет 4-6 месяцев. Различий с точки зрения частоты улучшения и длительности улучшения при назначении разных схем лечения не выявлено. Основными побочными эффектами являются тошнота и рвота. Темозоломид (TMZ) — алкилирующий препарат с тем же самым активным метаболитом (DTIC), но способный проникать через гематоэнцефалический барьер, и принимать этот препарат можно перорально. В рандомизированном исследовании III фазы было показано, что эффективность TMZ эквивалентна эффективности DTIC. Кроме этого, в виде монотерапии используют паклитаксел или высокие дозы интерлейкина-2. Болюсное введение интерлейкина-2 (ИЛ-2) является единственным иммунологическим методом лечения метастазирующей меланомы, одобренным Комиссией по контролю за лекарствами и питательными веществами (в 1998 г.), который может приводить к длительному полному излечению. Было показано, что ИЛ-2 является единственным препаратом, способным вызывать общее улучшение в 16% случаев, а длительное улучшение — у 5-8% пациентов, чаще всего при поражении легких, лимфатических узлов и/или метастазах в кожу.
Применение высоких доз ИЛ-2 ассоциируется со значительной токсичностью, поэтому такая терапия проводится только в специализированных программах под руководством опытных специалистов и после тщательного отбора пациентов.
Все чаще при меланоме проводят комбинированную химиотерапию, включая такие режимы как CVD (цисплатин, винбластин и дакарбазин). Сочетание CVD с терапией интерфероном-а и ИЛ-2 получило название биохимиотерапии и позволяет достичь более высокой частоты ответа по сравнению с изолированным применением CVD. В то же время биохимиотерапия отличается большей токсичностью и вряд ли сможет улучшить общую выживаемость.
2. Новые методы лечения. Мутация в гене B-raf была обнаружена в двух третях меланом. Сорафениб — это новый ингибитор B-raf и C-raf, доступный в пероральной форме, который, однако, в исследовании III фазы продемонстрировал незначительную активность у пациентов с неоперабельной меланомой III или IV стадии. Недавно в исследовании I фазы новый пероральный ингибитор BRAF, PLX4032 (также известный как R05185426) продемонстрировал ответ у 70% пациентов с метастатической меланомой. Этот препарат был одобрен в 2011 году для таргетной терапии при BRAF V600-позитивных опухолях IV стадии.
Меланомы с локализацией на конечностях и слизистых оболочках по своим генетическим характеристикам отличаются от других видов меланом. В большинстве случаев при этих меланомах не отмечается мутаций BRAF, однако существует субпопуляция, в которой имеются активирующие мутации или амплификация рецепторной тирозинкиназы KIT. В первых исследованиях ингибитора тирозинкиназы иматиниба был показан достоверный ответ у пациентов с метастатической меланомой с активирующей мутацией c-KIT. В настоящее время у пациентов с меланомой с мутациями c-KIT продолжаются исследования как одобренных, так и новых ингибиторов тирозинкиназы.
д) Профилактика меланомы. Настороженность населения и знания о меланоме и свойствах УФ излучения полезны, но до сих пор существует большая дистанция между знанием и поведением. Первичная профилактики должна фокусироваться на безопасной инсоляции, включая ограничение воздействия УФ облучения, и предотвращении солнечных ожогов, в особенности среди детей и подростков, у которых риск наиболее высок. Рекомендуется избегать инсоляции в часы наибольшей солнечной активности, а также использовать широкополые шляпы и солнцезащитные препараты. Кроме того в разговоре с пациентами, их супругами и членами семьи важно подчеркнуть роль раннего выявления опухоли при регулярном самообследовании кожи, настороженности в отношении кожных новообразований и знания ранних проявлений меланомы. Целью вторичной профилактики является ранняя диагностика, значительно снижающая заболеваемость и смертность, связанные с меланомой.
- Рекомендуем далее ознакомиться со статьей "Наблюдение пациентов с меланомой и их диспансеризация"
Редактор: Искандер Милевски. Дата публикации: 10.11.2018

