Алгоритм обследования при подозрении порфирии у пациента
Ведение болезни состоит из комбинации тщательного сбора анамнеза (практически полный наследственный анамнез), клинического обследования, биохимического анализа на порфирины и их предшественников в моче, кале и крови. В специализированных лабораториях эти диагностические меры могут быть расширены до измерения специфичной ферментной активности в эритроцитах, лимфоцитах или фибробластах больных и членов их семей.
Молекулярные технологии в настоящее время обеспечивают наиболее точную диагностическую информацию, основываясь на выделении ДНК из периферической крови с последующим проведением методом полимеразной цепной реакции и автоматического секвенирования ДНК. Более того, эти методы позволяют проводить детализированный анализ генов и их функции и делают возможным генетическое консультирование больных и членов их семей.
Иногда возникают ситуации, когда полученные результаты могут оставаться сомнительными даже при использовании таких современных диагностических инструментов. В особенности это касается двойственных порфирий.
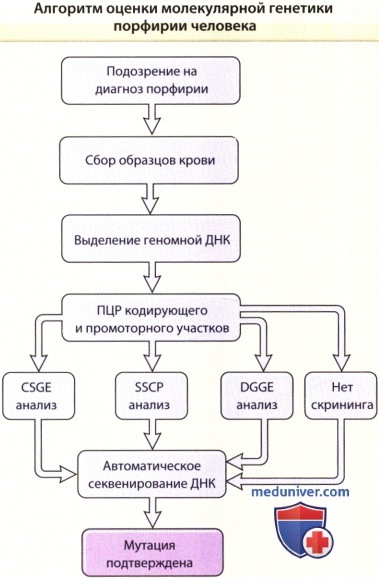
CSGE — конформационно-чув-ствительный гель-электрофорез; DGGE — денатурирующий градиентный гелевый электрофорез;
ПЦР — полимеразная цепная реакция; SSCP — полиморфизм конформации одноцепочечной ДНК.
а) Двойственные порфирии. При двойственных порфириях результаты лабораторных тестов могут указывать на сочетанный дефицит двух ферментов из цикла биосинтеза гема, либо у одного пациента, либо в пределах одной семьи. На настоящий момент есть данные почти о 15 пациентах и семьях с таким сочетанием признаков, что говорит о крайней редкости этих вариантов порфирии.
Большинство так называемых двойственных порфирий характеризуются комбинацией недостаточности уропорфириногендекарбоксилазы с недостаточностью порфобилиногендеаминазы, копропорфириногеноксидазы или протопорфириногеноксидазы, что неудивительно, поскольку распространенность ППК выше, чем распространенность любых других типов порфирии человека. У трех семей был установлен одновременный дефицит копрогеноксидазы и либо ПБГ-деаминазы, либо уроген-Ш-синтазы, либо АЛК-дегидратазы. У одного пациента с ВЭП дефицит уроген-Ш-синтазы сопровождался дефицитом уроген-декарбоксилазы.
До недавнего времени диагноз двойственной порфирии у всех пациентов и семей устанавливался на основании биохимического изменения порфиринов и/или их предшественников в моче и кале, а также ферментных исследований.
Пациенты с порфирией, у которых был проведен ДНК-анализ, явно продемонстрировали наличие мутаций в двух различных генах, кодирующих конкретный фермент в пути синтеза гема. Harraway и соавт. описали молодую пациентку, у которой развились симптомы на коже, подверженной солнечному излучению, и повышенная экскреция ПБГ с мочой. Однако диагноз ПП не мог быть подтвержден, и на основании результатов биохимического исследования ее мочи, кала и плазмы был предположен сочетанный дефицит ПБГ-деаминазы и уроген-декарбоксилазы. Последующее автоматическое секвенирование генов ПБГ-деаминазы (PBGD) и уроген-декарбоксилазы (UROD) выявило мутации в обоих этих генах, что подтвердило диагноз двойственной порфирии.
Akagi и соавт. изучали пациента с острыми приступами порфирии, сопровождавшимися повышенной экскрецией АЛК, ПБГ и КОПРО с мочой. Хотя эти признаки указывали на НП, авторы отметили также значительное повышение уровней АЛК и эритроцитарного цинк-ПРОТО, что говорило в пользу дефицита АЛК-дегидратазы. Последующее автоматическое секвенирование генов копроген-оксидазы (СРОХ) и АЛК-дегидратазы (ALAD) выявило мутации, вызывающие болезнь в обоих этих генах. Оба генетических дефекта были подтверждены опытами экспрессии in vitro, которые установили молекулярную основу двойственной порфирии у одного пациента, имеющего одновременный дефицит копроген-оксидазы и АЛК-дегидратазы.
Эти данные обращают особое внимание на то, что для пациентов, у которых биохимические и ферментологические исследования указывают на сочетание дефицита двух ферментов цикла синтеза гема, необходимо проводить молекулярно-генетический анализ соответствующих генов с целью идентификации мутаций, лежащих в основе индивидуального варианта двойственной порфирии.

б) Аномальный порфириновый профиль и сидеробластная анемия. Иногда сидеробластная анемия бывает связана с аномальными порфириновыми профилями. У этих пациентов встречается кожная фоточувствительность, напоминающая таковую при ЭПП, а затем у них развивается сидеробластная анемия. В некоторых случаях, оба состояния могут развиться с двухмесячным интервалом. У всех пациентов повышены уровни ПРОТО в эритроцитах и/или плазме; у многих также повышены уровни ПРОТО в кале. Активность феррохелатаз и, реже, АЛК-синтазы может быть снижена. Были описаны хромосомные аномалии, к которым относятся делеции в 18 и 20 хромосомах.
в) Молекулярно-генетическая стратегия при порфириях. При различных типах порфирий несоответствия между клиническими признаками и результатами биохимического обследования или ферментного анализа часто приводят к сомнительному или неправильному диагнозу. При острой порфирии, если точный диагноз не будет выставлен своевременно, это может иметь фатальные последствия.
Как только у пациента с порфирией выявлена мутация, определение асимптоматического гена у носителей среди членов семьи может быть легко осуществимо при использовании стандартных молекулярно-биологических методик. При острых порфириях определение таких «молчащих» носителей является первым и наиболее важным шагом для предотвращения жизнеугрожающих приступов. Генетический анализ является эффективным способом ранней постановки диагноза и, таким образом, увеличивает вероятность информированности пациентов и бессимптомных носителей из их семей о необходимости избегании провоцирующих факторов.
г) Животные модели и будущие возможности генной терапии. Для ЭПП и ПКК были описаны животные модели, которые предоставляют уникальные возможности исследовать патогенез данных типов порфирии in vivo и изучать осуществимость фенотипической реверсии путем генной терапии. Был достигнут ретровирусный генный транспорт человеческой кДНК феррохелатазы в дефицитные фибробласты пациентов с ЭПП. В преобразованных клетках каталитическая активность феррохелатазы повысилась с 7% до 550% от нормального уровня, была также продемонстрирована частичная метаболическая коррекция фенотипа. При ВЭП проводилась коррекция лежащего в основе ферментного дефекта в культивированных клетках путем ретровирусного генного транспорта, что привело к частичной нормализации состояния.
Избыточные уровни порфирина в преобразованных клетках снизились до нормальных. Эти исследования демонстрируют потенциал генной инженерии соматических стволовых клеток для лечения различных типов порфирии человека.

д) Выводы и перспективы. Порфирии, возникающие у человека, в большинстве случаев представлены пересекающимися клиническими и лабораторными признаками, что делает их точную диагностику сложной проблемой, особенно при острых состояниях. Кроме этого, клинические проявления и симптомы могут сильно различаться у разных пациентов и даже у одного и того же пациента в разные периоды жизни.
Биохимическое исследование порфиринов и их предшественников в моче и/или кале часто демонстрирует перекрестные результаты. Указанные методы, а также измерение ферментной активности в фибробластах или лимфоцитах являются в некотором роде неточными, и нередко выявляются показатели, которые не различаются между клинически здоровыми носителями патологических генов (так называемые «немые» носители) и нормальными контрольными исследованиями. Как только поставлен ДНК-обоснованный диагноз, пациенты и их семьи должны быть обеспечены генетическим консультированием и рекомендациями избегать провоцирующих факторов. В случае жизнеугрожающих острых приступов постановка генетического диагноза позволяет врачу немедленно начать адекватную терапию.
- Рекомендуем далее ознакомиться со статьей "Классификация амилоидоза"
Редактор: Искандер Милевски. Дата публикации: 2.11.2018

