Современное лечение пузырчатки
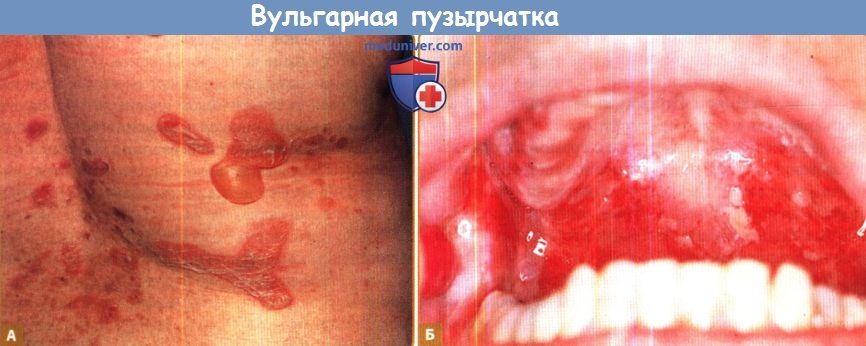
Несмотря на потенциально фатальный прогноз, в настоящее время отсутствуют одобренные FDA методы терапии. К лечению пузырчатки существуют различные подходы. Терапия вульгарной пузырчатки, согласно общепринятой точке зрения, должна осуществляться с момента возникновения первичных проявлений, даже если они носят ограниченный характер, так как в дальнейшем заболевание примет генерализованную форму и при отсутствии лечения будет иметь крайне неблагоприятный прогноз. Кроме того, осуществлять контроль заболевания в его начальной фазе легче, чем при генерализованном процессе. Вероятность летального исхода в случае задержки терапии может повышаться.
В свою очередь, листовидная пузырчатка способна в течение многих лет сохранять локализованный характер, и заболевание может иметь благоприятный прогноз даже при отсутствии системной терапии. В связи с этим для пациентов с листовидной пузырчаткой системная терапия не является обязательной — в этом случае лечебные мероприятия могут быть ограничены назначением местных кортикостероидов.
Тем не менее если поражение принимает генерализованную форму, терапевтический подход к листовидной пузырчатке в целом должен быть аналогичен таковому при вульгарной пузырчатке.
Недавно международная экспертная комиссия по пузырчатке предложила согласительное постановление относительно определений заболевания и результатов терапии. Кроме того, были разработаны клинические инструменты наблюдения за активностью заболевания. Стандартизация определений и параметров активности заболевания облегчит будущие клинические испытания методов терапии пузырчатки.
а) Кортикостероиды в лечении пузырчатки. Основным направлением терапии пузырчатки является применение системных глюкокортикоидов — преимущественно преднизона. До внедрения вспомогательной иммуносупрессивной терапии для лечения применялись очень высокие начальные дозы преднизона (> 2,0 мг/кг/день), хотя такие режимы ретроспективно ассоциировались со значительной морбидностью и смертностью в результате терапии. У многих пациентов контроль над заболеванием достигается при однократной ежедневной дозе 0,5-1,0 мг/кг/день, особенно в комбинации с вспомогательной иммуносупрессивной терапией, что способствует уменьшению количества осложнений и понижению смертности по сравнению с приемом более высоких доз кортикостероидов. У пациентов, которые не реагируют на первоначальную терапию или состояние их ухудшается, достигнуть контроля заболевания помогает разделение дозы на два-три приема.
Согласно рекомендациям согласительной комиссии, полная системная доза глюкокортикоидов составляет 1,5 мг/кг/день эквивалентно преднизону в течение трех недель. Следовательно, пациентам, чья ежедневная доза преднизона превышает примерно 100 мг, рекомендуется вспомогательная терапия, методы которой обсуждаются далее. Некоторые эксперты все еще рекомендуют применять для первоначального контроля торпидного заболевания возрастающие дозы преднизона (повышение на 50% каждые 1-2 недели до контроля над заболеванием или появления нежелательных побочных эффектов), суммарная ежедневная доза при этом достигает 240 мг.
При купировании активности заболевания, постепенно снижают до максимально низкой эффективной дозы. Минимально установленная ежедневная доза эквивалентна 10 мг преднизона. Хотя стандартные рекомендации отсутствуют, если активность заболевания можно полностью контролировать минимальными или более низкими дозами преднизона, то монотерапия глюкокортикоидами может быть адекватной с учетом сопутствующих заболеваний у пациента и противопоказаний к приему альтернативных иммуносупрессивных препаратов. Если у пациента наблюдаются постоянные рецидивы при приеме ежедневных доз преднизона в 10 мг или выше, рекомендуются вспомогательные иммуносупрессивные препараты. Интересно отметить, что преднизон контролирует возникновение пузырей в течение нескольких дней, при чем в этот период титр антител будет неизменным.
Возможное объяснение этого факта состоит в том, что преднизон может повышать синтез десмоглеинов или других молекул клеточной адгезии или изменять их посттранскрипционный процессинг, удлиняя период полураспада. Если IgG пузырчатки ингибирует десмосомы десмоглеинов, то преднизон может противодействовать этому явлению.
Топические кортикостероиды могут применяться в качестве монотерапии при легком течении заболевания или в качестве вспомогательной терапии для заживления новых очагов. Пациентам с поражением слизистых оболочек могут помочь эликсиры с глюкокортикоидами для полоскания или стоматологические накладные пластинки для нанесения кортикостероидных гелей или мазей класса I на десну. Дополнительно кортикостероиды класса I—IV применяются в качестве местной терапии для разрешения новых пузырей даже у пациентов, принимающих системные глюкокортикоиды.
б) Иммуносупрессия в лечении пузырчатки. Если для контроля заболевания требуются дозы глюкокортикоидов выше минимальных, или же имеются противопоказания для применения системных глюкокортикоидов, то для терапии пузырчатки применяются другие иммуносупрессивные препараты. Во многих случаях лечение часто начинают с одновременного приема иммуносупрессивного препарата и преднизона. Проспективные рандомизированные исследования показали, что такие иммуносупрессивные препараты, как микофенолата мофетил, азатиоприн и циклофосфамид оказывают стероидсберегающее действие; ретроспективные исследования отмечают уменьшение смертности при применении вспомогательных препаратов в сочетании со стероидами по сравнению с применением только стероидов.
Поскольку пациенты могут умереть вследствие осложнений терапии, важно строго контролировать всех пациентов на наличие потенциальных побочных действий, в частности аномалий в анализе крови, отклонений в лабораторных показателях функции печени и почек, заболевания желудочно-кишечного тракта, повышенного артериального давления, диабета, глаукомы, катаракты, остеопороза и инфекции.
При решении о приеме иммуносупрессивных препаратов, особенно в случае юных пациентов, следует учитывать потенциальное развитие злокачественных опухолей, которые ассоциируются с длительным приемом таких препаратов, а также риск бесплодия (для циклофосфамида) и тератогенности (для микофенолата мофетила, азатиоприна и циклофосфамида, которые при беременности относятся к препаратам категории D).
1. Азатиоприн. Азатиоприн исторически считается иммуносупрессивным препаратом первого выбора для пузырчатки, в ретроспективных исследованиях отмечается клиническая ремиссия примерно у 50% пациентов. В проспективном рандомизированном исследовании терапии высокими дозами метилпреднизалона (2,0 мг/кг/день) плюс азатиоприн (2,0 мг/кг/день), 72% пациентов достигли клинической ремиссии в среднем за 74 дня, хотя у 33% отмечались значительные побочные эффекты терапии, в том числе гипергликемия, головокружение, аномальные функциональные пробы печени и инфекция.
Азатиоприн является про-лекарством, которое преобразуется в активные метаболиты меркаптопурина, тиогуанина и тиоинозина, частично под действием тиопуриновой метилтрансферазы (ТПМТ), фермента уровни которого в популяции значительно варьируют. У 89% представителей европеоидной расы уровни ТПМТ нормальные или высокие, у 11% промежуточные, и у 0,3% отмечается дефицит ТМПТ, причем к последней группе относятся пациенты, которые не переносят терапию азатиоприном.
Кроме того, у 1%-2% лиц европеоидной расы может отмечаться сверхвысокий уровень ТПМТ, который коррелирует как с устойчивостью к терапии, так и с повышенной гепатотоксичностью вследствие избыточного производства метаболитов. В целом, около 5% пациентов не будут переносить терапию азатиоприном, хотя корреляция между генотипом и фенотипом не является безусловной.
У пациентов с нормальным уровнем ТПМТ согласованным критерием неэффективности терапии является отсутствие ответа на лечение в дозе 2,5 мг/кг/сут. в течение 12 недель. Однако практические трудности связаны с тем, что не все лаборатории определяют уровень ТРМТ. Кроме того, поскольку пациенты с нормальным уровнем ТРМТ также не застрахованы от токсических эффектов азатиоприна, целесообразно начинать терапию всем больным с низких доз (например, 50-100 мг/сут.) и титровать их до достижения клинической ремиссии, целевой дозы в 2,5 мг/кг/сут. или непереносимых побочных эффектов.
Необходимо осуществление частого гематологического и печеночного мониторинга, особенно в течение первых 8-12 недель, поскольку возможны отсроченные токсичные эффекты за счет аккумуляции метаболитов.
2. Микофенолта мофетил. Микофенолата мофетил также считается иммуносупрессивным препаратом первой линии для пузырчатки. В 2006 году FDA присвоила микофенолату мофетилу статус орфанного лекарства, что повысило шансы на разрешение нового лекарства к применению. Типичные дозировки составляют 30-40 мг/кг/день в два приема (2,0-3,0 г/день), хотя у некоторых пациентов, в частности у пожилых людей контроля над заболеванием можно достигнуть при дозах 1,0 г/день. В серии случаев было показано, что микофенолата мофетил быстро понижал титры антител и уменьшал активность заболевания даже у пациентов, которые не реагировали на азатиоприн.
Проспективное рандомизированное исследование по сравнению метилпреднизолона (2,0 мг/кг/день) с азатиоприном (2,0 мг/кг/день) и микофенолата мофетилом (2,0 г/день) у пациентов с пузырчаткой показало наступление клинической ремиссии у 72% пациентов из группы азатиоприна и у 95% пациентов из группы с микофенолатом мофетилом в среднем через 74 и 91 день соответственно. У 19% пациентов отмечались значительные побочные эффекты при приеме микофенолата мофетила, в группе азатиоприна они составили 33%. Ни одно из этих различий не было статистически значимым. Еще одно проспективное рандомизированное исследование показало, что азатиоприн был значительно эффективнее микофенолата мофетила в качестве стероидсберегающего препарата, однако в исследовании сравнивалась полная доза азатиоприна (2,5 мг/кг/день) с неполной дозой микофенолата мофетила (2,0 г/день).
При применении препарата необходима осторожность, поскольку фатальная инфекция и сепсис отмечались у 2-5% реципиентов трансплантатов, получавших микофенолата мофетил, а при постмаркетинговом контроле был отмечен повышенный риск инфекции с реактивацией цитомегаловируса, вируса опоясывающего герпеса, атипичного микобактериального туберкулеза и вируса Джона Каннингема (John Cunningham [JC]) при прогрессирующей многоочаговой лейкоэнцефалопатии. Интересно отметить, что микофенолата мофетил может оказывать защитное действие протий инфекции Pneumocystis carinii.
3. Циклофосфамид в лечении пузырчатки. Циклофосфамид, хотя более токсичный, чем азатиоприн или микофенолата мофетил, считается очень эффективным препаратом для контроля тяжелой степени заболевания; в одном сообщении у 19 из 23 пациентов с пузырчаткой была достигнута полная ремиссия в среднем за 8,5 месяцев. В нескольких небольших сериях случаев оценивались различные режимы приема циклофосфамида при пузырчатке, в том числе ежедневный прием внутрь (1,1— 2,5 мг/кг/день), ежедневный прием внутрь (50 мг), чередующийся с высокими дозами внутривенного дексаметазона и циклофосфамида, и иммуноаблятивный внутривенный циклофосфамид. Все методы оказывали эффективное действие в течение короткого периода времени, но ни один не привел к излечению.
Значительные побочные эффекты, в том числе гематурия, инфекция и переходно-клеточная карцинома мочевого пузыря наблюдались при приеме высоких доз, хотя в одном исследовании с более низкой ежедневной дозой циклофосфамида (1,1-1,5 мг/кг/день) профиль безопасности существенно не отличался от такового других иммуносупрессивных препаратов. С учетом риска бесплодия, циклофосфамид в целом не считается препаратом первого выбора для лечения вульгарной пузырчатки.
4. Дапсон. В серии случаев и рандомизированного, двойного слепого исследования показал тенденцию к эффективности в качестве стероидсберегающего средства при поддерживающей терапии вульгарной пузырчатки, хотя эти результаты не были статистически значимыми. Дапсон может применяться в комбинации с другими иммуносупрессивными препаратами, в частности, ритуксимабом (обсуждается далее), при этом он обладает дополнительным профилактическим действием против Pneumocystis pneumonia.
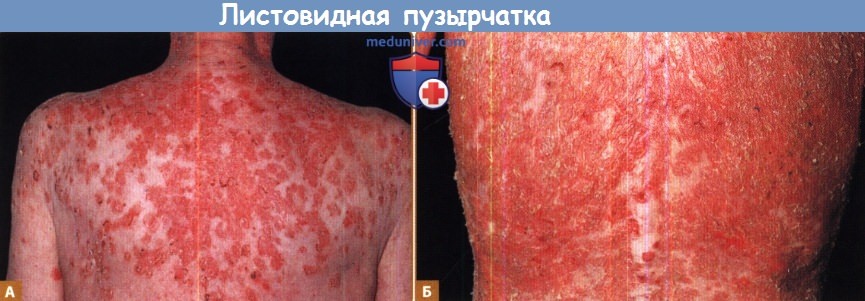
А. Шелушащиеся, покрытые коркой очаги на верхней части спины. Б. Эксфолиативная эритродермия в результате слияния очагов.
в) Дополнительные методы лечения пузырчатки. Если большинство обсуждавшихся выше стандартных методов терапии оказались не эффективными, можно применить дополнительные методы терапии.
1. Ритуксимаб при пузырчатке. Очень эффективным для лечения пузырчатки, устойчивой к традиционной терапии, является моноклональное анти-CD20-антитело ритуксимаб, который применяется для терапии В-клеточных лимфом. У пациентов с пузырчаткой это моноклональное антитело, вероятно, воздействует на В-клетки, предшественники производящих антитела плазматических клеток. В-клетки также участвуют в процессинге аутоантигенов и их презентации Т-клеткам, которые «помогают» стимулировать ответ аутоантител. Ритуксимаб вводится внутривенно капельно в дозе 375 мг/м2 один раз в неделю в течение четырех недель. Альтернативно может применяться режим дозирования для ревматоидного артрита (1000 мг внутривенно в 1-й и 15-й день). Курс терапии можно повторить через примерно 6 месяцев для пациентов с более торпидным заболеванием, хотя было показано, что один курс ритуксимаба оказывает высокоэффективное действие: у 86% пациентов отмечается полная ремиссия в течение 34 месяцев или дольше.
Активность заболевания обычно снижается в течение 1-2 месяцев после курса терапии. Некоторые эксперты считают ритуксимаб терапией выбора для тяжелой пузырчатки, не поддающейся контролю кортикостероидами и азатиоприном или микофенолата мофетилом или в случае противопоказаний для назначения кортикостероидов. Однако при терапии ритуксимабом наблюдались фатальные инфекции, в том числе пневмония, вызванная Pneumocystis, реактивация гепатита В, инфекция или реактивация JC-вируса, вызывающая прогрессирующую многоочаговую лейкоэнцефалопатию. Хотя эти осложнения редкие, некоторые специалисты рекомендуют проводить профилактику Pneumocystis в течение одного года после инфузии ритуксимаба.
2. Внутривенный иммуноглобулин. Еще одним методом уменьшения аутоантител в сыворотке является внутривенное применение γ-глобулина (IVIg) в высоких дозах. IVIg функционирует путем насыщения пула циркулирующего неонатального Fc-рецептора, повышая таким образом катаболизм сывороточных антител пациента, в том числе и патогенных аутоантител. Эта терапия полезна в качестве вспомогательной тем пациентам с пузырчаткой, которые не отвечают на традиционную терапию. Мультицентровое, рандомизированное, двойное, слепое исследование с плацебо-контролем подтвердило эффективность этой терапии при пузырчатке, но она дорогостоящая и, вероятно, требует постоянных инфузий для поддержания ремиссии. Возможны также значительные побочные эффекты, в том числе инсульт, тромбоз глубоких вен и почечная недостаточность при применении препаратов, содержащих сукрозу.
В некоторых центрах IVIg при меняется для первоначального купирования пузырей у тяжело больных пациентов, поскольку эта терапия не приводит к риску инфекций в такой степени, как кортикостероиды и иммуносупрессоры. IVIg применялись также в комбинации с ритуксимабом, хотя неясно, является ли эта комбинация более безопасной и эффективной, чем применение IVIg в качестве монотерапии.
3. Плазмаферез при пузырчатке. Плазмаферез иногда применяется при тяжелом течении пузырчатки или при отсутствии эффекта от комбинации преднизона и иммуносупрессора. Хотя в одном контролируемом исследовании плазмаферез оказался неэффективным, в других исследованиях отмечалось, как понижение сывороточных уровней аутоантител пузырчатки, так и уменьшение активности заболевания. Сообщалось, что плазмаферез плюс внутривенная пульс-терапия циклофосфамидом приводила к ремиссиям вульгарной пузырчатки. Для максимальной эффективности, вероятно, необходимо проводить плазмаферез пациентам, принимающим иммуносупрессивные препараты для предупреждения «эффекта рикошета», который может произойти после отмены IgG. Применялась также иммуноадсорбция протеина А, при которой IgG селективно удаляется из плазмы.
4. Внутривенная пульс-терапия высокими дозами глюкокортикоидов. Внутривенная пульс-терапия метилпреднизолоном в дозе 250-1000 мг, назначаемая в течение 4-5 последовательных дней путем примерно 3-часовой инфузии, может привести к длительной ремиссии и уменьшить общую дозу глюкокортикоидов, необходимую для контроля заболевания. Хотя целью такой терапии является уменьшение частоты осложнений вследствие длительного применения стероидов, она может вызывать все обычные для глюкокортикостероидов осложнения, а также сердечную аритмию с внезапной смертью, поэтому по поводу ее применения существует противоречивые мнения. Кроме того, контролируемое исследование показало, что вспомогательная пульс-терапия пероральным дексаметазоном вдобавок к стандартной терапии преднизолоном и азатиоприном, не оказала благоприятного эффекта пациентам с вульгарной пузырчаткой. Возможно, более низкие дозы преднизона, разделенные на несколько приемов, могут оказать такое же действие с меньшими побочными эффектами.
В целом наблюдается значительный прогресс в терапевтическом арсенале для лечения вульгарной пузырчатки с того времени, как до внедрения глюкокортикоидов она была болезнью с летальным исходом. Благодаря этому прогрессу, ряд «надгробных камней», наблюдаемый в гистологической картине вульгарной пузырчатки, больше не соответствует ее прогнозу.
- Рекомендуем далее ознакомиться со статьей "Причины и механизм развития паранеопластической пузырчатки"
Оглавление темы "Пузырчатка.":
