Клетки участвующие в патогенезе псориаза
1. Т-клетки при псориазе. В 1984 г. было показано, что появление псориатических очагов совпадало с притоком в эпидермис и активизацией Т-клеток. Вскоре после этого было также установлено, что разрешению псориаза в ходе фототерапии предшествовало исчезновение Т-клеток, преимущественно из эпидермиса. Высокоэффективным против псориаза оказался циклоспорин А (ЦсА), и этот эффект, как было обнаружено, объяснялся в первую очередь блокировкой Т-клеток, а не кератиноцитов.
Кроме того, при трансплантации костного мозга псориаз развивался или излечивался в зависимости от того, кто был болен, донор или реципиент. Роль Т-клеток при псориазе была продемонстрирована в 1996 г., когда было показано, что псориатический процесс можно индуцировать введением активированных аутологичных Т-клеток в непораженную псориатическую кожу, пересаженную мышам с тяжелым комбинированным иммунодефицитом.
Существующие данные указывают на то, что Т-клеточный ответ не активируется суперантигенами, а является антиген-специфическим, поскольку в псориатических бляшках неизменно выявляются клональные популяции CD4+ и CD8+ T-лимфоцитов. Вместе с тем большая часть Т-клеток в псориатической бляшке не проходит клональную экспансию и может накапливаться в ответ на изменение ее цитокинового состава. Фактически нет данных за вовлечение В-клеток или антител в патогенез псориаза.
Наиболее изученными Т-клетками являются популяции CD4+ и CD8+. Эти клетки имеют фенотип клеток памяти (CD45RO+) и экспрессируют кожный лимфоцитарный антиген (CLA — cutaneous lymphocyte antigen), лиганд Е-селектина, который избирательно экспрессируется на клетках капилляров кожи и поэтому обеспечивает им доступ в кожу. Т-клетки популяции CD8+ расположены преимущественно в эпидермисе, в то время как Т-клетки популяции CD4+ — в верхних слоях дермы.
Цитокиновый профиль псориатических очагов богат интерфероном-гамма (ИНФ-у) и указывает на Т-хелперную (по типу Тh1) поляризацию клеток CD4+ и Т-цитотоксическую (по типу Тс1) поляризацию CD8+ клеток. Также в псориатических очагах обнаруживают две другие субпопуляции CD4+ Т-лимфоцитов, дифференцировка которых стимулируется ИЛ-23 и которым свойственна продукция ИЛ-17 (Тh17-клетки) и/или ИЛ-22 (Th22 — клетки). Было показано, что они играют важную роль в поддержании хронического воспаления как при псориазе, так и при других аутовоспалительных заболеваниях. В то время как большая часть CD4+T клеток относится к подтипу Тh1, приблизительно 20% из них вырабатывают ИЛ-17 (Th 17) и 15% вырабатывают ИЛ-22 (Th22).
Также при псориазе выявляют эпидермальные CD8+ Т-лейкоциты, которые вырабатывают ИФН-у (Тс1), ИЛ-17 (Thl7) и ИЛ-22 (Th22).
Эти субпопуляции Т-лимфоцитов обладают известной функциональной пластичностью, и были описаны переходы клеток от Тh17 к Тc1 и от Тh17 к Тh1. У мышей большая часть Тh17-клеток также вырабатывает ИЛ-22, который после внутрикожной инъекции ИЛ-23 участвует в активации процессов воспаления в дерме и гиперплазии эпидермиса. В то же время у человека это дублирование функций существенно менее выражено, и можно четко выделить популяции Тh17 и Тh22-клеток.
Регуляторные Т-клетки подавляют иммунные реакции на специфические антигены и определяют не только ограничение интенсивности успешного ответа на патогенные факторы, но и иммунологическую толерантность.
Существует несколько популяций Т-регуляторов, из них лучше всего описана субпопуляция CD4+CD25+. В недавно выполненном исследовании показаны нарушение ингибиторной функции и невозможность подавления пролиферации эффекторных Т-клеток в этой популяции, вероятно в связи с содержанием большого количества ИЛ-6, который вырабатывается эндотелиальными, дендритными и ТЫ7 -клетками.
NKT-клетки (англ -Natural killer Т cells, естественные киллеры-Т-клетки) представляют собой гетерогенную популяцию Т-лимфоцитов, которая отличается ко-экспрессией Т-клеточных рецепторов и маркеров линейки NK-клеток, например CD16, CD56, CD57, CD94 и CD161. В отличие от традиционных Т-клеток, NKT-клетки распознают гликолипидные антигены, в составе антиген-презентирующей молекулы CD1d, сходной с МНС 1 класса. NKT-клетки составляют лишь малую часть лимфоцитов.
Тем не менее, их способность быстро секретировать большие количества цитокинов, включая ИФН-у, ИЛ-4, ИЛ-2, ИЛ-5, ИЛ-10, ИЛ-13, ИЛ-17 и ФНО-а, делает их потенциально важными регуляторами дифференцировки Т-клеток в участках воспаления. Хотя число NKT-клеток в псориатических очагах выше, чем во внешне неизмененной коже или у здоровых людей, их точная роль в развитии псориаза остается неясной.
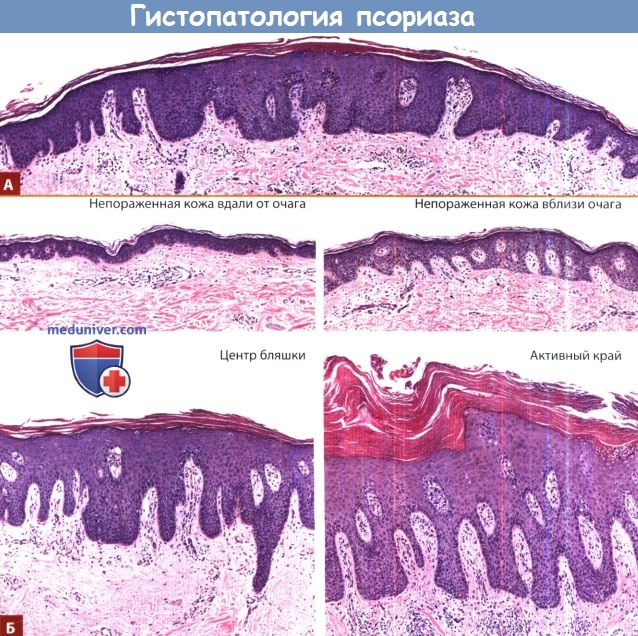
А. Небольшая псориатическая папула. На переходе от периферии к центру очага нарастает утолщение эпидермиса с удлинением межсосочковых клиньев,
возрастает расширение и извилистость сосудов и увеличивается мононуклеарный клеточный инфильтрат.
Обратите внимание на то, что структура рогового слоя в форме переплетения изменяется на компактную структуру с потерей зернистого слоя в центре очага (4-мм пункционная биопсия, гематоксилин-эозин, масштаб: 100 μМ).
Б. Сравнение непораженной и пораженной кожи. 4 биопсии были взяты у одного и того же пациента, которому принадлежит и микропрепарат А, в один и тот же день.
Образец «непораженной кожи вдали от очага» был получен с верхней части спины в 30 см от ближайшего видимого очага псориаза.
Образец «непораженной кожи вблизи очага» был взят на расстоянии 0,5 см от края псориатической бляшки размером 20 см, которая, по словам пациента, существует уже несколько лет.
Микропрепарат кожи из «центра бляшки» принадлежит сравнительно неактивному (менее красному и шелушащемуся) участку в центре этой бляшки.
Кожа из «пораженного края» очага была взята из активного (более красного и шелушащегося) участка в пределах 1 см внутри края этой же псориатической бляшки.
Сравнивая непораженную кожу вдали и вблизи очага, обратите внимание на то, что вблизи очага наблюдается увеличение толщины кожи и раннее удлинение эпидермальных выростов,
расширение и ранняя извилистость кровеносных сосудов, а также повышенное количество мононуклеарных клеток в верхней дерме, причем многие из них расположены вокруг сосудов.
У данного пациента в непораженной коже вблизи очага наблюдается повышенная частота дискератотических кератиноцитов, ранее этот результат отмечался на периферии псориатических очагов.
При сравнении менее активной и более активной зон псориатической бляшки обращает на себя внимание тот факт,
что в более активной зоне наблюдается увеличение мононуклеарного дермального инфильтрата, усиление гиперкератоза и паракератоза и микроабсцессы Мунро (4-мм пункционная биопсия, гематоксилин-эозин, масштаб: 100 μМ).
2. Естественные киллеры при псориазе. Как и NKT-клетки, естественные киллеры являются главными продуцентами ИФН-у и служат переходным звеном между врожденным и приобретенным иммунитетом. ЕК-клетки присутствуют при псориазе и могут спровоцировать появление псориатических очагов в модели ксенографта. ЕК-клетки частично регулируются рецепторами, содержащими иммуноглобулин (Ig)-подобные домены, которые распознают молекулы HLA-C и другие молекулы ГКГ класса I.
Рецепторы ЕК-клеток, содержащие Ig-подобные домены, представляют собой семейство из примерно 15 тесно сцепленных генов, расположенных на хромосоме 19q13.4, причем одни из них стимулируют, а другие ингибируют активизацию ЕК-клеток. Недавно была обнаружена ассоциация генов этих рецепторов с псориазом и псориатическим артритом. Было высказано предположение, что риск развития псориатического артрита определяется балансом между активирующим и ингибирующим генотипами.
Хотя и выглядит привлекательным предположение о том, что связь псориаза с наличием HLA-Cw6 может отражать KIR-опосредованное (KIR — иммуноглобулин-подобный рецептор естественных киллеров — killer cell immunoglobulin-like receptor) нарушение регуляции числа естественных киллеров, известно, что определенное число других HLA-C аллелей распознают тот же самый ингибирующий рецептор (KIR2DL1), в том числе HLACw2, HLA-Cw4, HLA-Cw5, HLA-Cw15 и HLACw17. Поэтому нельзя описать роль HLA-Cw6 в псориазе только лишь распознаванием KIR.
3. Дендритные клетки при псориазе. Методы лечения, направленные непосредственно против ключевых костимулирующих молекул, которые экспрессируются «профессиональными» антигенпрезентирующими дендритными клетками (ДК), значительно улучшали течение псориаза. Отсюда можно предположить, что Т-клетки в псориатических очагах находятся в постоянном контакте с ДК, которые играют определенную роль как в прайминге адаптивного иммунного ответа, так и в индукции аутотолератности. Были идентифицированы несколько популяций ДК, причем многие из них были обнаружены в зрелом состоянии в пределах псориатических очагов.
Хотя считается, что эти клетки занимают центральное место в патогенезе псориаза, специфическая роль каждой из популяций остается пока неясной.
в) Клетки Лангерганса. Клетки Лангерганса (КЛ) обычно характеризуются наличием лангерина и поверхностным фенотипом Cd1a и считаются незрелыми дендритными клетками (ДК). Подтверждено, что КЛ играют роль антиген-презентирующих клеток при контактном дерматите, однако их значение при псориазе остается неясным. В то время как плотность КЛ в очагах псориаза, определяемая как количество клеток на единицу площади, снижается, число этих клеток на единицу длины эпидермиса в нормальной, неизмененной коже и в очагах псориаза сходно.
ДК без характерных гранул Бирбека, но с молекулами созревания DCLAMP, которые обнаруживаются в дерме псориатических очагов, могут происходить из эпидермальных или дермальных незрелых ДК.
Недавно было отмечено, что клетки Лангерганса (КЛ) избирательно стимулируют дифференцировку Тh22-клеток, что роднит их с ДК дермы. Интересно, что миграция КЛ в ответ на действие воспалительных цитокинов существенно изменяется в неизмененной коже больных псориазом по сравнению со здоровыми, особенно при псориазе 1 типа (с ранним началом).
г) Дермальные дендритные клетки при псориазе. Дендритные клетки дермы не вырабатывают маркеров активации в нормальной коже в покое и в этом контексте они могут расцениваться как отличный от других тип незрелых ДК, сходный с миелоидными незрелыми ДК, которые выявляются в других тканях. Исследования с иммунофенотипированием показали, что популяция дермальных ДК достаточно комплексная, и что в псориатических очагах отмечается выраженное увеличение числа и созревание дермальных ДК.
В настоящее время принято считать, что клетки фактор ХIIIа+*, которые изначально были обнаружены по выраженной экспрессии МНС класса II и/или фактора ХIIIа, являются скорее макрофагами, чем ДК, и что наиболее надежный маркер ДК дермы миелоидного происхождения — CD11с. В псориатических очагах обнаружено три типа ДК миелоидного происхождения (CD11с). Во-первых, это популяция «резидентных» клеток дермы, которые обнаруживаются и в нормальной коже. Эти CD11c/CD1с ДК составляют около 10-15% всех ДК в псориатическом очаге Эти клетки более зрелые по сравнению с воспалительными ДК, но менее — в сравнении с полностью зрелыми ДК.
Вторую популяцию составляют зрелые ДК, у которых имеются маркеры DC-LAMP или CD83. ДК DC-LAMP формируют большие скопления с Т-клетками в дерме, в то время как ДК CD83 расположены более диффузно. Высказывалось предположение, что полностью зрелые ДК могут быть поддерживающей силой хронической активации Т-лимфоцитов, и что по своим характеристикам эти клетки очень сходны с таковыми в составе лимфатических узлов. Третья популяция ДК миелоидного происхождения — воспалительные ДК, которые имеют CD11c+/CD1c- и являются менее зрелыми по сравнению с CD1c+ субпопуляцией.
Эти клетки вырабатывают ИЛ-23 и вероятно способствуют дифференцировке Th 17. Приблизительно 80-90% всех ДК в псориатических очагах составляют эти сравнительно незрелые воспалительные ДК, причем, что интересно, общее число этих клеток может превышать число Т-клеток в очагах. Субпопуляция этих воспалительных ДК вырабатывает большое количество ФНО-а и iNOS и по аналогии с такими клетками у мышей получила название «Т1Р-ДК» (англ — TNF-a (ФИО) и iNOS — продуцирующие ДК).
Как было недавно установлено при генетическом анализе, количество TIP-ДК в псориатических очагах возрастает до 30 раз. По-видимому, эта популяция клеток обладает существенной пластичностью, поскольку цитокиновая микросреда при атопическом дерматите способствует появлению дермальных ДК, которые путем хемотаксиса привлекают иную субпопуляцию Т-клеток, нежели та, что обнаруживается при псориазе.
д) Воспалительные дендритные эпидермальные клетки. Воспалительные дендритные эпидермальные клетки (ВДЭК) считаются незрелыми дендритными клетками моноритарного происхождения. От клеток Лангерганса они отличаются отсутствием гранул Бирбека и более слабой экспрессией CD1а. ВДЭК, в отличие от КЛ, практически отсутствуют в здоровой коже, но их количество явно повышено в эпидермисе активных псориатических очагов, а также при множестве других воспалительных дерматозов.
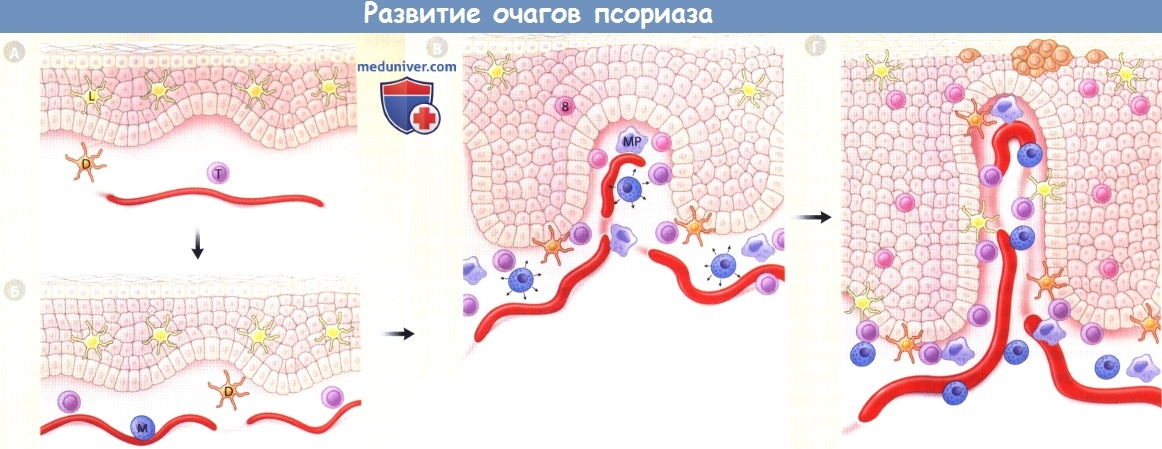
Нормальная кожа здорового человека (иллюстрация А) содержит в эпидермисе клетки Лангерганса, незрелые дентритные клетки (Д) и Т-клетки памяти кожного хоуминга в дерме (Т).
Во внешне здоровой коже больного псориазом (иллюстрация Б) наблюдаются слегка расширенные и извилистые капилляры и незначительное увеличение количества дермальных мононуклеарных и тучных клеток (М).
Эпидермис обычно слегка утолщен. При хроническом бляшечном псориазе интенсивность этих изменений определяется удаленностью от сформировавшегося очага.
Для переходной зоны развивающегося очага (иллюстрация В) характерно прогрессирующее расширение капилляров и повышение их извилистости,
а также увеличение количества тучных клеток, макрофагов (МР) и Т-клеток, наряду с усилением дегрануляции тучных клеток (стрелки).
Толщина эпидермиса возрастает, а эпидермальные выросты все больше удлиняются, межклеточные пространства расширяются, наблюдается транзиторный дискератоз, неравномерная потеря зернистого слоя и паракератоз.
Клетки Лангерганса (L) начинают покидать эпидермис, и туда начинают проникать воспалительные дендритные эпидермальные клетки (!) и Т-клетки популяции CD8+ (8).
Для полностью сформировавшегося очага (иллюстрация Г) характерны извилистые и предельно расширенные капилляры с 10-кратным увеличением кровотока,
многочисленные макрофаги под базальной мембраной и количественный рост дермальных Т-клеток (в основном CD4+), контактирующих с созревающими дермальными дендритными клетками (D).
В эпидермисе зрелого очага отмечается резкое (примерно 10-кратное) увеличение гиперпролиферации кератиноцитов, достигающей нижних надбазальных слоев; выраженное,
но не обязательно равномерное отсутствие зернистого слоя с уплотнением расположенного над ним рогового слоя и паракератозом;
рост количества Т-клеток популяции CD8+ и скопление нейтрофилов в роговом слое (микроабсцессы Мунро).
е) Плазмоцитоидные дендритные клетки. Плазмоцитодные дендритные клетки (пДК) неэффективно презентируют антигены Т-клеткам. Однако они регулируют воспаление и исходно связаны с адаптивным иммунитетом, вырабатывая при активизации большие количества ИНФ-α. В здоровой коже пДК отсутствуют, но их количество значительно возрастает как в пораженной, так и в непораженной коже больных псориазом, при этом они активируются только в пораженной коже. Интересно что, ингибиция пДК предотвращала развитие псориаза, что было показано на модели ксенографта у мышей.
И наоборот, имиквимод, который, как сообщается, ухудшает течение псориаза, вероятно, действует через эту систему ИНФ типа I, связываясь с толл-подобным рецептором 7 на пДК. Хотя ИФН-a, как оказалось, и играет роль в развитии псориатических очагов, его роль в прогрессировании хронического вульгарного псориаза остается неуточненной.
1. Тучные клетки. Тучные клетки на протяжении уже давно были обнаружены в ранних и развившихся псориатических очагах, характеризуются выраженной дегрануляцией при эруптивной (каплевидной) форме псориаза и при очагах, возникающих после отмены местных глюкокортикоидов. Интересно, что выработка тучными клетками ранее и вновь синтезированных медиаторов подавляется ЦсА и такролимусом, что позволяет предполагать, что антипсориатическое действие этих препаратов может быть реализовано не только через Т-лимфоциты, но и через тучные клетки. Недавно было показано, что именно тучные клетки вырабатывают больше всего ИЛ-17 как в синовиальной оболочке сустава при ревматоидном артрите, так и в псориатическом очаге.
2. Макрофаги. Макрофаги обильно инфильтрируют как ранние, так и развитые псориатические очаги. Недавно было показано, что CD163 может служить надежным маркером макрофагов кожного происхождения, и, как упоминалось ранее, эти клетки также вырабатывают фактор XIIIа. Популяцию CD11с—, CDla+, CD68+ макрофагов обнаруживают сразу под базальной мембраной, рядом с пролиферирующими кератиноцитами, которые вырабатывают макрофагальный хемокин МСР-1 (CCL2). Эти фагоцитарно-активные клетки могут участвовать в образовании фенетраций (отверстий) в базальной мембране. Недавние исследования на мышах в двух различных моделях псориаз-зависимой и независимой от Т-клеток — показали, что избирательная элиминация макрофагов приводила к быстрому улучшению очагов.
Эти новые данные позволяют предположить ключевую роль макрофагов в патогенезе псориаза, по крайней мере, через производство фактора некроза опухоли (ФНО-а), iNOS и ИЛ-23.
3. Нейтрофилы. Хотя в верхнем эпидермисе псориатических очагов нейтрофилы обычно присутствуют, они появляются в поздний период их развития. Количество нейтрофилов весьма вариабельно, а роль в патогенезе псориаза неясна. В недавних исследованиях на тех же моделях, которые применялись для изучения макрофагов, было показано, что в развитии псориатических очагов нейтрофилы, вероятно, не участвуют.
4. Кератиноциты. Кератиноциты являются основными производителями провоспалительных цитокинов и факторов роста, а также других медиаторов воспаления, в частности эйкозаноидов и медиаторов врожденного иммунитета, таких как кателицидины, дефензины и протеины S100. Псориатические кератиноциты участвуют в альтернативном механизме дифференцировки кератиноцитов, который называют регенеративным созреванием. Регенеративное созревание при псориазе активизируется в ответ на иммунологическую стимуляцию, но механизм, посредством которого это происходит, в настоящее время неизвестен.
5. Другие типы клеток. Другие типы клеток, такие как эндотелиальные клетки и фибробласты, также вероятно являются участниками патологического процесса. Эндотелиальные клетки активизированы в значительной степени в развивающихся и зрелых очагах псориаза и, в дополнение к обеспечению 10-кратного возрастания кровотока в очаге, играют главную роль в контроле над притоком лейкоцитов и сывороточных протеинов в псориатический очаг. Фибробласты поддерживают пролиферацию кератиноцитов посредством паракринного эффекта, причем при псориазе этот процесс усиливается. Фибробласты вырабатывают многие хемотаксические факторы и поддерживают миграцию Т-клеток из псориатических очагов. Таким образом, фибробласты также могут быть тесно связаны с псориазом, поскольку регулируют локализацию Т-клеток.
- Рекомендуем далее ознакомиться со статьей "Сигнальные молекулы в патогенезе псориаза"
Оглавление темы "Псориаз.":- У кого возникает псориаз? Эпидемиология
- Механизмы развития очагов псориаза. Патогенез
- Клетки участвующие в патогенезе псориаза
- Сигнальные молекулы в патогенезе псориаза
- Генетика в патогенезе псориаза
- Клиника и алгоритм диагностики псориаза
- Все болезни с которыми необходимо дифференцировать псориаз списком
- Осложнения псориаза у пациентов
- Прогноз и течение псориаза

