Патогенез (механизмы развития) вирусных нейроинфекций
Многие опасные нейроинфекции (менингит, энцефалит и т.д.) имеют вирусное происхождение. Вирусы обладают целым рядом уникальных свойств. Они способны инфицировать ЦНС, не вызывая видимых воспалительных реакций; реплицироваться в клетках на протяжении жизни индивида, не приводя к явным нарушениям функций целостного органа, а также могут вызывать повреждение ткани и затем полностью исчезать из организма.
Иммунопатологтический процесс, ассоциированный с вирусной нейроинфекцией, описан R. Dorries.
При попадании в организм и после нескольких циклов репликации вирус достигает ЦНС (обычно гематогенным путем). После прохождения вирусом ГЭБ клетки ЦНС инфицируются; происходит репликация вируса в клетках мозга, что приводит к активации окружающей микроглии.
Локальная продукция ИФН-а и ИФН-b вызывает экспрессию антигена (АГ) комплекса HLA на клетках ЦНС, а микроглия начинает поглощать клеточные обломки, аккумулируемые за счет реализации вирус-индуцированных цитопатогенетических эффектов. После фагоцитоза микроглия становится более активированной, ее клетки позитивно регулируют молекулы комплекса HLA, приобретают способность к представлению АГ и секретируют хемокины. Это инициирует активацию молекул адгезии на смежных эндотелиальных клетках ГЭБ. Трансмиграции активированных Т-лимфоцитов через ГЭБ сопутствует взаимодействие с АГ-презентирующими клетками, представляющими соответствующие пептиды в контексте АГ комплекса HLA.
CD8+ лимфоциты появляются в инфицированной вирусом ткани одними из первых среди мононуклеарных клеток (их индукция и привлечение находятся под глубоким влиянием NK-клеток). Последние, после инфицирования вирусом, секретируют ИФН-у, а этот цитокин стимулирует CD8+ лимфоциты и переключает иммунный ответ на Th1-тип CD4+ Т-клеточно-доминирующей реакции.
Вслед за CD8+ лимфоцитами проникающие в ткани Thl/CD4+ Т-клетки вступают в контакт с местными АГ-представляющими клетками. Это приводит к колоссальной позитивной регуляции (активации) молекул комплекса HLA, а также к секреции большего количества хемотаксических и токсичных субстанций.
Все возрастающее число воспалительных клеток (включая макрофаги/микроглию, а также конечные антителопродуцирующие плазматические клетки) привлекается в место вирусного инфицирования. Все захваченные клетки преимущественно представляют собой окончательно дифференцированные популяции, которым предстоит войти в процесс апоптоза во время или вскоре после выполнения своих эффекторных функций.
Клинические последствия и влияние эффекторной фазы на дальнейшее течение вирусной инфекции зависят от соотношения и «настройки» участвующих в процессе лимфоидных популяций. Как правило, любая задержка в рекрутировании эффекторных лимфоцитов в ткани или несбалансированное сочетание лимфоидных субпопуляций позволяют вирусу проникнуть в ЦНС, что, в свою очередь, вызывает тяжелые иммуноопосредованные эффекты со стороны тканей (помимо самой болезни).
Запоздавший или частично дефицитарный ответ иммунной системы может способствовать летальному исходу или вызывать аутосенсибилизацию к ЦНС-специфичным АГ посредством распространения эпитопов к АГ-представляющей системе в периферической лимфоидной ткани, что формирует основу для последующих «бустерных» реакций аутосенсибилизированных CD4+ клеток.
И наоборот, быстрый и специфический локальный ответ в ткани мозга приводит к эффективному ограничению распространения вируса, а следовательно — к субклинической терминации вирусной инфекции, опосредованной иммунной системой.
После ликвидации клеток, инфицированных вирусом, происходит уменьшение выраженности локального ответа посредством самоэлиминации причастных к процессу Т-клеточных популяций под воздействием пока не изученных сигнальных механизмов.
У вирусов имеются несколько стратегических механизмов «ухода» от Т-клеточно-опосредованной эрадикации, включая вмешательство в механизмы представления комплекса HLA класса I, а также «укрывательство» среди клеток, не имеющих экспрессии HLA класса I. Результатом этого может быть пожизненная персистенция вируса в ЦНС, т.е. состояние, которое предположительно активно контролируется Т-лимфоцитами.
При тяжелой иммуносупрессии может происходить реактивация вирусной репликации, что потенциально представляет для пациента угрозу летального исхода.
Система клеточного иммунитета предназначена для устранения вирусов, скрывающихся от антител внутри клеток. Антитела блокируют распространение цитолитических вирусов (высвобождаемых лизированными клетками), но обычно не эффективны по отношению к вирусам, модифицирующим АГ клеточных мембран и отпочковывающимся от них в виде инфекционных частиц. Последние способны распространяться на близлежащие клетки без участия антител.
Цитотоксические Т-лимфоциты поражают вирус-инфицированные клетки-мишени после распознавания новых поверхностных антигенов. Другая субпопуляция Т-клеток, взаимодействуя с зараженными вирусом клетками, высвобождает привлекающие макрофаги ИФН-у и ФНО, вследствие чего соседние клетки приобретают резистентность к вирусной инфекции.
Свободные вирусы нейтрализуются антителами, образование которых является тимус-зависимым процессом (в числе таких вирусов, как онкорна-, ортомиксо-, парамиксо-, тога-, рабдо-, арена-, герпес-, паповавирусы и некоторые другие).
Т-лимфоциты иммунизированного «хозяина» демонстрируют прямую цитотоксичность по отношению к клеткам, зараженным вирусами этой группы. Рецепторы CD8+ Т-лимфоцитов распознают новые поверхностные АГ на клетках-мишенях, а сами цитотоксические Т-лимфоциты в меньшей степени распознают вирусные штаммы, чем антитела. CD8+ клетки обладают большей перекрестной реактивностью, но рестриктированы (т.е. не поражают клетки, зараженные тем же вирусом, но несущие другие молекулы HLA класса I).
Если часть вирусов не контролируется цитотоксическими Т-лимфоцитами (уход вирусных частиц в соседние клетки), то используется другой механизм их инактивации. Т-хелперы, стимулированные АГ вируса, продуцируют ИФН-у, препятствующий репликации близлежащими клетками любого вируса, проникшего в них путем межклеточного транспорта. ИФН-у повышает неспецифическую цитотоксичность NK (по отношению к зараженным вирусом клеток). Выработка ИФН-у в ответ на стимуляцию вирусными компонентами (не имеющими отношения к нуклеиновым кислотам) служит важным протективным механизмом, особенно когда сами вирусы слабо стимулируют синтез интерферона.
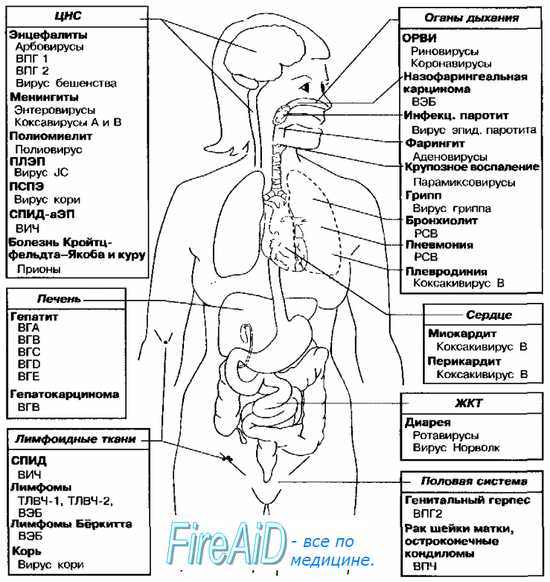
- Читать "Виды (представители) нейротропных вирусов"
Оглавление темы "Вирусные инфекции в неврологии":- Грипп у новорожденных детей - причины, диагностика, лечение
- Патогенез (механизмы развития) вирусных нейроинфекций
- Виды (представители) нейротропных вирусов
- Герпесвирусы (Herpesviridae) - строение, вызываемые инфекции
- Энтеровирусы (Enteroviridae) в неврологии - строение, вызываемые инфекции
- Вирус кори (Morbilli) в неврологии - строение, вызываемые инфекции
- Вирус паротита в неврологии - строение, вызываемые инфекции
- Вирус краснухи (Rubivirus) в неврологии - строение, вызываемые инфекции
- Вирус гриппа в неврологии - строение, вызываемые инфекции
- Аденовирусы (Adenoviridae) в неврологии - строение, вызываемые инфекции

