Стволовые клетки из трофобласта. Выделение линий эмбриональных стволовых клеток
До недавнего времени считалось, что получить из трофобласта ЭСК невозможно. Однако линия диплоидных стволовых клеток трофэктодермы, выделенная из бластоцисты, в среде, где вместо LIF содержится FGF2 и гепарин, пролиферирует и трансформируется в стволовые клетки (Rossant, 2001). Если удалить из среды FGF2, то клетки трофэктодермы прекращают размножение, в них начинается эндоредупликация хромосом, и трофэктодермальные клеточные элементы постепенно преобразуются в гигантские клетки трофобласта.
Вероятно, LIF не стимулирует пролиферацию клеток трофэктодермы вследствие того, что FGF2 запускает иной механизм транссигнализации, поскольку FGF2, связываясь с плазматическим рецептором (FGFR2), активирует в цитоплазме МАР-киназы — ERK1 и ERK2. Следовательно, при включении в клетках бластоцисты одного сигнального пути (LIF — gpl30 — JAK-киназы — STAT3) клетки внутренней клеточной массы трансформируются в плюрипотентные ЭСК, а при активации второго механизма трансмембранной передачи сигнала (FGF2 — FGFR2 — МАР-киназы ERK1/ERK2) в бластоцисте образуются стволовые клетки трофэктодермы.
Выбор сигнального пути, в свою очередь, зависит от активности гена oct4. Этот ген, принадлежащий домену POU, расположен в локусе t аутосомы 17 и экспрессируется в процессе оогенеза, в период дробления, а также в клетках внутренней клеточной массы бластоцисты и в первичных половых клетках (Niwa, 2000; Smith, 2001). Функциональная роль гена oct4 заключается в кодировке транскрипционного фактора, необходимого для возникновения плюрипотентных клеток, их дифференцировки и дедифференциации (Niwa, 2001; Smith, 2001).
Экспрессия гена oct4 в ЭСК изменяется в зависимости от взаимодействия этого транскрипционного фактора с кофакторами. Направленная регуляция экспрессии oct4 в бластоцистах показала, что при снижении его активности половина клеток образует трофэктодерму, тогда как при повышении индуцированной экспрессии oct4 возникают преимущественно ЭСК.
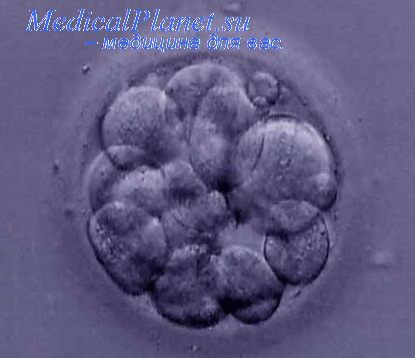
В эксперименте ЭСК не удается перевести в линию при культивировании тотипотентных бластомеров на стадии дробления, а также на стадии гаструляции и более поздних стадиях эмбрионального развития (Brook, Gardner ,1997). Мышиные ЭСК обычно выделяют на 3,5-4,5-й день беременности, что соответствует шестой (однослойная бластоциста) и седьмой стадиям (двухслойная бластоциста — ранний яйцевой цилиндр) нормального эмбриогенеза.
Очевидно, что только в доимплантационном периоде зародыши мышей содержат клеточные популяции, способные трансформироваться в ЭСК. Следовательно, выделение линий ЭСК возможно лишь на определенных стадиях эмбриогенеза. Тотипотентными, с точки зрения возможности развития жизнеспособного эмбриона с зародышевыми оболочками и плацентой, являются зигота и возникающие в ходе дробления бластомеры. Утрата тотальной потенции зародышевых клеток начинается на стадии поздней морулы, когда дальнейшее коммитирование бластомеров зависит от их расположения. Бластомеры ранней морулы сохраняют тотипотентность, поскольку экспериментальные манипуляции с изменением их локализации, например инверсия их расположения, не препятствует развитию полноценного зародыша.
Установлено, что на эффективность выделения ЭСК в линию влияет состояние бластоцист в момент их эксплантации. Использование бластоцист после моделирования семидневной диапаузы в половом тракте мышей, овариоэктомированных на 3,5-й день беременности и получавших прогестерон, способствует более успешному выделению линий стволовых эмбриональных клеток (Evans, 1981; Robertson, 1987). Предполагается, что в таких условиях увеличивается число бластомеров, образующих внутреннюю клеточную массу. Не исключено также, что происходит удлинение клеточного цикла и большинство бластомеров переходит в фазу G0 (Brook, Gardner, 1997).
Кроме того, создание стабильных плюрипотентных линий ЭСК зависит от генотипа зародышей: достаточно легко ЭСК выделяются из бластоцист мышиной линии 129, значительно трудней их получить при использовании мышей CS7BL/6 и практически невозможно выделить линию ЭСК из бластоцист мышей СВА/Са. Очевидно, ранние зародыши обладают какими-то генетическими особенностями, влияющими на развитие линии плюрипотентных ЭСК. Тем не менее, при культивировании изолированного эпибласта (Brook, Gardner, 1997), а также с помощью селективного отбора дифференцирующихся клеток (McWhir, 1996) линии ЭСК из ранних зародышей мышей СВА/Са все же были выделены.
- Читать далее "Техника получения линий стволовых клеток. Селекция чистой популяции стволовых клеток"
Оглавление темы "Культура эмбриональных стволовых клеток":1. Техника культивирования эмбриоидных телец. Гибридные клетки
2. Стволовые клетки из трофобласта. Выделение линий эмбриональных стволовых клеток
3. Техника получения линий стволовых клеток. Селекция чистой популяции стволовых клеток
4. Выделение линий первичных половых клеток. Пролиферация первичных половых клеток
5. Выделение эмбриональных стволовых клеток. Среды размножения стволовых клеток
6. Функциональная роль LIF. Влияние LIF на ткани
7. Влияние LIF на эмбрионы. Фенотипические особенности эмбриональных стволовых клеток
8. Пролиферация эмбриональных стволовых клеток. Клональный рост эмбриональных стволовых клеток
9. Состав клона эмбриональных клеток. Плюрипотентность эмбриональных стволовых клеток
10. Регенеративные возможности эмбриональных стволовых клеток. Генные маркеры клеток зародышевых листков

