Причины лейомиом матки. Механизмы развития
Лейомиомы определяют как доброкачественные моноклональные разрастания гладкой мышечной ткани. Каждая моноклональная миома может ассоциироваться с различными хромосомными транслокациями, дупликациями и делециями. Многие, однако не все, миомы содержат имеют цитогенетические отклонения, в то время как мышечная оболочка матки имеет нормальный кариотип — обычно они включают хромосомы 7,12 и 14. Большинство мутаций появляется в генах, отвечающих за клеточный рост или ответственных за архитектурную транскрипцию.
Выявлено два наследственных нарушения, при которых миомы матки — часть генетически обусловленного синдрома:
• Врожденный лейомиоматоз в сочетании с раком, происходящим из клеток почечного эпителия. Это аутосомно-доминантный синдром (гладкомышечные опухоли матки, кожи и почек).
• Синдром легочного лейомиоматоза и лимфангиомиоматоза. Возникает в результате мутаций в одном из двух генов, отвечающих за туберозный склероз — синдром, приводящий к развитию гамартом ы со сложной структурой.
В большинстве случаев миомы макроскопически проявляются как дискретные круглые опухоли, которые светлее, чем окружающая мышечная ткань матки, с блестящими на разрезе образованиями жемчужно-белого цвета. К особенностям тканевой структуры относится наличие переплетающихся тяжей из гладкомышечных волокон, между которыми расположена фиброзная ткань.
Влияние стероидных гормонов лежит в основе теории «клональной экспансии миомы». Миомы восприимчивы к эстрогенам и прогестерону, поэтому, скорее всего, они могут увеличиваться в размере и вызывать сопутствующую симптоматику у женщин репродуктивного возраста. С другой стороны, при наличии миом не отмечено увеличения концентрации циркулирующих эстрогенов и прогестерона в сыворотке крови.
Факторы, инициирующие развитие опухоли и еще подлежащие уточнению генетические факторы, связаны с ключевыми соматическими мутациями, способствующими развитию лейомиоцита из нормальной мышечной клетки и восприимчивыми к воздействию эстрогенов и прогестерона. Существенную роль в развитии миом имеет интегральное воздействие ЭР, ПР и рецепторов ЭФР. Как показал ряд исследований, по сравнению с нормальным миометрием в миомах отмечена повышенная концентрация рецепторов, чувствительных к эстрогенам, и ПР.
В миомах отмечен повышенный синтез ароматазы р450. В свете этого, наряду с воздействием циркулирующих эстрогенов на ЭР, большое значение в потенцировании действия эстрогенов на миоциты может иметь местная конверсия циркулирующих андрогенов в эстрогены.
Обычно считали, что эстроген — главный гормональный медиатор роста миом. Хотя прогестины применяют для лечения кровотечения при симптомной миоме, недавние исследования показывают, что прогестерон может играть значительно большую роль в качестве медиатора роста миом, чем это считали раньше. Доказано, что антипрогестин RU486 (мифепристон) вызывает уменьшение размера миом, а еще одно исследование показало, что в миомах в секреторную фазу увеличивается количество митозов по сравнению с пролиферативной фазой.
Развитие опухолевых новообразований — результат ускоренной клеточной пролиферации, опережающей тормозящий эффект апоптоза. Доказано, что апоптоз приостанавливается в миомах матки. Воздействие прогестерона повышает количество противодействующего апоптозу белка bcl-2, поэтому стимуляция роста миомы может быть результатом подавления апоптоза прогестероном. In vitro было отмечено, что при добавлении прогестерона к культуре клеток лейомиомы увеличивался синтез bcl-2 по сравнению с контрольными наблюдениями. В нормальном миометрии чрезмерного образования bcl-2 в присутствии прогестерона не отмечено.
В целом на процесс апоптоза влияет не только семейство bcl-2, но также соотношение Fas/FasL и Rb-1. Martel и соавт. описали различные механизмы развития апоптоза, недостаточно выраженные в лейомиомах, и наметили возможные «мишени» для терапии миом. Роль апоптоза в патогенезе миом — перспективная область будущих исследований с огромным потенциалом для применения в медицинской практике.
Кроме того, в патофизиологии роста миом было обнаружено синергичное взаимодействие эстрогеновой и прогестероновой стимуляций. Было также установлено возрастание количества ПР в результате повышения количества эстрогенов. Исследование в искусственных условиях показало, что прогестерон активирует экспрессию ЭФР, а эстрогены увеличивают также экспрессию его рецепторов.
Беременность и лейомиома
Влияние вызванных беременностью изменений гормонального фона на миому комплексное. Есть многочисленные сообщения о быстром развитии миом во время беременности; однако все проспективные исследования показывают, что большинство миом не изменяется в диаметре с I триместра до родов. Практически невозможно предсказать, какая миома будет увеличиваться.
Основные потенциальные осложнения во время беременности — боль и гибель плода. Боль способна возникать в результате миоматозной дистрофии. Данный феномен может быть следствием некроза, развившегося в связи с нарушением кровоснабжения субсерозной миомы или миомы на ножке. Обычно присутствует локальная болезненность, а при УЗИ выявляют кистозную неоднородную структуру.
К числу наиболее распространенных осложнений, вызванных миомами, относятся преждевременные роды, сильные послеродовые кровотечения и предлежание плаценты. Миомы, локализованные в нижних сегментах матки, могут стать показанием к кесареву сечению в связи с возникшей обструкцией родовых путей или неправильным предлежанием плода.
- Рекомендуем далее ознакомиться со статьей "Диагностика лейомиом матки. УЗИ, МРТ, гистеросальпингография"
Оглавление темы "Лейомиомы матки":- Осложнения оперативной гистероскопии. Ранние и поздние
- Маточное кровотечение после гистероскопии. Выбор расширяющей среды
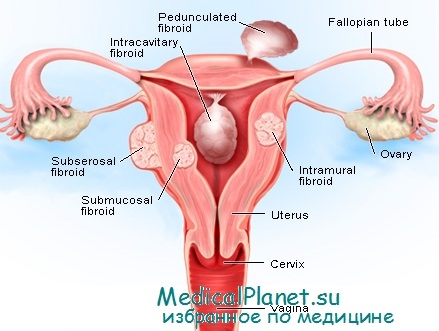
- Лейомиома матки. Классификация
- Клиника лейомиомы матки. Маточные кровотечения и боли
- Эпидемиология лейомиом матки. Распространенность
- Причины лейомиом матки. Механизмы развития
- Диагностика лейомиом матки. УЗИ, МРТ, гистеросальпингография
- Лечение лейомиом. Агонисты ГнРГ
- Тамоксифен, ралоксифен, азоприснил для лечения лейомиом матки
- Хирургическое лечение лейомиом матки. Гистерэктомия

