TOLL подобные рецпторы (TLR) кожи
а) Индуцированное Tlr высвобождение цитокинов. Показано, что активация TLR различных клеток запускает высвобождение как провоспалительных, так и иммуномодулирующих цитокинов. Активация TLR моноцитов и дендритных клеток индуцирует высвобождение IL-12 и IL-18, необходимых для развития Thl-реакции, и IL-1b, IL-6, IL-23, необходимых для Th17-реакций, а также противовоспалительного IL-10. Индукция специфического цитокинового ответа определяет тип адаптивной Т-клеточной реакции.
б) Дифференциация макрофагов и дендритных клеток. TLR регулируют фагоцитоз либо за счет активации слияния эндосом с лизосомами, либо за счет индукции гена программы фагоцитоза, регулирующей активность множества скэвенджер-рецепторов. Активация TLR моноцитов приводит к индукции ИЛ-15 и ИЛ-15R, что в свою очередь запускает дифференцировку в направлении CD209 + MF36, обладающих антимикробной активностью. Активация TLR моноцитов также индуцирует GM-CSF и GM-CSFR, что запускает дифференцировку в направлении незрелых дендритных клеток, способных синтезировать цитокины и эффективно представлять антиген Т-клеткам.
Кроме того, активация TLR незрелых дендритных клеток приводит к их дальнейшему созреванию, сопровождающемуся усилением способности стимулировать Т-клетки.
в) Противомикробная активность, индуцированная TLR. У дрозофилы Толл-белок является критическим для защиты организма. Подверженность мышей со спонтанными мутациями TLR бактериальным инфекциям указывает на то, что такую же роль TLR играют у всех млекопитающих. Активация TLR микробными липопротеинами вызывает активацию индуцируемого промоутера NO-синтазы (NIOS-1I или iNOS), что приводит к выработке NO, известного антимикробного агента. Имеется достаточно данных в пользу того, что активация TLR приводит к уничтожению внутриклеточного микроорганизма Mycobacterium tuberculosis как в макрофагах мыши, так и человека.
В макрофагах мышей активизация бактериального липопротеина TLR2 приводит к NO-зависимому уничтожению внутриклеточных туберкулезных бацилл. В моноцитах человека и макрофагах альвеол бактериальные липопротеины подобным же образом активируют TLR2 для уничтожения внутриклеточной бактерии М. tuberculosis. Однако этот антимикробный механизм, не зависит от NO. На самом деле, основной механизм противомикробного действия моноцитов человека, активированных TLR, включает индукцию 25-гидроксивитамина D3-1α-гидроксилазы (CYP27bl), который превращает 25D в активную форму 1,25D, стимуляцию и активацию рецептора витамина D (PBD) и нисходящую индукцию противомикробного пептида кателицидина. Способность активации TLR2/1 усиливать экспрессию CYP27b1 и PBD зависит от ИЛ-15.
Одновременная стимуляция активности ИЛ-1β и активация PBD индуцирует β-дефензин человека 2 типа, что также требуется для оказания противомикробного эффекта.
Активация толл-подобных рецепторов 3, 4, 7, 8 и 9 типов приводит к индукции противовирусной активности, которая зависит от секреции интерферона I типа и опосредуется специфическими сигнальными путями. Были идентифицированы два пути, опосредованных TLR: продукция интерферона I типа возникает посредством пути, не зависящего от MyD88, в ответ на активацию TLR3 и TLR4, и, после стимуляции агонистами толл-подобных рецепторов 7,8 и 9 типов, посредством зависящего от MyD88 пути.
Активация TLR может также наносить вред, приводя к повреждению тканей. Введение липополисахаридов (ЛПС) мышам может привести к септическому шоку, который зависит от TLR4. Полученные данные говорят о том, что активация TLR2 микроорганизмом Propionibacterium acne вызывает воспалительные реакции при вульгарном акне, которые приводят к повреждению ткани.
Aliprantis и соавт. показали, что микробные липопротеины обладают способностью вызывать как TLR-зависимую активацию защиты организма, так и патологические изменения тканей. Этот двойной сигнальный механизм похож на сигнальный путь рецептора ФНО и CD40, который приводит к активации ядерного фактора-кВ и к апоптозу. Подобным же образом иммунная система может использовать одни и те же молекулы для активации защитных механизмов, а затем, путем, апоптоза, тормозить развитие реакций, чтобы не вызвать повреждения ткани.
Активация TLR может приводить к ингибиции механизма антиген-презентации главного комплекса гистосовместимости (ГКГ) класса II, что может тормозить иммунные реакции, приводящие к альтерации тканей, но может способствовать и иммуносупрессии. И наконец, Толл-активация задействована в разрушении костной ткани.
Сделать вывод о ключевой биологической роли TLR в защите организма человека можно исходя из того факта, что мутации TLR4 связаны с гипо-реактивностью ЛПС у человека. Из этого можно заключить, что люди с генетическими изменениями в TLR более подвержены некоторым микробным инфекциям. Более того, возможно следует использовать механизм активации TLR как средство поддержки иммунных реакций в вакцинах и препаратах для лечения инфекционных заболеваний, а также для предотвращения реакций, вредных для организма.
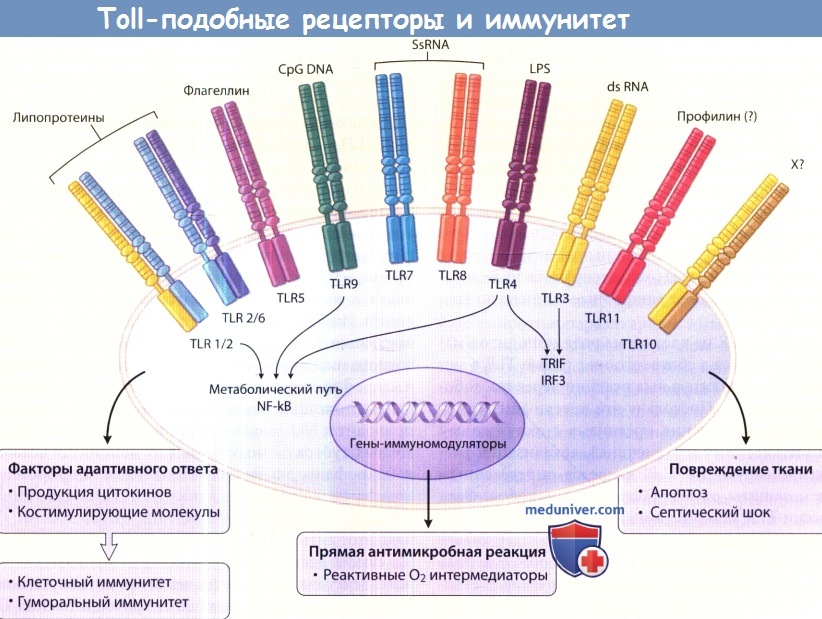
Активация TLR специфическими лигандами вызывает:
1) высвобождение цитокинов и костимулирующих молекул, которые определяют тип адаптивного иммунного ответа;
2) прямую антимикробную реакцию и 3) повреждение ткани.
CpGDNA = иммуностимулирующие, богатые цитозином и гуанином последовательности ДНК;
dsRNA = двухцепочечная РНК; LPS = липополисахарид; NF-kB = ядерный фактор кВ;
ssRHA = одноцепочечная РНК; X = неизвестный лиганд.
- Рекомендуем далее ознакомиться со статьей "Клетки врожденной иммунной системы кожи"
Оглавление темы "Иммунитет кожи.":- Болезни волос и кожи при цветной коже
- Рак кожи при цветной коже
- Советы по косметологическим процедурам при цветной коже
- Врожденный и адаптивный иммунитет кожи
- Молекулы врожденной иммунной системы кожи
- TOLL подобные рецпторы (TLR) кожи
- Клетки врожденной иммунной системы кожи
- Лимфоциты адаптивного иммунного ответа кожи
- Наивные Т-лимфоциты кожи
- T-хелперы кожи (Th1, Th2 лимфоциты кожи)

