Склеродермия: частота встречаемости, причины, механизмы развития
Склеродермия - краткий обзор:
- Системная склеродермия (ССД) представляет собой мультисистемное заболевание, характеризующееся выраженным фиброзом, воспалением и васкулопатией.
- Патогенез этого аутоиммунного процесса остается неясным.
- Дифференциальный диагноз системной склеродермии включает тяжелые формы локализованной склеродермии, а также много других склеродермоподобных состояний.
- Больные склеродермией разделяются на две основные группы в зависимости от распространенности склероза кожи [диффузный системный склероз и ограниченный системный склероз]. Пациенты с комбинированным синдромом характеризуются дополнительными клиническими признаками других ревматических заболеваний.
- Клинические признаки, которые присутствуют практически всегда, включают феномен Рейно и склероз кожи.
- Системная склеродермия (ССД) характеризуется склеротическими/фи-брозными нарушениями кожи и внутренних органов (желудочно-кишечного тракта, легких, почек и сердца), которые могут привести к тяжелой дисфункции почти любой системы организма.
- Разнообразие проявлений и течения ССД требует срочной помощи различных специалистов и последующих, как минимум ежегодных профилактических осмотров.
- Несмотря на неизлечимый характер заболевания, достигнуты значительные успехи в лечении органоассоциированных осложнений ССД.
а) Эпидемиология склеродермии. Системная склеродермия (ССД) — это редкое, мультисистемное заболевание, в основе которого лежат аутоиммунные процессы, дисфункция эндотелиальных клеток сосудов и активация фибробластов. Заболевание характеризуется большой индивидуальной вариабельностью в выраженности поражения кожи и внутренних органов, а также в течении патологического процесса и прогнозе. Наиболее часто поражаемыми органами являются кожа, пищевод, легкие, сердце и почки.
Системной склеродермией (ССД) чаще болеют женщины, соотношение мужчин и женщин — от 3:1 до 14:1. Возраст начала заболевания варьирует от 30 до 50 лет.. У мужчин отмечено более раннее начало. Представители негроидной расы заболевают ССД раньше, чем европеоиды. Опубликованные данные о заболеваемости возросли с 0.6 до 16 на миллион человек, что также справедливы в отношении распространенности, которая возросла с 2 до 233 пациентов на 1 миллион населения в год., что объяснялось методологическими различиями в отношении определения и подтверждения диагноза, а также периода исследования.
Смертность от системной склеродермии (ССД) наивысшая среди всех аутоиммунных ревматических заболеваний, индивидуально варьирующая от расовых и этнических особенностей, давности и тяжести поражения органов, типа системной склеродермии (ССД), возраста установления диагноза, гендерных различий. Несмотря на неизлечимый характер заболевания, достигнуты значительные успехи в лечении органоассоциированных осложнений системной склеродермии (ССД).
б) Этиология и патогенез системной склеродермии (ССД). Патогенез этого комплексного заболевания предполагает вовлечение различных типов клеток (эндотелиальных, эпителиальных, фибробластов и лимфоцитов), воздействующих друг с другом с помощью различных механизмов, зависящих от их микроокружения и ключевых медиаторов.
Клиническая гетерогенность системной склеродермии не исключает того, что у каждого отдельного пациента или среди подтипов болезни преобладают определенные патогенетические механизмы. Также, похоже, что на разных стадиях системной склеродермии сочетание механизмов различается. Кроме того, вполне вероятен генетический механизм этиопатогенеза, что находит отражение в тяжести заболевания и предрасположенности к его развитию; также высока вероятность влияния факторов окружающей среды и химических агентов в качестве триггеров заболевания.
1. Генетические факторы. Лучшее доказательство вклада генетических факторов в развитие системной склеродермии получено в исследованиях, которые сообщают о семейном характере заболевания, а также в исследованиях близнецовым методом. Хотя риск развития склеродермии у родственников довольно низок, относительный риск развития у родственников первой линии родства в 13 раз выше, чем в популяции. Некоторые исследования показывают, что отягощенный семейный анамнез по склеродермии является наиболее серьезным риском, равно как и этническая принадлежность.
Assassi и соавт. предполагают, что у членов семей, отягощенных по склеродермии, выявляются конкордатные специфичные для склеродермии антитела. Полное генетическое исследование хромосомной экспрессии в кожных биоптатах и циркулирующих клетках крови подтверждает мультифакторный комплексный путь развития склеродермии. Кроме того, это подтверждено сопутствующими генетическими исследованиями в контексте подхода «ген-кандидат». Наибольший успех наблюдается при генетическом анализе индивидуальных компонентов болезни, таких как профиль аутоантител. Вероятно, он генетически строго детерминирован, и это может лежать в основе взаимной специфичности характерной для системного склероза реактивности.
Было показано, что способность вызывать иммунный ответ к определенным антигенам, ассоциированным с системной склеродермией, определяется гаплотипами главного комплекса гистосовместимости. Ряд исследований предполагает связь HLA-DRB1*1302, DQB0604/0605 гаплотипов и пациентов положительных на антифибрилларин, в то время как HLA SRB1*0301 выявляется у пациентов с анти-полимиозитно-склеродермическими антителами (anti-Pm-Scl). По итогам множества исследований генетических маркеров выделен ряд «генов-кандидатов» (AIF-1, CD19, CD22, CD86, CTLA-4, CCL-2, СС1-5, CXCL-8, CXCR-2, IL-1a, IL-1β, IL-2, IL-10, IL-13, MIF, PTPN22, TNF-α). Однако как и при других системных заболеваниях, по очень многим причинам возможность воспроизвести эти изначально многообещающие результаты не была доказана. Исследования генетически гомогенных популяций, включая коренное американское племя Чокто, были особенно информативны. Интересно, что некоторые связи очень вероятны с точки зрения молекулярного патогенеза. Вероятно, эпистаз и эффект многочисленных модификационных генов не позволяют получить простые генетические связи при системной склеродермии, как и при других системных заболеваниях.

2. Иммунные реакции системной склеродермии (ССД). Получены убедительные доказательства воспалительных изменений кожи и легких при системной склеродермии. Один из примеров — присутствие высокоспецифичных патогномоничных аутоантител. Обобщение приведено в таблице ниже. Первичные воспалительные инфильтраты пораженных участков кожи преимущественно представлены клетками моноритарного ряда (Т-клетки, макрофаги, В-клетки и тучные клетки). В дальнейшем преобладают Т-лимфоциты, они выявляются как в пораженных органах, так и в циркуляторном русле. Т-клетки обычно представлены CD4+ (ключевым маркером активации), что указывает на олигоклональную экспансию и антиген-спровоцированную пролиферацию с увеличением количества Т2-хелперов.
В результате у пациентов со склеродермией наблюдается увеличение сывороточного уровня Т2-стимулирующих цитокинов, а именно, IL-2, IL-4, IL-10, IL-13 и IL-7. Кроме того, в пораженных участках кожи обнаруживаются В-клетки. Ряд исследований указывает на то, что В-клетки могут индуцировать продукцию экстрацеллюлярного матрикса (ЭЦМ) посредством секреции IL-6 и преобразующего фактора роста-b (ПФР-в) и участвовать в синтезе антител. Установлена связь некоторых антител с конкретным подтипом заболевания, что делает их важными диагностическими маркерами. В большинстве случаев системной склеродермии имеются положительные антинуклеарные антитела. Оно включает ряд отличительных реактивностей и антитела, образующиеся и при других аутоиммунных ревматических заболеваниях (например, антициклический цитруллинированный пептид, ревматоидный фактор). Ряд антител, имеет функциональную значимость, поскольку они направлены против антигенов поверхности клетки (антиэндотелиальные клеточные антитела (АЭКА), антифибриллиновые антитела, антитела к рецепторам тромбоцитарного фактора роста, и т.д.).
Однако функциональный вклад этих аутоантител остается областью для исследований. Некоторые исследования показали, что антигены, узнаваемые специфическими для системной склеродермии аутоантителами, могут быть экспрессированы на поверхности клеток. Лучшие доказательства функциональной значимости получены для антиэндотелиальных клеточных аутоантител и для аутофибробласт-реагирующих антител. Недавние работы показали присутствие аутоантител к фибриллину и стимулированных аутоантител, реагирующих с рецепторами фактора роста, выделенного из тромбоцитов (PRGF), однако эти наблюдения требуют дальнейшего подтверждения.
В некоторых случаях предложены механизмы микрохимеризма и болезни «трансплантат против хозяина», хотя относительно высокая частота микрохимеризма у здоровых людей или при других патологических состояниях указывает на то, что это может быть только предрасполагающим фактором, но не причиной, если это и играет роль при системной склеродермии.
3. Васкулопатия. Васкулопатия при склеродермии обусловлена нарушением сосудистого ремоделирования и восстановления. Этот процесс затрагивает микроциркуляторное русло и артериолы, а также, вероятно, является первичным звеном в патогенезе заболевания и последующего фиброза. Сосудистые нарушения включают в себя вазоконстрикцию, пролиферацию адвентиции и интимы, воспаление и тромбоз. Ранние проявления васкулярной дисфункции представлены увеличением сосудистой проницаемости с нарушением баланса между сосудорасширяющими и сосудосуживающими медиаторами (оксид азота, простациклин, генетически-связанный белок кальцитонина), а также медиаторами вазоконстрикции (эндотелии 1 (ЭТ 1), ангиотензин 2, α2-адренорецепторы). В результате нарушений кровотока развивается гипоксия тканей, что ведет к усиленной экспрессии эндотелиального сосудистого фактора роста (ЭСФР) и его рецепторов наряду с нарушением образования сосудов. Тем не менее, воспалительные цитокины, такие как TNF-α, могут стимулировать или ингибировать ангиогенез в зависимости от длительности стимуляции. В дополнение к данным функциональным нарушениям, внутрисосудистые и структурные изменения вызывают активный феномен Рейно (синдром Рейно) (ФР, СР) и с течением времени приводят к атрофии сосудов и ухудшению микроциркуляции. Эти васкулопатии клинически проявляются в поражении сосудов практически всех органов.
Ранние нарушения в микроциркуляторном русле в результате структурных изменений обнаруживаются прежде всего в капиллярах ногтевого ложа в виде вазоспазма при синдроме Рейно (СР). К тому же, сосудистые изменения, а именно, пролиферация эндотелия и накопление рубцовой ткани провоцируют одни из самых значимых осложнений склеродермии, включая гипертензию легочной артерии (ГЛА), склеродермический почечный криз (СПК) и васкулопатию пальцев.
4. Фиброз. Системная склеродермия — прототип мультисистемного фибротического заболевания. Первичное воспаление и гипоксия фибробластов запускают продукцию ряда белков, участвующих в ремоделировании внеклеточного матрикса, к примеру, тромбоспондина-1, фибронектина-1, лизилгидроксилазы-2, белка индуцированного трансформирующим фактором роста β (TGF-β). Отложение избыточного количества внеклеточного матрикса в специализированных органах является основной причиной большей части осложнений и летальных исходов при этой болезни. Грубоволокнистая соединительная ткань вырабатывается активированными фибробластами и миофибробластами. На ранних этапах болезни была установлена аутосомная популяция фибробластов, ответственная за усиленную продукцию и аккумуляцию экстрацеллюлярного матрикса. Инициаторами этого процесса является множество ключевых цитокинов и факторов роста, которые могут представлять логические терапевтические цели. Ключевым фактором служит нарушение баланса между механизмами синтеза и разрушения. Дремлющие фибробласты могут быть активированы трансформирующим фактором роста β (TGF-β), фактором роста соединительной ткани (ФРСТ), тромбоцитарным фактором роста (PDGF)) или эндотелином-1.
Вероятно, фибробласты проходят процесс дифференцировки в миофибробласты, что сопровождается повышением сократительной способности, ростом продукции внеклеточного матрикса и высвобождением цитокинов. Одновременно с изменением биофизических свойств соединительной ткани это приводит к постоянной активации фибробластов и, следовательно, к усиленному накоплению компонентов внеклеточного матрикса.
Схематическое обобщение патогенетических механизмов при системной склеродермии показано на рисунке ниже.
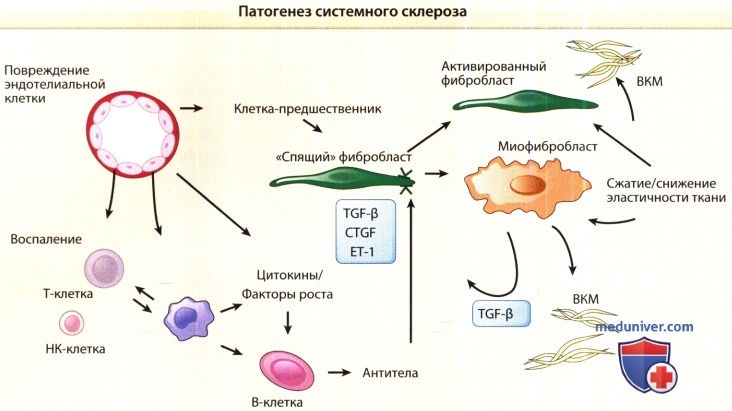
На схеме показано, как системный склероз развивается при комплексном взаимодействии между клетками иммунной системы, включая адаптивный и врожденный компоненты, сосудистое русло и соединительную ткань.
Взаимодействия клеточного матрикса также потенциально важны. Ранние сосудистые события приводят к последующему развитию относительно автономной популяции активированных фибробластов и миофибробластов, которые сжимают мягкие ткани и запасают избыточный внеклеточный матрикс.
Эти клетки могут развиваться из резидентных соединительнотканных фибробластов: трансдифференциацией из других типов клеток, включая активированные перициты микрососудов, с привлечением циркулирующих клеток-предшественников (фиброцитов). Вклад каждой линии клеток в фибротическое повреждение неясен. Многие факторы роста и цитокины вовлечены в этот процесс в качестве медиаторов, комплексные реципрокные сети могут приводить к формированию профибротического микроокружения.
Потенциальная терапия, модифицирующая заболевание, может быть направлена на медиаторы селективно или комбинированно [например, фактор некроза опухоли-β (ТНФ-β), эндотелии (ЕТ-1), фактор роста соединительной ткани (CTGF), фактор роста, выделенный из тромбоцитов, (PDGF)] или модулирование иммунных клеток (например, циклофосфамид) или эндотелиальных клеток (например, аналоги простациклина). Внеклеточный матрикс (ВКМ) может быть важным хранилищем медиаторов, которые позже высвобождаются и играют ключевую роль в патогенезе.
5. Факторы окружающей среды. Синдромы, сходные со склеродермией, были описаны в связи с воздействием внешних токсинов и лекарств. Эти агенты включают растворители (винилхлорид, бензол, толуол, эпоксидная смола), лекарственные препараты и наркотики (блеомицин, кардиопа, пентазоцин, кокаин, доцетаксел, метафенилендиамин), а также смешанные субстанции.
Склеродермия часто возникает у работников на добыче угля и золота. У мужчин старше 40 лет, страдающих от силикоза, вероятность развития склеродермии примерно в 190 раз выше по сравнению с теми, кто не подвергался воздействию пыли оксида кремния. Изучается также роль силиконовых имплантов и других продуктов, содержащих кремний, в развитии склеродермии. Тем не менее, в большинстве эпидемиологических исследований достоверной связи установлено не было. Необычная форма склеродермии, характеризующаяся развитием синдрома Рейно, склеродермоподобными изменениями кожи, нарушениями строения капилляров ногтевого валика (сходными с таковыми при склеродермии), остеолизисом дистальных фаланг, печеночным и легочным фиброзом (ЛФ), может развиваться у работников, подвергающихся воздействию поливинилхлорида. Блеомицин также провоцирует развитие ЛФ, синдрома Рейно, и кожных изменений неотличимых от характерных для склеродермии. Развитие вышеописанных изменений дозозависимо и обратимо при прекращении воздействия поражающего агента. В совокупности, химическими агентами вызвано небольшое количество склеродермо-подобных заболеваний. Крупные эпидемиологические исследования до сих пор не установили значимость роли токсинов и лекарственных препаратов в развитии склеродермии.
- Рекомендуем далее ознакомиться со статьей "Симптомы и клиника склеродермии (кожные и системные проявления)"
Редактор: Искандер Милевски. Дата публикации: 13.2.2019

