Propionibacterium acnes (P. acnes) как причина акне
Воспалительная реакция, которая является источником проблем при всех видах акне, направлена на ограниченное число чужеродных агентов. Вспомните, что термин чужеродный подразумевает под собой что-то, чего не должно быть в дерме. А дерма — это та часть кожи, которая находится под (с нижней стороны) базальной мембраной. Вспомните, что базальная мембрана располагается под эпидермисом в горизонтальном направлении, а затем идет глубже и охватывает все придатки кожи, от потовых желез и до волосяных луковиц. На одних участках мембрана более тонкая, на других более толстая.
Она повторяет контуры сально-волосяного фолликула (СВФ) подобно тому, как виниловые перчатки прилегают к пальцам. Осуществляет поддерживающую функцию придатков кожи, прикрепляет эпидермис к дерме. Она является полунепроницаемым барьером, позволяя ограниченному количеству воды, химических веществ и нескольким подвижным молекулам проникать в эпидермис и придатки кожи и обратно.
Недавно было описано химическое соединение — индуцируемый при гипоксии фактор 1 [hypoxia-inducible factor 1 (HIF-1)], которое отвечает за два процесса, активизирующихся в процессе развития акне. Было выявлено, что HIF-1 вызывает «гиперпролиферацию и незаконченную дифференцировку эпидермальных кератиноцитов». Он также «главный регулятор клеточной адаптации в условиях кислородного голодания» и «играет важную роль в продукции кератиноцитами цитокинов и привлечении нейтрофилов в кожу». Таким образом, HIF-1 стимулирует избыточный рост, вплоть до разрыва СВФ, а также способствует миграции клеток воспаления в зону ответа на аноксический стресс.
Как только барьер разрушен, чужеродный материал, находящийся в канале сально-волосяного фолликула (СВФ), становится «видимым» для иммунной системы человека. Это происходит, если иммунные клетки через дефекты базальной мембраны попадут в фолликулярный канал или если чужеродный материал из фолликулярного канала выйдет наружу. В любом случае иммунная система распознает чужеродный материал, и это первый сигнал для развития воспаления. Если иммунная реакция продолжается, фолликулярный канал все больше повреждается и часто разрывается. Значительное количество чужеродного материала из фолликулярного канала попадает в дерму. Там происходит стимуляция множества воспалительных процессов, регулируемых врожденной и приобретенной иммунной системой. И борьба усиливается.
Чтобы снять воспаление и вылечить акне, мы должны знать, какие чужеродные агенты, вызывающие воспаление, находятся в фолликулярном канале. А затем мы можем планировать устранение всех и каждого из них.
Propionibacterium acnes (Р. aeries). Bacillus acnes, «acne bacillus», впервые была описана Гилкристом (Gilchrist) в 1900 г. В 1909 г. она была переименована в Corynebacterium acnes, а позже в Propionibacterium acnes (Р. acnes). В род Propionibacterium входит 22 представителя, но при развитии акне только Р. acnes (который включает несколько штаммов) является единственно важным микроорганизмом. А раз это так, то в течение десятилетий дерматологи считали главной целью лечения устранение Р. acnes. Но есть проблема. Просто подавление антибиотиками популяции Р. acnes обычно не приводит к излечению. Этот простой факт должен был дать нам подсказку еще десятки лет назад, что здесь происходит что-то еще. Подробнее об этом ниже.
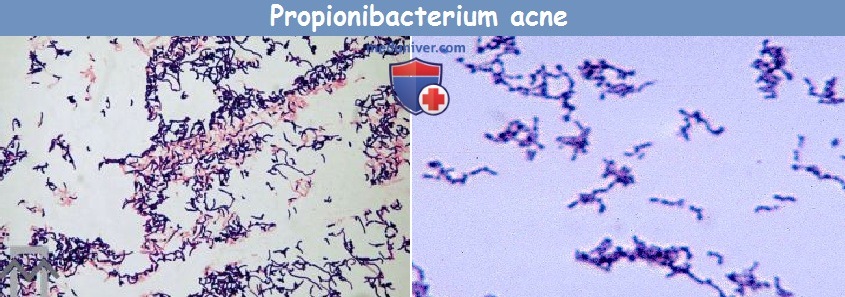
а) Значение P.acnes в норме. В основном было принято считать, что Р. acnes — естественный микроорганизм кожи каждого (комменсал), но это еще не вся история. Недавно при помощи простой усовершенствованной техники Бек-Томсен (Bek-Tomsen) показал, что Р. acnes имеет исключительные права на размещение в СВФ. Его работа продемонстрировала, что ни один другой организм не обладает такими требованиями. Более того, было сделано предположение, что этот относительно безобидный микроорганизм на самом деле играет роль защитника целостности СВФ. Эта концепция нашла подтверждение в других работах. Так как же реализуется такая защитная функция?
Представьте, что Р. acnes спокойно находится в фолликуле. Она является факультативным анаэробом. Это означает, что Р. acnes может выживать и размножаться в среде с очень малым количеством кислорода (или при его полном отсутствии). В норме фолликулы хорошо оксигенированы, поэтому «двигатель» Р. acnes находится в «нейтральном положении». Даже при таком незначительном повреждении канала, как царапина или ссадина, малое количество антигенов Р. acnes может выходить наружу. Или, что менее вероятно, блуждающие дендритные клетки, несущие на своей поверхности TLR2-рецепторы (toll-likereceptor 2) проникают в просвет канала. И если происходит контакт между Р. acnes и врожденной иммунной системой, то запускается каскад воспалительных реакций, в норме приводящий к восстановлению повреждения.
Нужно запомнить, что такое слабо выраженное воспаление предназначено для восстановления нормальной структуры канала. Целью воспалительного процесса, который мы так сильно стараемся подавить, является совсем не «разрушение». Обычно игнорируется его восстановительная функция, которую нарушают многие используемые нами лекарственные средства. Например, при экземе топические глюкокортикоиды вызывают истончение кожи кистей, и для восстановления ее нормальной толщины потребуются месяцы.
Исключая серьезные нарушения (как, например, при инверсном акне переполненный содержимым канал со слабыми стенками), восстановление быстро завершается, и все возвращается обратно к норме. Роль Р. acnes как сторожа иммунной системы выполнена. И только если что-то пойдет совсем не так, постоянное повреждение приведет к сильной, разрушительной воспалительной реакции.
б) Патогенетическое значение P.acnes. Мы гораздо больше знакомы с Р. acnes в качестве патогена, то есть для излечения заболевания необходимо устранить этот неблагоприятный агент. За последние 60 лет изобрели тетрациклин, эритромицин, доксициклин, миноциклин, лимециклин, азитромицин, сульфаниламиды с или без триметоприма, клиндамицин, кларитромицин, ампициллин, амоксициллин, ципрофлоксацин и даже рифампицин. Несмотря на такую агрессивную борьбу, мы до сих пор встречаем термин антибиотикорезистентное акне, обычно он встречается при вульгарном акне.
Если взять розацеа, то в таком списке будут метронидазол, неомицин, фузидовая кислота (Фузидиевая кислота), мупироцин, азелаиновая кислота, ретапамулин. Сделав еще один шаг вперед к инверсному акне (гнойному гидрадениту) (ИА/ГГ), мы увидим расширение списка за счет длительно действующих системных «ядерных» препаратов, включающих рифампицин, моксифлоксацин и метронидазол. Трудно поверить, что под таким натиском выживет какая-либо бактериальная инфекция. Однако только у 16 из 28 пациентов с ИА/ГГ достигается полная ремиссия при одновременном приеме до 12 мес трех антибактериальных препаратов. Мы до сих пор еще не знаем, что случится, когда лечение будет остановлено у тех 16 успешно вылеченных счастливых пациентов. Но мы можем угадать.
Что заставляет Р. acnes превращаться из кроткого комменсала в «патоген», способный разрушать лица, спины и души? И почему не работает наша самая агрессивная антибактериальная терапия? Вероятно, имеется четыре фактора, которые поддерживают функцию Р. acnes, и еще один, несмотря на опубликованные и указывающие на это данные, полностью игнорируется.
Во-первых, Р. acnes переходит из нейтрального состояния и действительно приступает к делу только в анаэробной (без кислорода) или микроаэрофильной (низкое содержание кислорода) среде. Так как же возникает такая бескислородная среда на здоровом лице подростка, полного жизни и энергии молодости, которое имеет хорошо развитую сосудистую сеть и снабжается всеми питательными веществами и метаболитами, необходимыми для поддержания и восстановления нормальных процессов? Возможно, но это не доказано, ответ заключается в том, что просто доступно слишком много всего хорошего.
Увеличение уровня инсулиноподобного фактора роста 1 [insulin-likegrowth factor 1 (IGF-1)], инсулина и экзогенных андрогенов в дополнение к эндогенным стероидам и эндогенному пубертатному IGF-1 приводит к избыточной стимуляции кератиноцитов фолликулярного канала. В фолликуле возникает пробка: внутреннее давление в пределах фолликулярного канала приводит к нарушению поступления питательных веществ, и особенно кислорода. Недостаточное количество нутриентов, поступающих в эту область, мешает нормальному протеканию метаболических процессов в кератиноцитах.
Возникающая одновременно с этим аноксия обеспечивает прекрасное место для роста Р. acnes. Р. acnes, питающиеся в таких анаэробных условиях за счет жирных кислот себума, усиленно размножаются до того момента, пока их колонии не достигнут настолько крупных размеров, что будут с легкостью видны на микроскопическом срезе. Когда перенапряженный фолликул прорывается или разрывается, популяция Р. acnes возрастает на несколько порядков, становясь мощнейшим стимулом для врожденной иммунной системы. Вот что зажигает пожар при вульгарном акне.
Во-вторых, Р. acnes обладают генетически обусловленной способностью поддерживать большое количество функций. Их ферментативные способности не слишком видны, когда микроорганизмы незаметно «бездействуют» в канале. В условиях гипоксии, когда происходит сдавление стенок переполненного и перерастянутого канала, Р. acnes способны ожить в полностью анаэробной среде. Происходит избирательное задействование широкого спектра генетически обусловленных метаболических функций.
Это показывает, какие изменения приводят к формированию полностью активного репродуктивного фенотипа микроорганизма, происходят при возникновении анаэробных или микроаэрофильных условий, которые данный микроорганизм предпочитает. Это может проявляться различными деструктивными способами.
Изменения затрагивают признаки, связанные с вирулентностью и адаптацией, такие как транспортная система и пути метаболизма, а также кодирование возможных вирулентных факторов, как адгезии дерматансульфат, изомераза полиненасыщенных жирных кислот, железосвязывающий белок HtaA и липаза GehA. Автор утверждает, что «потенциальная патогенность различных штаммов Р. acnes зависит не только от содержания генома определенного филотипа, но и от различной экспрессии генов».
В-третьих, в том, что происходит такой беспорядок, нет настоящей вины Р. acnes. В то время как геном обеспечивает значительный потенциал для разрушения, в дерме и гиподерме под базальной мембраной также возникает реакция на попавшие сюда множественные вещества. Это и непосредственные стимуляторы врожденной иммунной системы, и медленнее действующие, но все же очень мощные антигены адаптивной иммунной системы, которые она должна идентифицировать, на них среагировать и их нейтрализовать.
В-четвертых, требуется серьезное понимание того, что за стимуляцию иммунной системы несется совместная ответственность. Не только не учитывается наличие другого крупного микроорганизма фолликулярного канала, но даже попытки устранить бактериальную активность удивительным образом увеличили влияние другого участника, молчаливого товарища Р. acnes, дрожжеподобного грибка Malassezia.
- Рекомендуем далее ознакомиться со статьей "Дрожжеподобный гриб Malassezia как причина акне (прыщей)"
Оглавление темы "Причины появления прыщей.":- Propionibacterium acnes (P. acnes) как причина акне
- Дрожжеподобный гриб Malassezia как причина акне (прыщей)
- Стафилококки и стрептококки как причина акне (прыщей)
- Клещи Demodex как причина акне (прыщей)
- Пушковые волосы как причина акне (прыщей)
- Приобретенный иммунитет как причина акне (прыщей)
- Воспаление как причина акне (прыщей)
- Медиаторы как причина акне (прыщей)
- Аллергия как причина акне (прыщей)
- Пигментация и рубцевание после прыщей (акне)

