Естественное старение кожи - причины, механизмы, гистология (патогенез, морфология)
Старение кожи включает два отдельных феномена. Естественное старение — универсальные, предположительно неизбежные изменения, связанные только с течением времени; фотостарение — накладывается на естественное старение и связано с изменениями в результате хронического воздействия солнца, которое не является ни универсальным, ни неизбежным. Внешнее старение кожи обычно называют фотостарением, подчеркивая этим большую и хорошо изученную роль хронического воздействия солнца. Первый феномен изначально проявляется едва заметными физиологическими изменениями с несомненно важными последствиями как для здоровой, так и больной кожи.
Второй феномен имеет множество морфологических и физиологических проявлений и соотносится более тесно с признаками постаревшей кожи в популярном смысле этого понятия.
Возрастные изменения кожи приводят к ее постепенному физиологическому угасанию. Основные, связанные с возрастом изменения внешнего вида кожи, включают сухость (огрубение), морщинистость, дряблость и разнообразные доброкачественные новообразования. Состарившаяся кожа неэластична и значительно дольше восстанавливается после повреждений.
а) Механизмы естественного старения кожи. Согласно основной теории старения, суммарное повреждение биомолекул, включая ДНК, в результате постоянного образования свободных радикалов приводит к повышению уязвимости клеток и в итоге к старению или апоптозу. Кожа, как и любая другая система организма, постоянно подвергается воздействию активных форм кислорода (АФК), образующихся в процессе аэробного метаболизма. Хотя кожа содержит сеть антиоксидантных ферментов (супероксид дисмутаза, каталаза и глутатион пероксидаза) и неферментные антиоксидантные молекулы (витамин Е, коэнзим Q10, аскорбат, каротиноиды), эта система не является абсолютно эффективной, а с возрастом имеет тенденцию к еще большему снижению функционирования.
Оксидативный стресс повышает уровень стресс-регулируемых белков, включая фактор, индуцируемый гипоксией (HIFs) и ядерный фактор кВ (NFkB). Индуцируемые гипоксией факторы (ИГФ) влияют на экспрессию генов, регулирующих метаболизм, выживание и подвижность клетки, целостность клеточной мембраны, ангиогенез, гематопоэз и другие функции. Как ИГФ так и ядерный фактор кВ (NF кВ) индуцируют экспрессию провоспалительных цитокинов, таких как, интерлейкин (ИЛ)-1 и ИЛ-6, фактор роста эндотелия сосудов (VEGF), фактор некроза опухолей-а (TNF-a). Эти белки участвуют в иммунорегуляции и определяют выживание клеток стимулируют экспрессию разрушающих матрикс металлопротеинов и, по современным представлениям, играют главную роль в процессе старения.
Кроме того, ИГФ стабилизируют субпопуляции злокачественных клеток со свойствами стволовой клетки (раковых стволовых клеток) и индуцируют их самообновление, стимулируя экспрессию сигнальных механизмов, важных для выживания и пролиферации. Это указывает на возможное участие «возрастной» гипоксии клеток в поддержании популяции раковых стволовых клеток.
Оксидативное повреждение также затрагивает теломеры. Согласно недавно предложенной гипотезе существует общий клеточный сигнальный путь, активизирующийся при повреждении ДК1К и затрагивающий конечные части теломер. Конечная часть из 3’-конца теломерного участка протягивается за комплементарный 5’ конец, оставляя один скрученный и богатый G-повторами конец ДНК. Предполагается, что и при укорочении теломера, и при восстановлении повреждения теломера, происходящих в результате оксидативного стресса, нормальная петлевидная структура на конце теломер обрывается, открывая 3’ участок ДНК, который в норме «похоронен» в петлевидной структуре. Открытие повторяющейся последовательности тандема TTAGGG, по-видимому, затем приводит к активации р53 и стимулирует р53 зависимые ответы, которые, как известно, включают пролиферативное старение и апоптоз.
Таким образом, естественное старение кожи включает прогрессивный оксидативный стресс и теломерную сигнализацию, так как теломеры укорачиваются в результате серии клеточных делений и в ответ на оксидативные повреждения ДНК.
Оксидативное повреждение воздействует также на клеточные белки, что приводит к образованию многочисленных карбонильных групп (С=0). На разрушение таких белков типично направлены протеасомы, функция которых с возрастом угасает, что приводит к накоплению поврежденных белков, препятствующих адекватному функционированию клеток.
Еще один механизм, который участвует в процессе старения кожи, — это старение клеток и ограничение способности клеток к делению. Существует мнение, что этот механизм развился в многоклеточных организмах для предупреждения рака. Для стареющих клеток характерны критически короткие теломеры, необратимая остановка роста, устойчивость к апоптозу и изменение дифференцировки. Такие клетки избыточно экспрессируют гены, блокирующие прогрессирование клеточного цикла, а также гены, кодирующие белки, в частности фибронектин, и протеазы, участвующие в модуляции внеклеточного матрикса, такие как коллагеназа и стромелизин. Кроме того, понижаются уровни некоторых тканевых ингибиторов матриксных металлопротеиназ (ММП).
К дополнительным механизмам относится аминокислотная рацемизация, процесс замещения в белках D-аминокислот L-аминокислотами, что влияет на функцию белков и делает их менее подверженными деградации. Наконец, при химической конденсации альдегидов редуцирующих сахаров с белковыми аминогруппами происходит неферментативное гликозилирование белков, что приводит к коричневой окраске, утрате функции и изменениям в деградации. Гликозилирование белков внеклеточного матрикса, таких как коллаген дермы, приводит к перекрестным соединениям с захватом и секвестированием других непораженных белков.

б) Старение эпидермиса. Многие морфологические и функциональные возрастные изменения в коже описаны много лет назад и поэтому подробно здесь не рассматриваются. Наиболее заметным и стойким гистологическим изменением является ослабление дермально-эпидермального соединения со сглаживанием как сосочков дермы, так и эпидермальных тяжей, что приводит к значительному уменьшению площади поверхности между эпидермисом и дермой, снижению коммуникативного процесса и питания. Показано, что дермально-эпидермальное расслоение легче происходит в старой коже, что однозначно объясняет склонность такой кожи к разрывам и образованию поверхностных ссадин в результате незначительного травмирования.
В период от 30 до 80 лет происходит истончение эпидермиса на 10—50%. Нарастают различия в толщине эпидермиса и размере отдельных кератиноцитов, включая клетки базального слоя. Согласно имеющимся данным, эпидермальные кератиноциты стареют, а стареющие клетки более устойчивы к апоптозу. Следовательно, такие кератиноциты с большей вероятностью аккумулируют мутации, что приводит к увеличению риска их злокачественной трансформации. Эпидермальные стволовые клетки—это популяция клеток, ответственных за поддержание функции эпидермиса. Пока неизвестно, уменьшается ли популяция стволовых клеток эпидермиса с увеличением возраста. В некоторых исследованиях показана утрата постаревшей кожей популяции стволовых клеток эпидермиса, что подтверждается утратой клеток, экспрессирующих признанные маркеры стволовых клеток кератиноцитов, а именно CD7 (рецептор трансферрина) и α6-интегрин, в то время как в других исследованиях констатируется, что, в отличие от стволовых клеток других тканей, стволовые клетки эпидермиса с возрастом сохраняют свой количественный состав и функциональность, и количество РФК в них не возрастает.
Это объясняется высокими уровнями антиоксидантных ферментов, в частности супероксиддисмутазы. При электронной микроскопии защищенная от воздействия солнца старая кожа характеризуется некоторым расширением пространств между кератиноцитами из-за раздвоения плотной пластинки (lamina densa) и закрепления фибрильного комплекса в зоне базальной мембраны, а также потери множества микроворсинчатых выступов цитоплазмы базальных клеток в дерму.
Средняя толщина и степень компактизации рогового слоя, по-видимому, с возрастом не меняются, хотя отдельные корнеоциты становятся крупнее. Характер поверхности кожи («мозаика» тонких линий, видимо, опосредованная архитектурой сосочков дермы) с возрастом становится менее правильным. У пожилых людей отмечается общее понижение содержания липидов в роговом слое, а также пониженное содержание воды, частично в результате уменьшения синтеза холестерина. Возрастное увеличение концентрации pH в роговом слое тормозит активность участвующих в липидном обмене ферментов. Влияние возраста на кожную абсорбцию отчасти зависит от структуры всасываемых веществ, при этом гидрофильные препараты, такие как гидрокортизон и бензойная кислота, абсорбируются старой кожей хуже, чем молодой, а гидрофобные препараты, такие как тестостерон и эстрадиол, абсорбируются одинаково хорошо.
Видимо, большее клиническое значение имеет тот факт, что старение серьезно влияет на восстановление барьерной функции рогового слоя при повреждениях, очевидно, из-за медленного замещения нейтральных липидов, приводящего к снижению количества липидов во вновь формирующихся ламеллярных тельцах. С возрастом снижается синтез липидов и активность ферментов, ответственных за образование липидов рогового слоя, что, видимо, связано с аберрациями в элементах, регулирующих транскрипцию, или с нарушениями передачи аутокринных/паракринных сигналов.
У пожилых людей кожа часто выглядит сухой и шелушащейся, особенно на нижних конечностях, где связанное с возрастом снижение содержания филлагрина в эпидермисе наиболее заметно. Количество филлагрина, необходимого для объединения кератиновых филаментов в макрофибрилы, также снижается при вульгарном ихтиозе. Считается, что недостаток филлагрина приводит к повышенному образованию чешуек при обоих состояниях. Такие структурные изменения также могут влиять на барьерную функцию кожи.
Уровни эпидермального обмена и индекс включения тимидиновой метки снижаются приблизительно на 30-50% между третьим и восьмым десятилетиями жизни наряду с соответствующим удлинением цикла обновления рогового слоя. Уровни линейного роста также снижаются для волос и ногтей. Интенсивность репаративных процессов в эпидермисе с возрастом сходным образом снижается.
Доказано, что на каждое десятилетие жизни приходится приблизительно 10-20% снижение числа ферментативно активных меланоцитов от оставшейся популяции клеток, что, по всей видимости, приводит к ослаблению защитного барьера кожи по отношению к УФ излучению. Возрастное уменьшение способности ДНК к репарации связано также с утратой защитного меланина и повышением риска развития рака кожи. Также с возрастом отмечается прогрессивное снижение числа меланоцитных невусов, количество которых максимально (от 15 до 40 штук у одного человека) на третьем и четвертом десятилетии жизни, а у человека старше 50 лет имеется в среднем четыре таких невуса, которые у лиц старше 80 лет наблюдаются очень редко.
В возрасте ранней и поздней зрелости на 20-50% уменьшается количество морфологически идентифицируемых эпидермальных клеток Лангерганса, эффекторных иммунных клеток кожи, ответственных за презентацию антигенов. Оставшиеся клетки имеют морфологические отклонения, включающие снижение количества и укорочение дендритов, а также обладают сниженной антиген-представляющей активностью. Эти изменения, дополняемые снижением продукции цитокинов кератиноцитами и лимфоцитами и ухудшением миграции через лимфатическую систему, по всей видимости, вносят вклад в наблюдающееся возрастное снижение иммунной реактивности кожи.
С возрастом ухудшается и эндокринная функция эпидермиса человека — синтез витамина D. Витамин D при соединении с ядерным рецептором запускает транскрипцию множества генов. Недостаток витамина D приводит к развитию остеопороза, а также, как стало известно в последнее время, вносит вклад в возникновение диабета, артериальной гипертензии и многих опухолей. Кроме его хорошо изученной роли в гомеостазе кальция, витамин D, связываясь со своим ядерным рецептором (1,25D-VDR), влияет на транскрипцию многочисленных генов, в том числе кодирующих белки в сигнальном механизме Wnt, влияющем на образование ороговевшего эпителия, а также на рост волос. Рецептор 1,251)-VDR активирует также гены, кодирующие белки, которые участвуют в реакциях врожденного и адаптивного иммунитета, и подавляет ИЛ-17, главный индуктор аутоиммунных заболеваний, таких как сахарный диабет типа 1, рассеянный склероз, волчанка и ревматоидный артрит.
1,25D-VDR оказывает также противовоспалительное действие, поскольку понижает активность NFkB и СОХ2. И наконец, рецептор 1,25D-VDR индуцирует активность опухолевых супрессоров, белков р53 и р21, и активность FoxO, препятствуя оксидативному повреждению и индуцируя в коже ферменты репарации ДНК. У пожилых людей уровень витамина D в сыворотке крови часто снижен, что приводит к остеомаляции, то есть недостаточной минерализации костей, связанной с гиповитаминозом D. Хотя нехватка витамина D у пожилых бесспорно является следствием ряда факторов, включающих отказ от молочных продуктов (основной пищевой источник витамина Д), недостаточное пребывание на солнце и использование солнцезащитных средств, установлено, что в периоды ранней и поздней зрелости уровень эпидермального 7-дегидрохолестерола на участок поверхности кожи линейно снижается приблизительно на 75%.
Соответственно предполагается, что недостаток этого непосредственного биосинтетического предшественника может ограничивать синтез витамина D. Все эти наблюдения в совокупности указывают, что возрастное уменьшение содержания витамина D может ускорять процесс старения, и обосновывают применение добавок витамина D в диету пожилых людей.
Что касается уязвимости к оксидативному стрессу, то с возрастом происходит прогрессирующее накопление поврежденных белков и липидов. Более того, активность антиоксидантных защитных систем с возрастом снижается и, кроме того, снижается способность восстановления поврежденной ДНК. Комбинация этих процессов увеличивает мутагенность клеток и/или их тенденцию к старению.

в) Старение дермы. Истончение дермы у пожилых достигает 20%, однако в защищенных от солнца областях выраженное истончение происходит только после 80 лет. Старая кожа относительно бедна клетками и сосудами, и в ней происходит связанная с возрастом потеря нормальных эластических волокон и дермального коллагена.
Ослабление воспалительных реакций у пожилых является результатом снижения синтеза и секреции цитокинов кератиноцитами и воспалительных медиаторов, а также нарушения эндотелиального ответа. Микрососуды дермы у людей среднего возраста и пожилых также могут обнаруживать легкое утолщение стенок, особенно на нижних конечностях в результате действия гравитации; в коже очень пожилых людей происходит истончение сосудистой стенки более чем на половину по сравнению с молодым возрастом, что связанно с отсутствием или уменьшением количества периваскулярных вуалевидных клеток. Видимо, это обусловливает ломкость сосудов. Уменьшение содержания эластина определяет ригидность сосудов. Исследования, проведенные с помощью электронной микроскопии, выявили фокальную дегенерацию эластического компонента артериол дермы. Предполагается, что в основе многих физиологических нарушений в коже пожилых людей, включая бледность, пониженную температуру и приблизительно 60% снижение базального и пикового кровотока в коже, лежит выраженная, связанная с возрастом, потеря васкулярной сети, особенно вертикальных капиллярных петель, находящихся в дермальных сосочках у молодых людей, а также увеличение расстояния от эпидермиса до оставшихся петель.
VEGF эпидермального происхождения, по-видимому, играет важную роль в поддержании кровоснабжения дермы, индуцируя экспрессию анти-апоптических белков в эндотелиальных клетках, а сниженный уровень VEGF в коже пожилых, видимо, приводит к апоптозу эндотелиальных клеток. Также, согласно последним данным, происходит возрастное снижение уровня и ангиогенных, и анти-ангиогенных факторов, нарушающих кожный ангиогенный гомеостаз. Сниженная проницаемость эндотелиальных клеток и сниженная способность вызывать адгезию лейкоцитов приводят к нарушению иммунного ответа. При воздействии высокой или низкой температуры сосуды пожилых людей обнаруживают сниженную способность к сужению, расширению или шунтированию кровотока. Нарушенная терморегуляция, которая иногда приводит пожилых к тепловому удару или фатальной гипотермии, отчасти может быть связана со снижением вазоактивности артериол дермы, а также потерей подкожной жировой клетчатки. Разрежение сосудистой сети, окружающей волосяные фолликулы и экзокринные, апокринные и сальные железы, может приводить с возрастом к постепенной атрофии и фиброзу этих структур.
Показано, что связанное с возрастом снижение резорбции волдырей и клиренса кожи, вызванное трансэпидермально абсорбируемыми веществами, видимо, является результатом изменений как сосудистого русла, так и внеклеточного матрикса. Напротив, время, необходимое для развития пузырей с напряженной покрышкой после местной аппликации гидроксида аммония у пожилых приблизительно в два раза больше, чем у молодых, что говорит о снижении с возрастом уровня транссудации. В нескольких исследованиях подтверждено нарушение трансфера клеток и растворов между внесосудистым и внутрисосудистым пространством дермы, что несомненно зависит от многих факторов.
С возрастом отмечается снижение плотности и просвета лимфатических сосудов, сопровождающееся их повышенной ригидностью, а также ослаблением лимфатического дренажа в результате очевидного снижения количества эластических волокон в окружающих тканях. Способность эффективно перекачивать лимфу из интерстициальных пространств в лимфатическую систему с возрастом нарушается, частично из-за понижения активности ферментов, катализирующих производство окиси азота.
Биохимические изменения коллагена, эластина и основного вещества дермы приводят к повышению ригидности кожи, что, прежде всего, определяется изменениями коллагена. Содержание коллагена на единицу поверхности кожи у взрослого человека снижается приблизительно на 1% в год, а оставшиеся коллагеновые фибриллы дезорганизуются, компактизируются и гранулируются, а также обнаруживают увеличение количества поперечных связей коллагена. Последние являются результатом уменьшения синтеза коллагена I и III типов, снижения ферментного процессинга коллагена, а также неферментного гликозилирования, процесса, ведущего к молекулярному повреждению белков с длительным периодом полураспада, таких как, например, коллаген; а также повышения уровня коллагеназ. Такие изменения несомненно вносят вклад в ухудшение заживления ран у пожилых людей.
Начиная с раннего взрослого периода, уменьшается число эластических волокон и их диаметр. К старости они часто становятся фрагментированы, имеют небольшие пузырьки и лакуны, особенно в области дермо-эпидермального соединения, что происходит в результате ферментной деградации эластина. С возрастом эластические волокна также обнаруживают образование поперечных связей и признаки кальцификации. На биохимическом уровне с возрастом отмечается снижение содержания многих компонентов эластических волокон, таких как эластин, фибриллин и фибулин-2. С возрастом отмечается снижение уровня фибулина-5, белка внеклеточного матрикса, выполняющего роль каркаса для эластических волокон. Исходя из этого, предлагается рассматривать фибулин-5 в качестве маркера кожного старения.
Содержание мукополисахаридов, глюкозаминогликанов (GAG) и протеогликанов основного вещества, снижается как по отношению к сухому веществу кожи, так по отношению к коллагену, что особенно касается гиалуроновой кислоты. Видимо, это связано со сниженной секрецией гиалуронана или сниженной экстрагируемостью гиалуроновой кислоты. Возраст также влияет на состав GAG и связывание с эластином, задерживая дренаж молекул в лимфатические сосуды. Эти изменения могут снижать тургор кожи, так как протеогликаны связывают массу воды в 1000 раз большую своего веса, а также влияют на депонирование, ориентацию и размер коллагеновых волокон.
Изменения механических свойств кожи с возрастом включают прогрессирующую потерю упругого восстановления, что соотносится с постепенным разрушением эластической сети дермы и выраженным удлинением периода, необходимого для восстановления исходной толщины кожи после иссечения. При ультразвуковых исследованиях in vivo выявлены связанные с возрастом различия в распределении воды в дерме, бесспорно влияющие на пластичность, упругость и эластичность кожи. В целом картина возрастных изменений в дерме включает возрастающую ригидность, потерю эластичности и лабильности с замедлением реакций на повреждение и стресс.
д) Естественное старение подкожно-жировой клетчатки, старение мышц и костей. Наряду с остальными поперечно-полосатыми мышцами, мышцы лица накапливают «возрастной пигмент» липофусцин, маркер повреждения клеток. Наряду со снижением нервно-мышечной регуляции это вносит вклад в формирование морщин. Кроме того, на определенных участках лица, таких как лоб, около-глазничные, щечные, височные и околоротовые области, подкожно-жировая клетчатка истончается. Напротив, отмечается выраженное накопление жировой ткани в других областях, таких как подбородочная, челюстные области, носогубные складки и латеральная скуловая область. В отличие от лица молодых, где жир диффузно распределен, жир у взрослого человека под действием гравитации вносит вклад в провисание и дряблость кожи.
Наконец, как и в других частях скелета, в костях лицевого черепа с возрастом происходит редукция костной массы. Костной резорбции преимущественно подвержены нижняя и верхняя челюсть и лобные кости. Потеря костной ткани в этих областях усиливает провисание кожи и приводит к стиранию границ контура межу нижней челюстью и шеей, такой отчетливой у молодых.
е) Старение кожных желез, нервов. Количество эккринных желез большинства областей тела у взрослых постепенно снижается приблизительно на 15% от среднего числа. Спонтанное потоотделение уменьшается у здоровых взрослых по сравнению с молодыми людьми на 70%, что, прежде всего, связано с меньшим объемом продуцируемого каждой железой пота и является предрасполагающим фактором к развитию теплового удара у пожилых. Размер и функция апокриновых желез также с возрастом снижаются. Размер и число сальных желез, по-видимому, с возрастом не меняются, однако отмечается экспоненциальное снижение продукции кожного сала как у мужчин, так и у женщин, что, по всей вероятности, обусловлено снижением выработки андрогенов половыми железами или надпочечниками.
Количество телец Пачини и Мейсснера — кожных органов, ответственных за восприятие ощущения давления и легкого прикосновения, прогрессивно снижается между вторым и девятым десятилетиями жизни приблизительно на 1/3 их изначальной средней плотности, что сопровождается значительной вариабельностью размеров и неоднородностью структуры.
Сниженное сенсорное восприятие старой кожи охватывает ощущения легкого прикосновения, чувства вибрации и способность различать две ближайшие точки и их положение в пространстве. С возрастом на 20% повышается порог болевой чувствительности кожи, а нарушенная констрикция артериол при смене горизонтального положения на вертикальное отражает сниженный ответ симпатической нервной системы.
ж) Влияние климакса (менопаузы) на старение кожи. Эстрогены играют решающую роль в женском развитии и репродукции, а также оказывают влияние на кожу и волосы. Неудивительно, что после менопаузы их влияние резко снижается. В типичных случаях менопауза наступает в начале пятого десятка жизни, и учитывая, что ожидаемый возраст жизни женщин в развитых странах составляет 80 лет, в постменопаузе они проводят приблизительно одну треть жизни. У женщин в пременопаузе преобладающим эстрогеном является эстрадиол, продуцируемый яичниками, и его уровень после наступления менопаузы снижается более чем на 90%, так что в дальнейшем преобладает менее активный эстроген—эстрон. Уровни прогестина и андрогена после наступления менопаузы также сильно снижаются. Снижение уровня эстрогена лежит в основе многих физиологических явлений, включая приливы жара, атрофию репродуктивной ткани и изменения в нерепродуктивных эстроген-чувствительных тканях.
Связанное с возрастом снижение барьерной функции кератиноцитов, иммунорегуляции и заживления ран, по-видимому, являются следствием падения уровня эстрогенов и/или ослабления ответа клеток на имеющиеся эстрогены. Поскольку и эстрогеновые, и андрогенные рецепторы экспрессируются на выделенных из кожи клетках, по-видимому, оба гормона играют роль в формировании структуры и функции кожи.
Структурные и функциональные изменения кожи в постменопаузе. Снижение уровня циркулирующих эстрогенов ассоциировано с уменьшением содержания коллагена в дерме, повышением растяжимости кожи и снижением ее эластичности. Также в постменопаузе отмечаются сниженная способность удерживать воду, повышенная сухость и увеличение количества тонких морщин, а также снижение уровня кожного сала. Эти изменения в большей степени связаны с менопаузой, нежели с хронологическим старением самим по себе, а образование морщин более выражено у женщин в постменопаузе, не принимающих заместительную гормональную терапию, по сравнению с женщинами, получающими гормоны.
После менопаузы ухудшение процесса заживления ран связано со снижением содержания коллагена I типа. Известно, что эстроген и прогестерон также модулируют воспаление в коже, ускоряя пролиферацию кератиноцитов и синтез коллагена, снижая активность матриксных металлопротеиназ (ММР) и повышая синтез дермальных мукополисахаридов и гиалуроновой кислоты.
з) Причины ускорения естественного старения кожи. Курение сигарет ускоряет процесс фотостарения, особенно у женщин, при этом наблюдается прямая корреляция числа выкуренных в год пачек сигарет с выраженностью морщин и сероватой окраской кожи. При гистологическом исследовании в «коже курильщика» выявляется утолщение и фрагментация эластических волокон, что сходно с гистологической картиной поврежденной солнцем кожи.
Однако в то время как в поврежденной солнцем коже эластоз ограничивается сосочковым слоем дермы, изменения эластических волокон в коже курильщика происходят также и в сетчатом слое дермы. Предполагается, что такой эластоз дермы является результатом повышенной активности эластазы нейтрофилов, хронической ишемии дермы и проокислительных эффектов курения сигарет, дополняемых сниженными уровнями витамина А, что уменьшает способность сдерживать активные формы кислорода и увеличивает повреждения ДНК. Также курение связано со снижением содержания в роговом слое воды и ускоренным гидроксилированием эстрадиола, что приводит к снижению содержания эстрогенов в коже и в свою очередь может вносить вклад в развитие ее сухости и атрофии.
У курильщиков отмечается низкая способность к заживлению ран и повышенная заболеваемость раком кожи, а также повышение степени тяжести изменений, подобных изменениям при фотостарении по сравнению с некурящими с аналогичными другими факторами риска, что обусловлено наличием в дыме сигарет мутагенов, напрямую влияющих на клетки дермы и эпидермиса. Усиливая оксидативный стресс, сигаретный дым нарушает синтез коллагена и индуцирует синтез и выделение матриксных металлопротеиназ. К тому же полициклические ароматические углеводороды, которые присутствуют в сигаретном дыме, связываются с арил-гидрокарбоновым рецептором в цитоплазме.
При активации этот рецептор транслоцируется в ядро и индуцирует транскрипцию генов, кодирующих метаболизирующие ксенобиотики ферменты, а также белки, контролирующие рост клетки, цитокины, факторы ядерной транскрипции и регуляторы протеолиза внеклеточного матрикса.
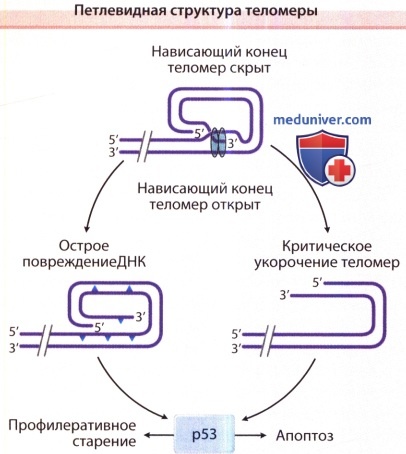
Теломера в норме представляет собой петлевидную структуру, фиксированную 150--200 основаниями (TTAGGG повторами) на 3'-конце, который образует одноцепочечный нависающий фрагмент.
Если петля разрывается, теломера критически укорачивается (например, в результате повторных клеточных делений или в результате повреждения тело-меры УФ излучением или окислительным процессом),
нависающий участок становится открытым, что активизирует опухолевый супрессор, белок р53, вызывающий в зависимости от типа клеток полиферативное старение или апоптоз.
IL = интерлейкин.
- Рекомендуем далее ознакомиться со статьей "Естественное старение волос - причины, механизмы (патогенез)"
Оглавление темы "Старение кожи.":- Причины и механизмы старения кожи (патогенез)
- Естественное старение кожи - причины, механизмы, гистология (патогенез, морфология)
- Естественное старение волос - причины, механизмы (патогенез)
- Фотостарение кожи - признаки, механизмы (патогенез)
- Связь болезней кожи с возрастом человека
- Опухоли кожи пожилых - типы, признаки
- Заболевания кожи пожилых - типы, признаки

