Лечение лангергансоклеточного гистиоцитоза (ЛКГ)
Стратегия лечения лангергансоклеточного гистиоцитоза выбирается на основании возраста пациента, распространенности заболевания и локализации поражений.
При поражении одной системы — кожи или костной — лечение неагрессивное. У детей только с поражением кожи можно ограничиться наблюдением. Для лечения ограниченных очагов могут использоваться препараты местного действия, в том числе кортикостероиды (в том числе для внутриочаговых инъекций), такролимус и имиквимод. При выявлении изолированного поражения кожи у взрослых может оказаться эффективной терапия хлорметином. У одного пациента с локализованной формой ЛКГ полное исчезновение проявлений было достигнуто после проведения 12 серий узковолновых УФ-В с кумулятивной дозой 970 мл/см.
Значительное улучшение в значительном числе случаев наблюдалось после ПУФА-терапии. Для лечения эозинофильной гранулемы вокруг естественных отверстий было предложено применение углекислого лазера. Системные кортикостероиды или антимикотические препараты при ограниченном поражении показаны только при наличии резистентности к лечению. Применение талидомида в дозе 100 мг/сут. в течение месяца, а затем 50 мг/сут. в течение 1-2 месяцев может приводить к ремиссии. Обычно после прекращения лечения болезнь рецидивирует.
Представляется, что эффект талидомида является результатом иммуномодулирующих и противовоспалительных свойств этого препарата. В одном случае полная ремиссия поражений кожи была достигнута после перорального приема изотретиноина. Пациент получал 1,5 мг/кг/сут. препарата в течение восьми месяцев, а рецидив и поражения органов не возникли в течение пяти лет. При доступности поражений методом выбора у пациентов с изолированным поражением костей является удаление или выскабливание. У детей инъекции глюкокортикоидов в избранные места могут предотвратить хирургическую травму, нарушающую развитие зубов или рост плоских или длинных костей.
У взрослых при вовлечении позвоночника, турецкого седла и опорных костей с риском спонтанного перелома показана лучевая терапия. Недавно были получены данные, указывающие, что индометацин в ежедневной дозе 1-2,5 мг/кг при применении на протяжении в среднем 7,7 месяцев (диапазон от 5 до 12 месяцев) может оказаться эффективным для лечения изолированного ЛКГ костной ткани у детей. У детей лучевая терапия должна остаться в резерве на случай отсутствия ответа на другие методы для предотвращения риска длительных побочных эффектов. В случае множественных поражений костей, как и при мультиорганном поражении, рекомендуется монохимиотерапия.
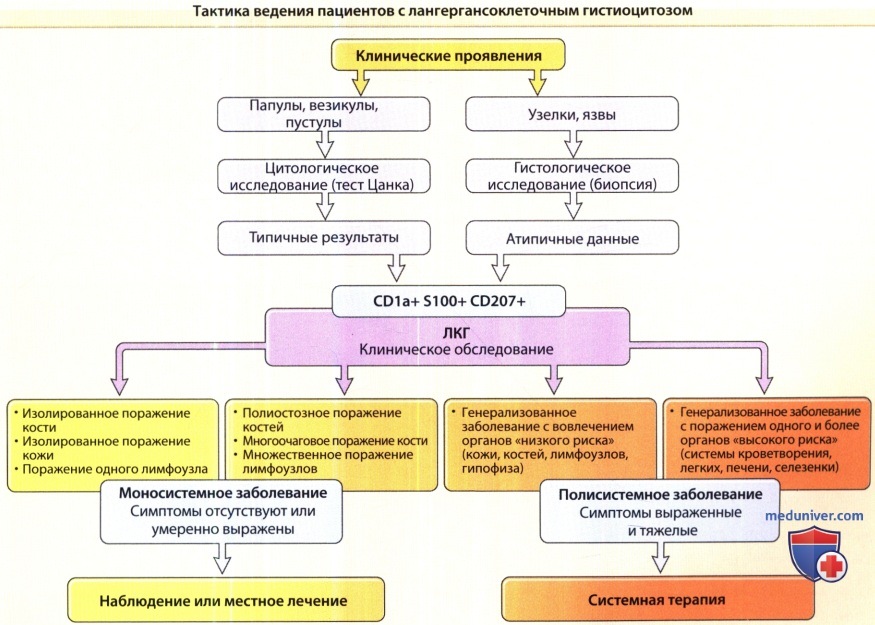
При полисистемном заболевании есть несколько подходов к лечению болезни. В настоящее время наиболее подходящим лечением является, видимо, монохимиотерапия винбластином или этопозидом с глюкокортикоидами, или без них. Винбластин вводится внутривенно в дозах 0,1-0,2 мг/кг (6,5 мг/м2) один раз в неделю в течение 1-3 месяцев. Повторное назначение алкалоида должно проводиться только при появлении новых поражений. В случае рецидива назначается повторный курс монохимиотерапии, что приводит к полному излечению в 60% случаев.
И, наконец, в качестве стартового метода лечения может служить метилпреднизолон (30 мг/кг внутривенно на протяжении 3 дней подряд).
При неэффективности монохимиотерапии следует рассмотреть возможность многокомпонентной терапии, включающей винкристин, циклофосфамид, доксорубицин и хлорамбуцил. В случаях рефрактерной и далеко зашедшей ЛКГ применялись циклоспорин и интерферон-а2, а также 2-хлордезоксиаденозин (2-ХдА, кладрибин). Кладрибин высокоактивен у пациентов с ЛКГ, хотя ответ различается в различных группах риска. Согласно недавно полученным данным, монотерапия кладрибином в значительной степени эффективна у пациентов с поражением, не представляющим угрозы для жизни, например, при вовлечении костной ткани, но характеризуется ограниченной активностью при рефрактерном течении болезни. В большом проспективном исследовании единственными прогностическими факторами ответа на терапию кладрибином были возраст на момент проведения терапии и время от установления диагноза до применения кладрибина.
Ответ на лечение и выживаемость были достоверно лучше у пациентов старше двух лет, а время от установления диагноза до применения кладрибина также существенно отличалось у ответивших пациентов по сравнению с теми, кто не ответил на лечение. Вероятность развития серьезных побочных эффектов при применении кладрибина (транзиторная нейтропения, абсолютная моноцитопения, супрессия Т-клеток, аутоиммунная гемолитическая анемия и выраженное поражение кожи) требует тщательного анализа соотношения «риск-польза» в каждом конкретном случае. Пациенты из группы высокого риска, которые не отвечают на терапию кладрибином, характеризуются высокой вероятностью летального исхода. В настоящее время в открытом пилотном исследовании Общества по изучению гистиоцитоза изучают возможность улучшения ответа у пациентов с рефрактерным ЛКГ с помощью добавления цитозина арабинозида (Ara-С) к кладрибину.
В некоторых случаях успех приносила аллогенная трансплантация костного мозга или аутогенная трансплантация очищенного от CD1a костного мозга. Также исследуются и другие подходы, в том числе трансплантация стволовых клеток с использованием миелоаблативной и немиелоаблативной подготовки.
Дополнительно рекомендуемая литература по лангергансоклеточному гистиоцитозу (ЛКГ):
1. Jaffe R et al: Histiocytic and dendritic cell neoplasms, introduction. In: WHO Classification of Tumors of Haematopoietic and Lytnpoid Tissues, edited by SH Swerdlow et al. Geneva, Lyon, WHO Press, 2008.
2. Favara BE et al: WHO Committee on Histiocytic/Reticulum Cell Proliferations, Reclassification Working Group of the Histiocyte Society. Contemporary classification of histiocytic disorders. Med Pediatr Oncol 29(3): 157-166, 1997.
3. Satter EK, High WA: Langerhans cell histiocytosis: A review of the current recommendations of the Histiocyte Society. Pediatr Dermatol 25(3):291-295,2008.
4. Bidre E et al: Extensive, erosive congenita] self-healing cell histiocytosis. J Eur Acad Dermatol Venereol 23:835-862,2009.
5 Madrigal-Martinez-Pereda C et al: Langerhans cell histiocytosis: Literature review and descriptive analysis of oral manifestations. Med Oral Patol Oral Cir Bucal 14(5): E222-E228,2009.
6. Shima H, Takahashi T, Shimada H: Protein-losing enteropathy caused by gastrointestinal tract-involved Langerhans cell histiocytosis. Pediatrics 125(2): e426-e432,2010.
7. Allen CA, Flores R, Rauch R: Neurodegenerative central nervous system langerhans cell histiocytosis and coincident hydrocephalus treated with vincristine/cytosine arabinoside. Pediatr Blood Cancer 54:416-423,2010.
8. Ertan G, Huisman ТА: Susceptibility-weighted imaging in neurodegeneration in Langerhans cell histiocytosis. / Pediatr 156(6): 1032, 2010.
9. Battistella M et al: Neonatal and early infantile cutaneous langerhans cell histiocytosis: Comparison of selfregressive and non-self-regressive forms. Arch Dermatol 146(2): 149-156,2010.
10. Weitzman S et al: 2’-Chlorodeoxyadenosine (2-CdA) as salvage therapy for Langerhans cell histiocytosis (LCH). Results of the LCH-S-98 protocol of the Histiocyte Society. Pediatr Blood Cancer 53(7):1271-1276,2009.
- Вернуться в оглавление раздела "дерматология."
Редактор: Искандер Милевски. Дата публикации: 6.1.2019

