Цитокин фактор некроза опухоли (ФНО) и его рецепторы
ФНО-а является прототипом семейства сигнальных молекул, проявляющих свое биологическое действие через семейство соответствующих рецепторных молекул. ФНО-а был первоначально выделен на основании его двух интересных биологических эффектов: (1) геморрагического некроза злокачественных опухолей и (2) ассоциированной с воспалением кахексии.
Хотя ФНО-а осуществляет многие из своих важных биологических эффектов в качестве растворимой молекулы, заново синтезированный ФНО-а существует на клеточной поверхности в форме трансмембранного белка. Специфическая металлопротеиназа, известная как конвертирующий ФНО-а фермент (ТАСЕ), ответственна за большую часть ФНО-а, секретированного Т-клетками и миелоидными клетками. Ближайшим родственником ФНО-а является ФНО-β, известный также как лимфо-токсин-а (LT-а).
К другим родственным молекулам в семействе ФНО относятся лимфотоксин β (LT-β), который связывается с LT-a, образуя гетеродимер LT-a1β1, Fas-лиганд (FasL) родственного ФНО и вызывающего апоптоз лиганда (TRAIL), а также индуцированный активацией родственный ФНО цитокин (TRANCE) и лиганд CD40 (CD 154). Хотя некоторые из этих членов семейства ФНО традиционно не считаются цитокинами, их структура (все они являются мембранными протеинами типа II с внутриклеточным N-концевым и внеклеточным С-концевым элементами) и сигнальные механизмы схожи с аналогичными для ФНО.
Растворимые формы ФНО-а, LT-а и Fas-лиганда являются гомодимерами, а доминирующая форма LT-β представляет собой мембранный гетеродимер LT-а1β1. Тримеризация членов семейства ФНО их тримерными лигандами необходима для инициации сигнала и экспрессии биологической активности.
Первоначальное изучение свойств рецепторов ФНО привело к открытию двух рецепторных белков, способных связывать ФНО-a с высокой аффинностью. Рецептор ФНО р55 (TNFR1) отвечает за большинство биологических свойств ФНО, а рецептор р75 (TNFR2) способен также проводить сигналы (в отличие от IL1R2, который служит исключительно биологическим «отстойником» для ИЛ-1).
TNFR1 и TNFR2 имеют достаточно протяженные участки близкой гомологии, и оба присутствуют в большинстве типов клеток. Тем не менее между ними имеются значительные различия.
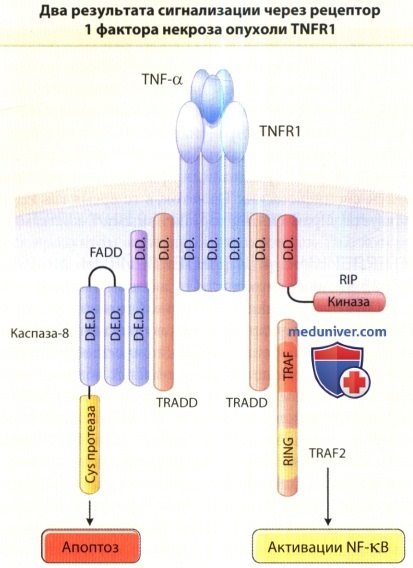
Вовлечение TNFR1 в действие тримерным фактором некроза опу-холи-a (ФНО-а) может запустить механизм апоптоза и/ или активации нуклеарного фактора кВ (NF-kB).
В обоих процессах участвует ассоциированный с TNFR домен смерти адаптерного белка (TRADD), который связывается CTNFR1 посредством взаимодействий между «доменами смерти» (DD) на обоих белках.
Для активации NF-kB требуются ассоциированный cTNFR фактор 2 (TRAF2) и взаимодействующий с рецептором белок (RIP).
Апоптоз индуцируется, когда содержащий домен смерти белок адаптера (Fas-ассоциированного белка домена смерти или FADD) взаимодействует с TRADD.
FADD также содержит «домен эффектора смерти» (D.E.D.), который взаимодействует с каспазой 8, чтобы инициировать процесс апоптоза.
Cys = цистеин.
В отличие от цитокиновых рецепторов для некоторых других крупных семейств, в сигнализации ФНО не участвует путь Jak/STAT. В клетках ФНО-а вызывает два типа реакций: (1) провоспалительные и (2) вызывающие индукцию апоптотической гибели клеток. Провоспалительное действие ФНО-а, которое включает стимуляцию экспрессии молекул адгезии и индукцию вторичных цитокинов и хемокинов, происходит в большей степени благодаря активации NF-кВ и может передаваться как через TNFR1, так и через THFR2.
Индукция апоптоза посредством сигнала через TNFR1 зависит от региона, известного как домен смерти, который отсутствует у TNFR2, а также от взаимодействий с дополнительными белками доменов смерти в пределах сигнального комплекса TNFR1. Сигнал, инициированный связыванием лиганда с TNFR1, Fas или другими рецепторами семейства ФНО, содержащими домен смерти, в итоге приводит к активизации каспазы 8 или 10 и изменениям ядра и фрагментации ДНК, характерным для апоптоза.
Как минимум два из семейства рецепторов TNFR (TFNR1 и LT-TFNR1) также содействуют нормальному анатомическому развитию лимфоидной системы. У мышей с дефицитом ФНО-а отсутствуют зародышевые центры и фолликулярные дендритные клетки. Мыши с мутацией TFNR1 имеют те же аномалии, кроме того, у них отсутствуют пейеровы бляшки. При нулевых мутациях в LT-a и LT-β выявляются и другие аномалии в лимфоидном органогенезе, а также неспособность к развитию периферических лимфоузлов.
ФНО-a является важным медиатором кожного воспаления, и его экспрессия индуцируется в ходе почти всех воспалительных реакций в коже. Нормальные ке-ратиноциты человека и линии кератотических клеток синтезируют достаточные количества ФНО-a после стимуляции липополисахаридами или УФ-светом. Кожное воспаление, стимулированное ирритантами и контактными сенсибилизаторами, ассоциируется с активной индукцией производства ФНО-a в кератиноцитах. Воздействие ФНО-a заставляет клетки Лангерганса мигрировать к дренирующим лимфоузлам, что дает возможность сенсибилизировать наивные Т-клетки.
Одним из молекулярных механизмов, который может способствовать вызванной ФНО-a миграции клеток Лангерганса в лимфоузлы, является уменьшение экспрессии молекул адгезии Е-катедрина после воздействия ФНО-a. Индукция рецептора 7 хемокина СС на эпидермальных и дермальных антиген-презентирующих клетках зависит от их перемещения в дренирующую лимфосистему. Из рецепторов TNFR кератины экспрессируют преимущественно TNFR1. Аутокринные сигнальные петли с участием ФНО-a и TNFR1 приводят к производству в кератиноцитах различных, индуцируемых ФНО, вторичных цитокинов.
Центральная роль ФНО-a в воспалительных заболеваниях, включая ревматоидный артрит и псориаз, стала очевидной в результате клинических исследований. Лекарства, действующие на патогенетические механизмы, вовлекающие ФНО, включают гуманизированные анти-ФНО-a антитела (инфликсимаб-infliximab), полностью человеческие анти-ФНО-а антитела (адалумимаб — adalumimab) и растворимый рецептор ФНО (этанерцепт — etanercept). Лекарства этого класса одобрены FDA для терапии многих воспалительных и аутоиммунных заболеваний, таких как болезнь Крона и ревматоидный артрит. Все эти анти-ФНО-препараты одобрены FDA для лечения псориатического артрита, а этанерцепт утвержден для лечения хронического бляшечного псориаза.
Этот класс лекарственных препаратов является потенциально важным и для лечения других воспалительных дерматозов. Парадокс состоит в том, что такие препараты эффективны не во всех случаях аутоиммунных заболеваний — множественный склероз после лечения этими препаратами незначительно ухудшается. Антагонисты ФНО являются сильнодействующими иммуномодулирующими лекарственными средствами, поэтому при их применении требуется соответствующая осторожность. При лечении антагонистами ФНО случаи кожной Т-клеточной лимфомы, вначале считавшиеся случаями псориаза, быстро прогрессировали в фульминантное заболевание. Антагонисты ФНО также способствуют выходу латентных микобактериальных инфекций из-под контроля иммунной системы с угрозой летального исхода заболевания.
- Рекомендуем далее ознакомиться со статьей "Цитокины семейства ИЛ-17"
Оглавление темы "Цитокины иммунологии кожи.":- Пути передачи сигнала цитокинами кожи
- Нуклеарный фактор кВ (NF-kB), ингибитор кВ и первичные цитокины кожи
- Участие белков JAT и STAT в пути сигнала
- Цитокины семейства интерлейкинов-1: ИЛ-1, ИЛ-18, ИЛ-33
- Цитокин фактор некроза опухоли (ФНО) и его рецепторы
- Цитокины семейства ИЛ-17
- Семейство рецепторов гемотопоэтина (семейство рецепторов хемокинов класса I)
- Цитокины интерлейкин-2 (ИЛ-2) и интерлейкин-15 (ИЛ-15)
- Цитокины интерлейкин-4 (ИЛ-4) и интерлейкин-13 (ИЛ-13)
- Цитокины интерлейкин-9 (ИЛ-9) и интерлейкин-21 (ИЛ-21)

