Механизм развития (патогенез) холангиокарциномы
Холангиокарцинома, вторая по частоте (после ГЦК) злокачественная опухоль печени, представляет собой новообразование, развивающееся из желчных протоков, расположенных как внутри печени, так и вне ее. Холангиокарцинома является причиной 7,6% смертей от онкологических заболеваний во всем мире и 3% смертей в США. Распространенность заболевания в США различна: наибольшая частота отмечается среди испаноязычных американцев (1,22 случая на 100 тыс. человек), а наименьшая — среди лиц с темным цветом кожи (0,17-0,5 случая на 100 тыс. человек).
Факторами риска развития холангиокарциномы являются первичный склерозирующий холангит, врожденная фиброполикистозная болезнь желчных путей (в частности, болезнь Кароли и кисты общего желчного протока), вирусный гепатит С и предшествующее воздействие торотраста (контрастного вещества, ранее использовавшегося при визуализации желчных протоков). Однако большинство холангиокарцином в странах Запада развивается вне связи с указанными состояниями.
В Юго-Восточной Азии, где распространенность холангиокарциномы выше, основным фактором риска является хроническое инфицирование желчных путей печеночной двуусткой О. sinensis и другими представителями класса трематод.
В зависимости от локализации холангиокарциномы подразделяют на внутрипеченочные и внепеченочные. От 80 до 90% холангиокарцином являются внепеченочными. Тем не менее за последние 20 лет в США, странах Западной Европы и Японии растет частота внутрипеченочных форм опухоли, тогда как заболеваемость внепеченочными формами остается постоянной. К внепеченочным опухолям относят перихилярные опухоли (опухоли Клацкина), которые локализуются в области ворот печени, в зоне слияния правого и левого печеночных протоков (50-60%), а также опухоли дистальных желчных протоков (20-30%). Последние локализуются в непосредственной близости от ампулы фатерова сосочка.
Опухоли этой области также включают аденокарциному слизистой оболочки двенадцатиперстной кишки и рак поджелудочной железы и рассматриваются совместно как периампулярные карциномы.
Прогноз внепеченочной опухоли независимо от ее локализации неблагоприятный: 2-летняя выживаемость после постановки диагноза составляет всего 15%. Период от диагностирования до летального исхода при внутрипеченочной форме составляет в среднем 6 мес даже после хирургического вмешательства. Внутрипеченочные холангиокарциномы обычно обнаруживают на поздних стадиях заболевания и только после появления симптомов нарушения оттока желчи или при обнаружении объемного новообразования в печени. Перихилярные и дистальные опухоли проявляются симптомами обструкции желчных протоков, холангита и болью в правом подреберье.
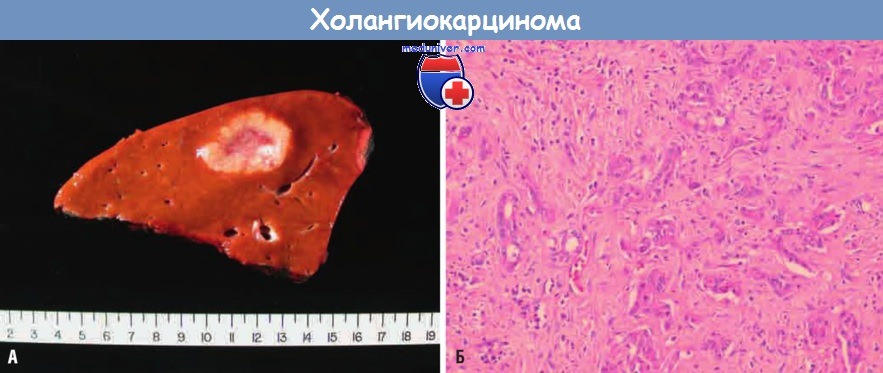
(А) Крупная опухоль, расположенная в правой доле печени, с множественными метастазами по всему органу (аутопсийный препарат).
(Б) На микропрепарате видны тубулярные железистые структуры, окруженные плотной склерозированной стромой.
Морфология. Внепеченочные холангиокарциномы к моменту постановки диагноза обычно имеют небольшой размер. Большинство опухолей представляют собой плотные сероватые узелки в стенке желчного протока. Некоторые могут диффузно инфильтрировать стенку протока, другие имеют вид сосочковых или полиповидных образований. Большинство опухолей являются аденокарциномами, иногда с выраженными признаками слизеобразования. Редко присутствуют признаки плоскоклеточной дифференцировки. Практически всегда определяется хорошо выраженная фиброзная строма, окружающая эпителиальный компонент.
Опухоли Клацкина обычно растут медленнее, чем холангиокарциномы других локализаций, при этом в них выявляются выраженные фиброзные изменения, а отдаленные метастазы развиваются нечасто.
Внутрипеченочные холангиокарциномы развиваются в нецирротической печени и могут распространяться вдоль внутрипеченочной системы портальных трактов, формируя древовидные опухолевые структуры. Иногда формируются массивные опухолевые узлы. В любом случае характерны сосудистая инвазия и распространение опухоли по воротным лимфатическим сосудам, что приводит к распространенным внутрипеченочным метастазам. При микроскопическом исследовании холангиокарциномы напоминают аденокарциномы других органов с любым вариантом строения.
Большинство опухолей являются высокодифференцированными или умеренно дифференцированными склерозированными аденокарциномами с хорошо выраженными железистыми и тубулярными структурами, выстланными кубическим или низким цилиндрическим эпителием. Эти опухоли в основном являются десмопластическими и характеризуются наличием плотной коллагеновой стромы, разделяющей железистые структуры. По этой причине опухоль обычно имеет очень плотную консистенцию и зернистую структуру. В 50% случаев при аутопсии выявляют метастазы в лимфатические узлы и гематогенные метастазы в легкие, кости (главным образом в позвоночник), надпочечники, головной мозг или другие органы. Возможен смешанный вариант, когда присутствуют элементы как ГЦК, так и холангиокарциномы.
Различают 3 формы смешанного варианта:
(1) одновременно присутствуют отдельные опухолевые узлы ГЦК и холангиокарциномы;
(2) «сливающаяся» опухоль (образуется в результате слияния опухолевых масс ГЦК и холангиокарциномы с четким разграничением между ними);
(3) опухоль, у которой элементы ГЦК и холангиокарциномы перемешаны на микроскопическом уровне.
Такие «смешанные» опухоли встречаются редко, однако при тщательном микроскопическом исследовании холангиокарциномы достаточно часто выявляют мелкие фокусы гепатоцеллюлярной дифференцировки.
ГЦК и холангиокарцинома могут развиваться из общей бипотенциальной клетки-предшественника (овальной клетки), способной трансформироваться как в гепа-тоциты, так и в эпителиальные клетки желчных протоков.
Патогенез. В патогенез холангиокарциномы вовлечены несколько сигнальных путей. Среди них — гиперэкспрессия IL-6, которая приводит к активации АКТ и антиапоптотического белка MCL-1. Также при холангиокарциноме увеличивается экспрессия СОХ-2, ERB-2 и с-МЕТ. По данным различных исследований, экспрессия KRAS увеличивается в 20-100% наблюдений, при этом в * 40% наблюдений экспрессия гена р53 снижается. Другие нарушения заключаются в амплификации EGFR, снижении экспрессии регуляторов клеточного цикла и гена-супрессора опухолей р16/INK4А.
В настоящее время для повышения точности диагностики в дополнение к гистологическому исследованию используют флуоресцентную гибридизацию in situ со специальными маркерами на EGFR, а также цифровой анализ плоидности опухолевых клеток. Хирургическое вмешательство является единственно возможным и эффективным методом лечения.
- Рекомендуем ознакомиться со следующей статьей "Механизм развития (патогенез) метастатических опухолей печени"
Оглавление темы "Патогенез заболеваний печени":- Механизм развития (патогенез) поражения печени при эклампсии и преэклампсии
- Механизм развития (патогенез) острой жировой дистрофии печени беременных
- Механизм развития (патогенез) холестаза беременных
- Механизм развития (патогенез) узловой гиперплазии печени
- Механизм развития (патогенез) гемангиом печени
- Механизм развития (патогенез) аденомы печени
- Механизм развития (патогенез) гепатобластомы
- Механизм развития (патогенез) рака печени
- Механизм развития (патогенез) холангиокарциномы
- Механизм развития (патогенез) метастатических опухолей печени

